Гиперваскуляризация щитовидной железы что
Узелки щитовидной железы: что делать врачу
Почти у каждого второго человека можно выявить один или несколько узелков в щитовидной железе. В поле зрения клинициста попадают узелки, найденные при физикальном осмотре или самим пациентом, а также те, которые были выявлены случайно при проведении лучевых исследований по другому поводу (например, УЗИ сонных артерий, КТ головы и шеи, ПЭТ). Самая важная тактическая задача врача в этой ситуации – исключить рак щитовидной железы, встречающийся у 4-7% пациентов, обратившихся за консультацией по поводу выявленного узелка.
Непальпируемые узелки (инсиденталомы) имеют такую же вероятность оказаться раком, как и пальпируемые узелки такого же размера. Поэтому начальное обследование, вне зависимости от того, пальпируется ли узелок, должно включать в себя физикальный осмотр, измерение уровня ТТГ и УЗИ щитовидной железы.
Физикальное обследование обладает низкой прогностической ценностью в отношении рака щитовидной железы. Однако некоторые факты анамнеза могут насторожить в отношении этой патологии – к ним относятся быстрый рост образования на шее, перенесенная лучевая терапия на область головы и шеи, семейный анамнез рака щитовидной железы и опухолевых синдромов (MEN2, FAP, синдром Cowden). Физикальные находки несмещаемой плотной опухоли, симптомы обструкции дыхательных путей и паралич голосовых связок также крайне подозрительны в отношении рака щитовидной железы.
При пониженном уровне ТТГ существует вероятность, что узел гормонально активен. В таком случае следует выполнить сцинтиграфию щитовидной железы.
При нормальном или повышенном ТТГ и показаниях к пункции по данным УЗИ следующий шаг – тонкоигольная биопсия узла. Дополнительно к этому, пациентам с низким ТТГ необходимо обследование для поиска причины гипотиреоза.
Сцинтиграфия щитовидной железы используется для оценки функционального статуса узелка. Понижение ТТГ увеличивает вероятность того, что найденный узел гиперфункционирует. Так как такие «горячие» узлы очень редко являются злокачественными, нет необходимости их пунктировать. Нефункционирующие узлы – выглядят «холодными», то есть захватывают радиофармпрепарат слабее, чем окружающая ткань; для них может потребоваться биопсия. Автономные узлы выглядят «горячими» (захватывают РФП сильнее, чем окружающая паренхима), если они гиперфункционируют. Такие узлы составляют всего 5-10% от всех пальпируемых, крайне редко оказываются злокачественными, и поэтому не требуют биопсии. Узлы неопределенного характера: так как сцинтиграфия – двухмерное исследование, из-за наложения окружающей паренхимы железы невозможно определить функциональное состояние многих, особенно мелких, узелков; такие результаты исследования тоже не исключают необходимости тонкоигольной биопсии.
УЗИ щитовидной железы
Метод позволяет определить размер узла, анатомию железы и других структур шеи, включая лимфоузлы; он гораздо более информативен, чем КТ, сцинтиграфия и физикальный осмотр.
Существуют сонографические признаки, подозрительные в отношении злокачественности узла. Однако их предсказательная ценность широко варьируется, и лишь на основании УЗ-картины невозможно выставить показания к хирургическому лечению. Однако, данные УЗИ можно использовать для отбора пациентов на биопсию.
УЗ-признаки, ассоциированные с различной вероятностью злокачественности узелка. Также в последние годы в практику активно внедряется шкала TIRADS, позволяющая стандартизовать заключения диагностов и достигнуть высокой воспроизводимости результатов.
Тонкоигольная аспирационная биопсия
Показания по результатам УЗИ — накапливаются доказательства, что наличие подозрительной УЗ-картины имеет большую предсказательную ценность в отношении рака щитовидной железы, чем просто размер узелка.
Тонкоигольной биопсии подлежат все узелки, вне зависимости от размеров, со следующими свойствами:
Субкапсулярно расположенные и прилегающие к возвратным нервам или трахее
Выходящие за пределы капсулы органа
Любые узелки при наличии шейной лимфаденопатии
«Выпячивание» тканей узелка за ободок кальцификатов
Узелки менее 5 мм трудно пропунктировать, перед биопсией такого узелка стоит обсудить с пациентом риск неинформативного исследования и ложноотрицательного результата.
Также биопсии подлежат узелки размером от 1 см в наибольшем измерении, если они солидные или гипоэхогенные, и обладают одним или более из следующих признаков:
Преобладание переднезаднего размера («высоты») над латеральным («шириной»)
Также возможность биопсии стоит рассмотреть у некоторых пациентов с семейным анамнезом рака ЩЖ, опухолевыми синдромами, анамнезом облучения головы и шеи в детском возрасте, или у предпочитающих биопсию наблюдению. Однако, большинство пациентов с подозрительными субсантиметровыми узелками можно наблюдать.
Узелки с сонографической картиной, характерной для группы низкого риска (изоэхогенные, гиперэхогенные, частично кистозные без подозрительных находок в солидном компоненте можно подвергнуть биопсии при достижении ими размера в 1,5-2 см.
Полностью кистозные узелки без солидного компонента стенок не требуют биопсии.
Наблюдение за узелками, не попадающими под критерии для биопсии
Частота контрольных обследований зависит от УЗ-характеристик узелка. Одна из допустимых схем наблюдения:
1 раз в 6-12 месяцев для субсантиметровых узелков с подозрительными характеристиками;
1 раз в 1-2 года для узелков низкого и среднего риска;
1 раз в 2-3 года для узелков очень низкого риска.
В дальнейшем период между исследованиями можно увеличить при стабильности размеров узлов.
Кистозные узелки — подавляющее большинство таких узелков являются доброкачественными дегенерирующими аденомами. Однако, раки щитовидной железы тоже могут быть кистозными. Как и для солидных, для кистозных узелков наличие подозрительных признаков на УЗИ имеет большую предсказательную ценность в отношении ЗНО, чем сам по себе размер узла.
Выбор оптимального лечения зависит от морфологических характеристик узелка и его функционального статуса.
Цитологическое исследование — результаты тонкоигольной биопсии оцениваются по шкале Bethesda, включающей 6 категорий результатов, каждый из которых требует разного подхода к лечению.
Результаты цитологического исследования оцениваются по стандартизованной системе Bethesda, имеющей 6 категорий результатов, каждому из которых соответствуют своя вероятность наличия злокачественной опухоли в узелке.
Им проводят периодический УЗ-мониторинг, сначала раз в 1-2 года, а затем – раз в 2-5 лет, при необходимости сокращая интервал для больших узелков и при наличии подозрительной УЗ-картины, или удлиняя для меньших узелков с классическими УЗ-признаками доброкачественного процесса. При наличии подозрительной УЗ-картины возможно повторное проведение ТАБ через 12 месяцев, если по результатам предыдущей получено заключение о доброкачественности.
Небольшие изменения размера узла в динамике не являются показанием к повторной ТАБ. Однако, рекомендуется повторная пункция в следующих сценариях:
Значительный рост (более чем на 50% в объеме или 20% в диаметре, при условии, что рост в двух измерениях не менее 2 мм)
Появление новых подозрительных в отношении ЗНО признаков в узелке
Новые симптомы, связанные с узелком
При повторном доброкачественном результате ТАБ дальнейшее наблюдение за узелком с помощью УЗИ не нужно.
Неопределенная цитология (Bethesda III и IV) — При получении цитологического ответа о наличии фолликулярного образования/атипии неопределенного значения (FLUS/AUS) или фолликулярного новообразования, результат исследования считается неопределенным. Дальнейшая диагностика и лечение таких узелков включает в себя повторную ТАБ, молекулярно-генетическое исследование, в некоторых случаях – хирургическое лечение.
Подозрение на ЗНО (Bethesda V) — в эту диагностическую категорию попадают образования с признаками характерными, но недостаточными для диагноза папиллярного рака ЩЖ. Вероятность наличия рака или неинвазивного фолликулярного образования (NIFTP) у таких пациентов около 50-75%, их необходимо направить на хирургическое лечение.
Злокачественное образование (Bethesda VI) — в эту категорию включены папиллярный, медуллярный и анапластический рак, лимфома щитовидной железы и метастазы опухолей других органов. Таким пациентам также необходимо хирургическое лечение.
Для доказанной морфологически папиллярной микрокарциномы, не выходящей за пределы органа при отсутствии поражения лимфоузлов и признаков низкой дифференцировки, альтернативой операции является активное наблюдение, в особенности для коморбидных пациентов. Однако, предоперационный диагноз папиллярной микрокарциномы редок при следовании вышеописанным рекомендациям для биопсии.
Неинформативный (Bethesda I) — важно, что отсутствие злокачественных клеток в пунктате не может считаться отрицательным результатом биопсии, если при процедуре не было получено достаточного количества фолликулярной ткани. В этом случае предлагается повторить ТАБ через 4-6 недель, используя УЗИ-наведение.
При повторной неинформативной цитологии стоит рассмотреть проведение трепанобиопсии под УЗИ. В исследовании на пациентах с предыдущей неинформативной ТАБ, при трепанобиопсии диагностически значимый результат был получен в 74 процентах случаев, в то время как при повторной ТАБ – лишь в 52%; после двух неинформативных ТАБ, аналогичные показатели составили 86 и 29%.
Хирургическое удаление, в особенности для больших солидных узелков с подозрительными УЗ-признаками, или наблюдение (особенно – для меньших, частично кистозных узелков), являются разумными опциями ведения для пациентов с повторно неинформативными результатами биопсий.
Devita, Hellman, and Rosenberg’s Cancer : principles & practice of oncology—10th edition
Haugen BR, Alexander EK, Bible KC, et al. 2015 American Thyroid Association Management Guidelines for Adult Patients with Thyroid Nodules and Differentiated Thyroid Cancer: The American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. Thyroid 2016; 26:1.
Хронический аутоиммунный тиреоидит (ХАИТ)
Удовиченко Олег Викторович
врач-эндокринолог
Синонимы – тиреоидит Хашимото, зоб Хашимото.
Что такое хронический аутоиммунный тиреоидит
Это хроническое воспаление щитовидной железы, вызванное ошибочной выработкой антител против нее.
Причины заболевания хроническим аутоиммунным тиреоидитом
ХАИТ относится к большой группе аутоиммунных заболеваний, это их типичный представитель.
Их суть заключается в том, что иммунная система по ошибке начинает вырабатывать антитела против белков собственного организма. Причиной является, с одной стороны, врожденная склонность иммунной системы к таким ошибкам, а с другой — встреча с вирусом, белки которого похожи на белки клеток щитовидной железы.
Для ХАИТ характерна наследственная предрасположенность. Заболевание встречается значительно чаще у женщин, чем у мужчин.
Стадии протекания хронического аутоиммунного тиреоидита
Их можно выделить лишь условно.
На первом этапе в крови обнаруживается повышенный уровень антител к щитовидной железе, но ее активного разрушения антителами не происходит (это так называемые здоровые носители антител). Среди женщин в определенных возрастных группах распространенность такого носительства достигает 20%.
У части пациентов все же начинается процесс разрушения ткани щитовидной железы антителами, но железа при этом нормально выполняет свою функцию по выработке гормонов (и их уровень в крови остается нормальным)
У части пациентов железа все же повреждается антителами настолько, что выработка гормонов снижается и развивается гипотиреоз. Но вероятность этого невелика и составляет 2% в год.
Симптомы хронического аутоиммунного тиреоидита
Если еще не развился гипотиреоз (для которого характерна особая клиническая симптоматика), аутоиммунный тиреоидит обычно на дает выраженных симптомов. Чаще это заболевание выявляется случайно, при обследовании щитовидной железы «на всякий случай».
Но некоторые пациенты описывают дискомфорт в области щитовидной железы (передней поверхности шеи).
Лечение хронического аутоиммунного тиреоидита у взрослых и детей
Важно понимать, что лечение самого по себе ХАИТ не проводится. На сегодняшний день медицина не располагает высокоэффективными, безопасными и одновременно не очень дорогими средствами лечения аутоиммунных заболеваний.
Общий принцип лечения аутоиммунных болезней — подавление активности иммунной системы.
При ХАИТ потенциальный вред от подобного лечения превышает вред от гипотиреоза.
Поэтому общепринятым подходом, рекомендуемым как мировыми, так и отечественными экспертами, является периодический (примерно 1 раз в год) контроль уровня гормонов щитовидной железы для исключения их дефицита.
Если их дефицит (гипотиреоз) все же развивается — в постоянном режиме проводится заместительная терапия, прием основного гормона щитовидной железы в таблетках.
Как происходит лечение ХАИТ в клинике «Рассвет»
Несомненно, рекомендуемый ведущими экспертами подход к лечению этой болезни применяют и эндокринологи нашей клиники.
При этом мы не делаем ненужных анализов и не назначаем необоснованно частых посещений эндокринолога. Например, нет необходимости регулярно контролировать уровень антител к ткани щитовидной железы («АТ к ТПО»), для которого свойственны волнообразные колебания с течением времени. Нередко приходится наблюдать, что эндокринологи, не знающие о рекомендуемых принципах лечения ХАИТ, назначают средства с сомнительной эффективностью, но аргументируют это тем, что у части больных после их применения уровень антител к ткани щитовидной железе становится ниже.
При этом мы помним, что многие жалобы, похожие на симптомы заболеваний щитовидной железы, бывают вызваны дефицитом железа, депрессией или тревожными состояниями. В подобной ситуации эти заболевания нужно активно выявлять и лечить, что действительно улучшает самочувствие пациента.
Рекомендации клиники «Рассвет» больным ХАИТ
Хронический аутоиммунный тиреоидит — заболевание с относительно благоприятным течением, хотя есть некоторые его последствия, которые надо вовремя выявить (гипотиреоз).
Необходимо помнить, о том, что не все изменения в самочувствии, которые беспокоят пациента, обязательно вызваны состоянием щитовидной железы. Поэтому важно не пропускать другие заболевания, которые также могут требовать лечения.
Ультразвуковая оценка васкуляризации узловых образований щитовидной железы
ФГБУ «Федеральный медицинский биофизический центр им. А.И. Бурназяна» ФМБА России
E-mail:
РЕФЕРАТ: В статье проанализирован опыт комплексного ультразвукового исследования объемных образований щитовидной железы у 249 пациентов, подвергшихся оперативному вмешательству.
По распространенности в популяции узловые образования доминируют в структуре тиреоидной патологии, особенно в эндемичных районах, составляя 40-50% всех заболеваний щитовидной железы. Клиническая значимость узловой патологии щитовидной железы определяется высокой распространенностью рака щитовидной железы, который встречается в 5-10% выявленных узлов 5.
Среди методов лучевой диагностики ведущие позиции занимает ультразвуковое исследование, достоинства которого – простота, неинвазивность, доступность, относительно низкие экономические затраты – сочетаются с высокой информативностью. В большинстве случаев ультразвуковое исследование, дополненное тонкоигольной аспирационной биопсией патологических очагов, является основным методом диагностики узловых образований щитовидной железы 7. Совершенствование ультразвуковых технологий и внедрение в практику методик допплеровского картирования позволили выполнять ультразвуковую ангиографию щитовидной железы, качественно и количественно оценивать особенности ее васкуляризации [7, 10-14]. Вместе с тем, данные литературы относительно взаимосвязи выраженности васкуляризации узла и его злокачественности по-прежнему весьма разнообразны.
Материалы и методы
Диагностические возможности ультразвукового исследования (УЗИ) в выявлении и дифференциальной диагностике узловой патологии щитовидной железы (ЩЖ) проанализированы на основании обследования 249 больных. Результаты УЗИ сопоставлены с интраоперационными данными и верифицированы результатами гистологического исследования удаленной ЩЖ.
Всем пациентам было проведено традиционное клиническое и лабораторное обследование, а также инструментальная диагностика.
Комплексное ультразвуковое исследование щитовидной железы выполнялось по общепринятой методике на ультразвуковых диагностических аппаратах HDI 5000 (ATL, США), Acuson «Sequoia» – 512 (Siemens, Германия), Vivid-7 (GE, США), Voluson-730 Pro (GE, США), мультичастотными датчиками 5-12 МГц с использованием различных режимов сканирования.
В процессе исследования при полипозиционном сканировании в В-режиме оценивались положение, форма, контуры железы, ее эхогенность и эхо-структура, наличие дополнительных образований и локальных участков ткани железы с нарушенной акустической структурой, анатомо-топографические соотношения железы с соседними органами.
При наличии дополнительных образований (узлов) оценивали их количество, локализацию, контуры, эхогенность и эхо-структуру, распространение за капсулу ЩЖ. Всем без исключения больным в обязательном порядке по общепринятой методике осматривались зоны регионарного лимфооттока.
Качественный анализ кровотока в паренхиме железы и узловых образованиях проводили с использованием режимов цветового допплеровского кодирования (ЦДК) и энергетического допплера (ЭД). Для оптимизации цветового изображения использовали индивидуальные настройки параметров аппаратуры: мощность сигнала, частота повторения импульсов, фильтры. Однако сравнительную оценку васкуляризации паренхимы и узловых образований у одного и того же пациента в динамике или у различных пациентов проводили при стандартных настройках ультразвуковых приборов в программах «Thyroid». Качественный анализ кровоснабжения паренхимы щитовидной железы проводили в режиме ЦДК и ЭД, выделяя различную выраженность васкуляризации паренхимы (скудную, обычную, повышенную).
Ангиоархитектонику узловых образований определяли согласно градациям, используемым отечественными и зарубежными авторами [3, 106, 152, 198], и дифференцировали узловые образования с 4 типами сосудистого рисунка.
При изучении интенсивности кровоснабжения, как и в ряде исследований [8, 13, 15], выделяли узлы с интранодулярной гиперваскуляризацией (при наличии выраженной внутриузловой сосудистой сети) и интранодулярной гиповаскуляризацией (с наличием единичных сосудов внутри узла).
При оценке внутриузловой ангиоархитектоники отмечали такие качественные характеристики, как ход сосуда, протяженность, характер сосудистого рисунка, равномерность диаметра сосудов, внутриузловую «насыщенность» сосудами и т.д.
В ряде случаев исследование ангиоархитектоники узловых образований щитовидной железы дополняли трехмерной реконструкцией сосудистого рисунка в режиме энергетического допплера (3D-ангио).
Сравнение выборок, не подчиняющихся нормальному распределению, проводили с использованием методов непараметрической статистики. Такие данные в тексте, таблицах и рисунках представляли в виде Ме (медианы), минимальных и максимальных значений. При сопоставлении двух независимых выборок пользовались критерием Манна-Уитни (T). Для сравнения относительных показателей при анализе качественных переменных использовались критерии z и критерий χ 2 (хи-квадрат) с поправкой Йетса на непрерывность. Критический уровень значимости при проверке статистических гипотез принимался равным 0,05.
Используя принцип решающей матрицы, оценивали показатели диагностических тестов (истинно отрицательные результаты (ИО), истинно положительные результаты (ИП), ложно отрицательные результаты (ЛО), ложно положительные результаты (ЛП)) и информативность данных признаков (чувствительность, специфичность, точность, прогностическая ценность положительного результата, прогностическая ценность отрицательного результата). Указанные статистические показатели рассчитывали по формулам:
Результаты исследования и обсуждение результатов
Среди 249 оперированных пациентов у 49 человек (19,7%) установлен рак ЩЖ, который в 3 случаях сочетался с аденомой, у 41 (16,5%) – аденомы ЩЖ, у 151 (60,6%) – узловой коллоидный пролиферирующий зоб, в том числе в 16 случаях рецидивный, и у 5 (2,0%) – узловая форма аутоиммунного тиреоидита (АИТ). В 1 наблюдении (0,4%) пациенту удалена невринома шеи, в 1 (0,4%) случае – аденома паращитовидной железы и еще у 1 пациентки (0,4%) – аберрантная ЩЖ. В 24,5% наблюдений узловая патология ЩЖ сочеталась с диффузным или диффузно-узловым аутоиммунным тиреоидитом.
Результаты наших исследований, свидетельствующие о наличии узловых образований в ЩЖ, совпали с интраоперационными и морфологическими данными у 239 больных. В 157 (65,7%) наблюдениях обнаружено многоузловое поражение ЩЖ, с наличием от 2 до 9 узлов в каждой доле, и в 82 (34,3%) – одиночные узлы ЩЖ. Пятеро пациентов оперированы по поводу диффузно-узловой формы АИТ, ни при УЗИ, ни на операции других узловых образований у них выявлено не было. Результативность УЗИ в выявлении узловых образований ЩЖ составила: чувствительность – 98,8%, специфичность – 87,5%, точность – 98,4%, прогностическая ценность положительного результата – 99,6%, прогностическая ценность отрицательного результата – 70,0%.
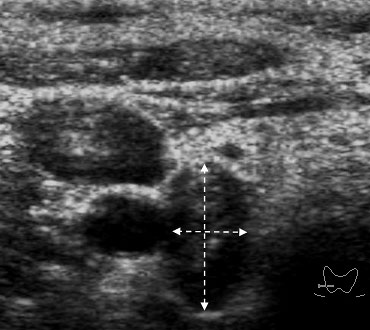
В 5 наблюдениях (2,0%) результаты УЗИ были ошибочны: в одном случае за крупный узел нижнего полюса правой доли ЩЖ принята невринома надключичной области (рис. 1), в другом за гиперплазированные паратрахеальные лимфоузлы – аденома паращитовидной железы (рис. 2). У 3 оперированных больных не распознаны узлы ЩЖ, сформировавшиеся на фоне диффузного зоба или АИТ.
Рисунок 1. Эхограмма невриномы (двусторонняя стрелка) шеи.
Сканирование в режиме ЦДК.
Рисунок 2. Аденома паращитовидной железы (стрелки).
В общей сложности у 239 пациентов проанализированы и сопоставлены с результатами гистологического исследования эхографические характеристики 528 узловых образований ЩЖ. При этом изучались серошкальное изображение узлов и их ангиоархитектоника в режимах ЦДК и ЭД, а при необходимости – в режиме трехмерной реконструкции сосудистого рисунка (3D-ангио). Из 528 узлов 56 (10,6%) соответствовали различным формам рака ЩЖ, 45 (8,5%) – доброкачественным опухолям (фолликулярным аденомам) ЩЖ и остальные 427 (80,9%) – узловому в разной степени пролиферирующему зобу. Результаты сопоставления ультразвукового изображения узловых образований с их морфологическим строением и статистическая значимость полученных данных представлены в таблицах 1-3.
Таблица 1. Размеры узловых образований щитовидной железы
различной морфологической структуры
| Размеры узлов | Морфологическое строение узлов | |||||||
|---|---|---|---|---|---|---|---|---|
| Рак | Аденома | Коллоидные узлы | Итого | |||||
| Кол-во | % | Кол-во | % | Кол-во | % | Кол-во | % | |
| До 10 мм | 16 | 28,6 | 5 | 11,1 | 195 | 45,6 | 216 | 40,9 |
| 11-20 мм | 17 | 30,4 | 15 | 33,3 | 102 | 23,9 | 134 | 25,4 |
| 21-30 мм | 13 | 23,2 | 16 | 35,6 | 66 | 15,5 | 95 | 18,0 |
| 31-40 мм | 5 | 8,9 | 5 | 11,1 | 32 | 7,5 | 42 | 8,0 |
| > 40 мм | 5 | 8,9 | 4 | 14,9 | 32 | 7,5 | 41 | 7,8 |
| Всего | 56 | 100,0 | 45 | 100,0 | 427 | 100,0 | 528 | 100,0 |
Таблица 2. Локализация узловых образований щитовидной железы
различной морфологической структуры
| Размеры узлов | Морфологическое строение узлов | |||||||
|---|---|---|---|---|---|---|---|---|
| Рак | Аденома | Коллоидные узлы | Итого | |||||
| Кол-во | % | Кол-во | % | Кол-во | % | Кол-во | % | |
| Верхний полюс | 14 | 25,0 | 2 | 4,4 | 104 | 24,4 | 120 | 22,3 |
| Средняя треть | 24 | 42,9 | 20 | 44,4 | 141 | 33,0 | 185 | 35,0 |
| Нижний полюс | 10 | 17,9 | 20 | 44,4 | 147 | 34,4 | 177 | 34,0 |
| Перешеек | 8 | 14,3 | 3 | 6,8 | 35 | 8,2 | 46 | 8,7 |
| Всего | 56 | 100,0 | 45 | 100,0 | 427 | 100,0 | 528 | 100,0 |
В структуре опухолевых заболеваний ЩЖ обращает внимание присутствие мелких очагов, размерами менее 10 мм (до 28,6% среди раков и до 11,1 % среди аденом) (табл. 1). Это затрудняло их дифференциацию при полинодозном поражении ЩЖ и обнаружение среди мелких пролиферирующих коллоидных узелков и инциденталом. До 17,8% раковых узлов были представлены крупными очаговыми образованиями, размерами более 30 мм в диаметре, что также было характерно и для узлового пролиферирующего зоба. Зависимости частоты встречаемости рака от размеров узла нами не выявлено (χ 2 =3,70, р=0,448).
Малигнизированные узлы чаще локализировались в средней трети доли, тогда как аденомы преимущественно располагались как в нижнем полюсе, так и в средней трети доли (табл. 2). Эхографические характеристики узловых образований различной морфологической структуры отличались большим разнообразием ультразвуковых признаков, что также затрудняло диагностику злокачественной патологии с помощью УЗИ (табл. 3).
Таблица 3. Ультразвуковые признаки узловых образований щитовидной железы
в сопоставлении с результатами морфологического исследования
| Признаки | Морфологическое строение узлов | Статистическая значимость | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Рак | Аденома | Узловой кол. зоб | |||||||
| Кол-во узлов | % | Кол-во узлов | % | Кол-во узлов | % | χ 2 | р | ||
| Эхогенность | Гипоэхогенность | 40 | 71,4 | 18 | 40,0 | 164 | 38,4 | 7,711 | 0,021 |
| Изоэхогенность | 13 | 23,2 | 19 | 42,2 | 172 | 40,3 | 3,116 | 0,211 | |
| Гиперэхогенность | 2 | 3,6 | 2 | 4,4 | 33 | 7,7 | 1,069 | 0,447 | |
| Смешанная | 1 | 1,8 | 6 | 13,3 | 58 | 13,6 | 5,479 | 0,065 | |
| Итого: | 56 | 100 | 45 | 100 | 427 | 100 | |||
| Границы | Ровные | 24 | 42,9 | 42 | 93,3 | 366 | 85,7 | 8,077 | 0,018 |
| Неровные | 32 | 57,1 | 3 | 6,7 | 61 | 14,3 | 35,948 | 0,0001 | |
| Итого: | 56 | 100 | 45 | 100 | 427 | 100 | |||
| Контур | Четкий | 24 | 42,9 | 43 | 95,6 | 394 | 92,3 | 9,677 | 0,008 |
| Нечеткий | 32 | 57,1 | 2 | 4,4 | 33 | 7,7 | 63,644 | 0,0001 | |
| Итого: | 56 | 42,9 | 45 | 100 | 427 | 100 | |||
| Ободок | Ободок Halo | 6 | 10,7 | 14 | 31,1 | 45 | 10,5 | 10,944 | 0,004 |
| Нет | 50 | 89,3 | 31 | 68,9 | 382 | 89,5 | 1,163 | 0,559 | |
| Итого: | 56 | 100 | 45 | 100 | 427 | 100 | |||
| Структура | Однородная | 14 | 25,0 | 10 | 22,2 | 153 | 35,8 | 2,873 | 0,238 |
| Неоднородная | 42 | 75,0 | 35 | 77,8 | 284 | 66,5 | 18,376 | 0,0001 | |
| Итого: | 56 | 100 | 45 | 100 | 427 | 102,3 | |||
| Кальцинаты | Кальцинаты | 23 | 41,1 | 14 | 31,1 | 27 | 6,3 | 48,497 | 0,0001 |
| Нет | 33 | 58,9 | 31 | 68,9 | 400 | 93,7 | 5,297 | 0,071 | |
| Итого: | 56 | 100 | 45 | 100 | 427 | 100 | |||
| Жидкость | Жидкостные участки | 12 | 21,4 | 9 | 20,0 | 123 | 28,8 | 1,59 | 0,451 |
| Нет | 44 | 78,6 | 36 | 80,0 | 304 | 71,2 | 0,41 | 0,815 | |
| Итого: | 56 | 100 | 45 | 100 | 427 | 100 | |||
| Капсула ЩЖ | Нарушение капсулы ЩЖ | 7 | 12,5 | 0 | 0,0 | 0 | 0,0 | 53,14 | 0,0001 |
| Нет | 49 | 87,5 | 45 | 100 | 427 | 100 | 0,21 | 0,9 | |
| Итого: | 56 | 100 | 45 | 100 | 427 | 100 | |||
| I | 2 | 3,6 | 0 | 0,0 | 22 | 7,5 | 4,124 | 0,125 | |
| II | 3 | 5,4 | 2 | 4,4 | 76 | 25,8 | 14,533 | 0,0001 | |
| III с внутриузловой гиперваскуляри-зацией | 12 | 21,4 | 21 | 46,7 | 77 | 26,1 | 4,847 | 0,089 | |
| III с внутриузловой гиповаскуляри-зацией | 32 | 57,1 | 19 | 42,2 | 108 | 36,6 | 3,271 | 0,195 | |
| IV | 7 | 12,5 | 3 | 6,7 | 12 | 4,1 | 5,544 | 0,063 | |
| Итого: | 56 | 100 | 45 | 100 | 295 | 100 | |||
В процессе ультразвукового обследования пациентов с узловыми образованиями ЩЖ решали несколько диагностических задач, которые определяли дальнейшую хирургическую тактику, в том числе выбор объема операции. Главная из них – определение морфологической структуры обнаруженных очагов тиреоидной паренхимы. При обнаружении злокачественной патологии не менее важно было оценить стадийность заболевания, то есть распространение процесса за пределы ЩЖ. И наконец, в-третьих – выявление всех узловых образований в тиреоидной паренхиме, определение их размеров, пространственного расположения, дифференциация участков неизмененной паренхимы, подлежащих сохранению.
При обнаружении узловых образований в тиреоидной паренхиме в первую очередь дифференцировали их злокачественную или доброкачественную природу.
Ретроспективный анализ показал, что в наших наблюдениях рак ЩЖ чаще встречался при множественном узловом поражении ЩЖ (в 62,5% случаев) и присутствовал в одном или нескольких узлах при многоузловом зобе. Одиночные раковые узлы выявлены в 21 случае (37,5%). Вместе с тем частота встречаемости рака ЩЖ в общей структуре моно- и полинодозного поражения ЩЖ практически не различалась и составляла соответственно 28,6%, и 19,9% (различия статистически не значимы, критерий χ 2 =0,912, р=0,340).
Одновременно несколько раковых очагов в одной или обеих долях гистологически верифицированы у 7 (14,3%) пациентов (у 2 в одной доле и у 5 в обеих долях (рис. 3)), причем в 2 случаях в виде микрофокусов до 3-5 мм в диаметре. В этих 2 наблюдениях (4,1% больных) микрофокусы злокачественных новообразований были предположены при УЗИ и определялись в виде гипоэхогенных участков неправильной формы с неровными контурами, размерами 4-5 мм в диаметре, расположенных в непосредственной близости с «основным» раковым узлом (рис. 4). В остальных 5 наблюдениях дополнительные злокачественные новообразования в тиреоидной паренхиме при УЗИ найдены не были.
Рисунок 3. Узлы папиллярного рака (белые стрелки) в правой доле и левой доле ЩЖ.
Рисунок 4. Узел папиллярного рака (двусторонняя стрелка)
и микрофокус рака (белая стрелка и пунктирные маркеры).
По морфологическому строению преобладали высокодифференцированные раки: 58,9% узлов соответствовали папиллярной карциноме, 26,8% – фолликулярной карциноме. Солидный (папиллярный и фолликулярный) рак встретился в 7,1% узлов, медуллярный – в 5,4% и недифференцированный – в единичном наблюдении (1,8%). В 10 наблюдениях (20,4%, 10/49) раку ЩЖ сопутствовал аутоиммунный тиреоидит с выраженными диффузно-псевдоузловыми изменениями паренхимы ЩЖ, а у 3 (6,1%, 3/49) больных рак ЩЖ сочетался с фолликулярными аденомами.
Стадия Т1-2 верифицирована у 33 (67,3%) больных, Т3 – у 7 (14,3%), Т4 – у 9 (18,4%). Лимфогенное метастазирование на стороне поражения обнаружено у 10,2% пациентов. Отдаленные метастазы в кости скелета были выявлены у одного больного (2,0%).
Раковые узлы несколько чаще локализовались в средней трети долей (42,9% узлов), реже в верхнем полюсе (25,0%), в нижней трети (17,9%) и в перешейке (14,2%) (критерий χ 2 =8,220, р=0,0540). И, как уже отмечалось, практически 1/3 узлов (28,6%) составили очаги менее 10 мм в диаметре (табл. 1, 2).
По сравнению с доброкачественными образованиями для раковых узлов были характерны следующие эхографические признаки: гипоэхогенность узла (71,4%), неоднородность структуры (75,0%), нечеткие неровные контуры (51,7%), более высокая встречаемость микрокальцинатов (41,1%) (таблица 3, рис. 5) Такие признаки были выявлены у 67,9% злокачественных очагов. При узлах менее 20 мм в диаметре «типичное» ультразвуковое изображение рака ЩЖ встретилось в 78,8% наблюдений, а при более крупных узлах (свыше 20 мм в диаметре) – лишь в 36,4%.
Рисунок 5. Узел папиллярного рака (двусторонняя стрелка).
«Типичное» ультразвуковое изображение злокачественного узла ЩЖ.
В 32,1% случаев определялось иное ультразвуковое изображение ракового узла, больше соответствующее коллоидному зобу (рис. 6) или аденоме (рис. 7). Такое «нетипичное» ультразвуковое изображение рака ЩЖ чаще выявлялось среди узловых образований размерами свыше 20 мм в диаметре (52,4%), а также среди фолликулярных аденокарцином, при солидных раках и в случае низкодифференцированного рака ЩЖ. Установлению правильного диагноза в этих случая на дооперационном этапе особенно помогала тонкоигольная аспирационная биопсия.
Рисунок 6. Узел папиллярного рака ЩЖ (двусторонняя стрелка). «Нетипичное»
ультразвуковое изображение злокачественного узла ЩЖ. Панорамное сканирование.
Рисунок 7. Узел папиллярного рака ЩЖ (двусторонняя стрелка). «Нетипичное»
ультразвуковое изображение злокачественного узла в перешейке ЩЖ.
Изучение сосудистого рисунка узловых образований тиреоидной паренхимы не способствовало значимому повышению результативности УЗИ в дифференциальной диагностике рака среди других узловых образований ЩЖ (табл. 4).
Таблица 4. Сравнение информативности серошкального УЗИ
и УЗИ с использованием цветокодирующих методик
| Показатели | Серошкальное УЗИ | Серошкальное УЗИ + цветокодирующие методики | Значения критерия z |
|---|---|---|---|
| Чувствительность | 62,5% | 64,3% | 0.002, р=0.942 |
| Специфичность | 84,5% | 87,7% | 1.327, р=0.185 |
| Точность | 82,2% | 85,2% | 1.336, p=0.216 |
| Прогностическая ценность положительного результата | 32,4% | 38,3% | 0.817, р=0.414 |
| Прогностическая ценность положительного результата | 95,0% | 95,4% | 0.248, р=0.808 |
Для большинства (78,5%) раковых узлов была характерна смешанная перинодулярная и внутриузловая ангиоархитектоника с преобладанием внутриузловой гиповаскуляризации, что не отличало их от трети коллоидных узлов и половины аденом (табл. 3, рис. 8). Рассчитанный критерий χ 2 для частоты встречаемости III типа сосудистого рисунка среди раков, аденом и узловых коллоидных узлов составил χ 2 =2,790, р=0,248.
Рисунок 8. Узел папиллярного рака ЩЖ (двусторонняя стрелка).
Сосудистый рисунок узла в режиме ЦДК (слева) и ЭД (справа).
Отсутствие васкуляризации в раковых узлах встретилось лишь в 2 наблюдениях (3,6%) при узлах менее 10 мм в диаметре. Невозможность визуализации их ангиоархитектоники объяснялась наличием кальцинатов, которые частично (рис. 9) или практически полностью выполняли очаги.
Рисунок 9. Аваскулярный узел папиллярного рака (стрелка)
с кальцинатами в структуре. Сканирование в режиме ЭД.
Аваскулярные узловые образования нередко встречались среди коллоидных пролиферирующих узлов (в 7,5% случаев), но это, как правило, были мелкие узелки диаметром не более 6-7 мм. Несмотря на отсутствие значимых различий, среди злокачественных новообразований чаще, чем среди коллоидных узлов и аденом, выявлялись очаги с отсутствием перинодулярной васкуляризации (IV тип сосудистого рисунка). В таких узлах в режимах ЦДК (ЭД) регистрировался внутриузловой, как правило, малоинтенсивный кровоток с отдельными внутриузловыми «обрубленными» и хаотично расположенными сосудами (рис. 10). В этих случаях применение 3-мерной реконструкции сосудистого рисунка (режим 3D-ангио) способствовало уточнению ангиоархитектоники узла, наличия, хода, выраженности и взаиморасположения узловых сосудов (рис. 11).
Рисунок 10. Скудная внутриузловая васкуляризация узла папиллярного рака
(двусторонняя стрелка) (IV тип сосудистого рисунка). Сканирование в режиме ЭД.
Рисунок 11. Сосудистый рисунок узла папиллярного рака (двусторонние стрелки)
в режиме ЭД (слева) и в режиме 3D-ангио.
Несмотря на отсутствие значимого повышения информативности УЗИ с использованием доплеровских методик в дифференциальной диагностике узловых образований различного морфологического строения, результаты ЦДК, ЭД, 3-мерной реконструкции сосудистого рисунка (режим 3D-ангио) следует учитывать при интерпретации ультразвукового изображения любого внутрипаренхиматозного очага. В случае выявления узлового образования только с внутриузловой васкуляризацией (IV тип сосудистого рисунка) и хаотичным дезорганизованным ходом сосудов с большой долей вероятности можно предполагать злокачественную природу узла, особенно при наличии «серошкальных ультразвуковых признаков злокачественности». При получении сосудистого рисунка с перинодулярной и внутриузловой васкуляризацией (III тип) дифференцировать рак, аденому и коллоидный узел при сходной серошкальной картине сложно. Вместе с тем, перинодулярная и внутриузловая гиперваскуляризация с правильным равномерным «спицеобразным» ходом сосудов чаще (в наших наблюдениях в половине случаев) соответствует аденоме (рис. 12). Таким образом, несмотря на то, что цветовое картирование существенно не повышает информативности ультразвуковой диагностики узловых образований щитовидной железы, это исследование является, на наш взгляд, необходимым не только для полноты характеристики обнаруженных образований, но и для корректного проведения обязательной пункционной биопсии.
Рисунок 12. Сосудистый рисунок аденомы ЩЖ в режиме 3D-ангио.
Анализируя сосудистый рисунок выявленных узловых образований, мы обратили внимание, что степень васкуляризации узлов в большей степени определялась размером узла, а не его морфологической структурой (табл. 5).
Таблица 5. Зависимость васкуляризации узловых образований от размеров узлов
| Тип сосудистого рисунка | Размеры узловых образований в мм | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ≤ 10 | от 11 до 20 | от 21 до 30 | от 31 до 40 | > 40 | Всего | |||||||
| Кол-во | % | Кол-во | % | Кол-во | % | Кол-во | % | Кол-во | % | Кол-во | % | |
| I | 23 | 18,1 | 1 | 0,9 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | 24 | 6,1 |
| II | 48 | 37,8 | 22 | 20,6 | 7 | 8,4 | 2 | 4,9 | 2 | 5,3 | 81 | 20,5 |
| III с внутриузловой гиперваскуляризацией | 15 | 11,8 | 42 | 39,3 | 30 | 36,1 | 12 | 29,3 | 11 | 28,9 | 110 | 27,8 |
| III с внутриузловой гиповаскуляризацией | 31 | 24,4 | 35 | 32,7 | 45 | 54,2 | 25 | 61,0 | 23 | 60,5 | 159 | 40,2 |
| IV | 10 | 7,9 | 7 | 6,5 | 1 | 1,2 | 2 | 4,9 | 2 | 5,3 | 22 | 5,6 |
| Итого | 127 | 100 | 107 | 100 | 83 | 100 | 41 | 100 | 38 | 100 | 396 | 100 |
| значения χ 2 значения р | 28,241 0,0001 | 49,128 0,0001 | 75,567 0,0001 | 39,884 0,0001 | 36,059 0,0001 | |||||||
Так, среди мелких узлов (менее 10 мм в диаметре) преобладали (63,8%) узлы со скудной васкуляризацией (II или IV типа) или аваскулярные очаги. С увеличением размеров узлов уменьшалась частота встречаемости скудно васкуляризированных образований (с 36,2% при размерах менее 10 мм до 9,8% и 10,6% при размерах очагов свыше 30 и 40 мм). Кроме того, среди образований мелкого и среднего калибра (до 20 мм) с III типом сосудистого рисунка в наших наблюдениях встречались преимущественно узлы с внутриузловой гиперваскуляризацией, а среди более крупных (свыше 20 см и особенно свыше 40 мм в диаметре) – с интранодулярной гиповаскуляризацией.
В общей сложности на дооперационном этапе обследования информативность УЗИ в диагностике злокачественных опухолей ЩЖ составила: чувствительность – 63,4%, специфичность – 87,7%, точность – 85,2%, прогностическая ценность положительного результата – 38,3%, прогностическая ценность отрицательного результата – 95,4%. Информативность УЗИ во многом зависела от размеров опухоли, акустической структуры опухолевого узла, распространенности процесса, количества узлов, наличия синхронных поражений ЩЖ. Так, чувствительность УЗИ при выявлении рака при одиночном и многоузловом поражении составляла соответственно 85,7% против 51,4% (различия статистически значимы, z=2,305, р=0,021). Преобладание в наших наблюдениях пациентов с множественными узловыми образованиями ЩЖ (62,5% против 37,5%), высокая встречаемость «нетипичного» ультразвукового изображения ракового узла (32,1%), большое количество (41,0%) крупных узлов диаметром свыше 2 см объясняли недостаточно высокую чувствительность УЗИ в дифференциации злокачественной патологии ЩЖ. Существенному повышению результативности диагностики рака ЩЖ способствовали тонкоигольные аспирационные биопсии (ТАБ) подозрительных узлов с цитологическим исследованием пунктата. При сочетании УЗИ и ТАБ чувствительность метода возросла до 83,9%, специфичность – до 90,9%, точность – до 89,8%, прогностическая ценность положительного результата – до 62,7%, прогностическая ценность отрицательного результата – до 96,9%.
В случае обнаружения подозрительного в плане злокачественности очага в паренхиме ЩЖ возможностями УЗИ определяли распространенность опухолевого процесса, обращая внимание на нарушение целостности капсулы ЩЖ, наличие измененных лимфоузлов. Дополнительно проводили ультразвуковое обследование других органов и систем (печень, почки), учитывая возможность отдаленного метастазирования.
При исследовании всех образований, а особенно с прикапсульной локализацией и подозрительных на малигнизацию, в обязательном порядке изучали целостность капсулы ЩЖ. Среди заподозренных при УЗИ раках ЩЖ нарушения целостности капсулы в виде неровности, «смазанности» и прерывистости ее контура выявлено у 7 больных с раком ЩЖ (рис. 13).
Рисунок 13. Нарушение целостности капсулы ЩЖ (стрелки)
с инвазией опухоли (двусторонняя стрелка) в прилежащие мышцы.
Измененные лимфоузлы в зонах регионарного лимфооттока найдены при УЗИ у 19 пациентов с раковыми узлами в тиреоидной паренхиме. В 3 наблюдениях ультразвуковое изображение пораженных лимфоузлов очень походило на эхографическую картину ракового узла в ЩЖ. Лимфоузлы были гипоэхогенные, с ровным или неровным четким контуром, ближе к округлой форме, с соотношением длины к ширине Вверх