зачем нужна таблица растворимости
Как пользоваться таблицей растворимости в химии
Функции таблицы растворимости
Таблица Менделеева — не единственный помощник в работе химика. Не менее важным инструментом для решения химических уравнений является таблица растворимости веществ. Прежде всего она помогает определить, растворяется ли вещество в воде. Если оно не растворяется, можно узнать каким будет осадок и решить ионное уравнение.
Растворимость веществ
Если вещество может образовать с другим однородное соединение, значит оно растворимо. Степень растворимости у всех веществ разная. В зависимости от этого все вещества делят на группы:
Каждое вещество имеет коэффициент растворимости, показывающий величину массы, которую оно может растворить. На растворение зачастую влияет температура и давление, при которых происходит реакция.
Осторожно! Если преподаватель обнаружит плагиат в работе, не избежать крупных проблем (вплоть до отчисления). Если нет возможности написать самому, закажите тут.
Полная таблица растворимости
В школьном курсе химии используется упрощенная таблица растворимости. Для более высокого уровня изучения или работы необходима полная, где приводятся данные о большем количестве реакций и включено больше химических элементов и соединений.
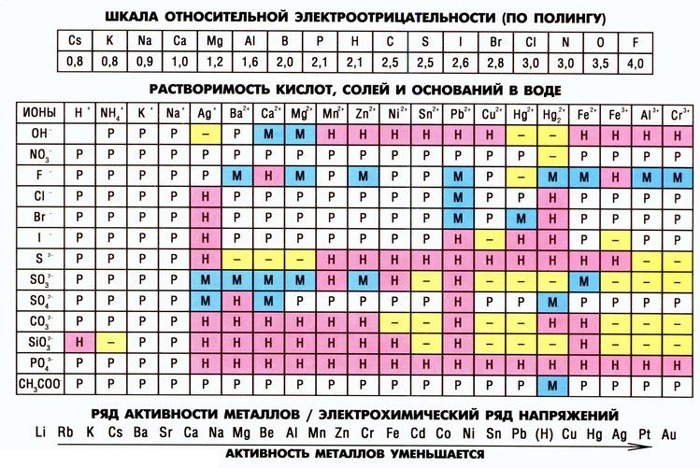
Школьная таблица растворимости
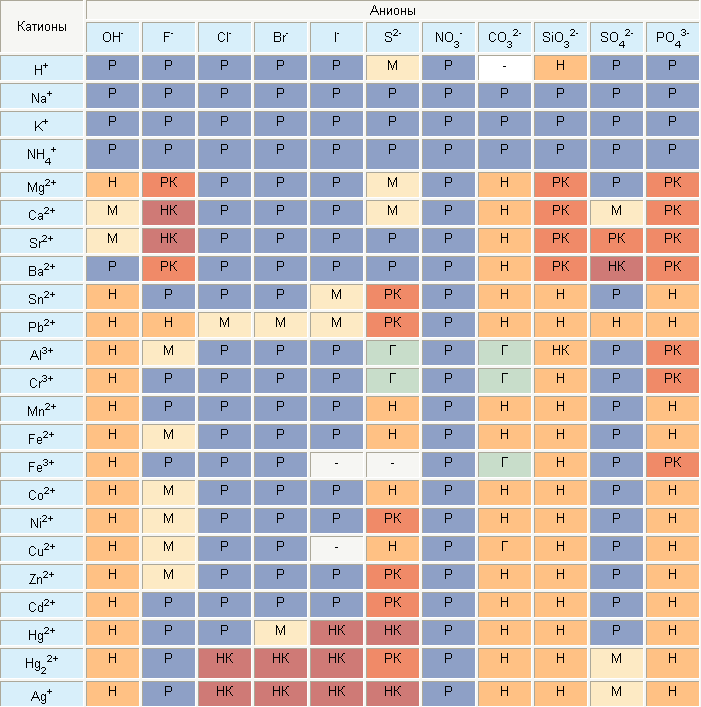
Полная таблица растворимости
Условные обозначения
В таблице указаны названия химических элементов и соединений, а также условные обозначения, говорящие о степени растворимости. Часть обозначений действительна и для школьной. В полной таблице учтена способность веществ растворяться в кислотах.
Как применять таблицу
Растворимость
Растворимость (Р, χ или ks) – это характеристика насыщенного раствора, которая показывает, какая масса растворенного вещества может максимально раствориться в 100 г растворителя. Размерность растворимости — г/ 100 г воды. Поскольку мы определяем массу соли, которая приходится на 100 г воды, в формулу растворимости добавляем множитель 100:
здесь mр.в. – масса растворенного вещества, г
mр-ля – масса растворителя, г
Иногда используют обозначение коэффициент растворимости kS.
Задачи на растворимость, как правило, вызывают сложности, так как эта физическая величина для школьников не очень привычна.
Растворимость веществ в различных растворителях меняется в широких пределах.
В таблице приведена растворимость некоторых веществ в воде при 20 o С:
Растворимость, г на 100 г H2O
Растворимость, г на 100 г H2O
От чего же зависит растворимость веществ? От ряда факторов: от природы растворенного вещества и растворителя, от температуры и давления. В справочных таблицах предлагается вещества делят на хорошо растворимые, малорастворимые и нерастворимые. Такое деление очень условное, поскольку абсолютно нерастворимых веществ нет. Даже серебро и золото растворимы в воде, однако их растворимость настолько мала, что можно пренебречь ей.
Зависимость растворимости от природы растворенного вещества и растворителя*
Большинство солей щелочных металлов и аммония хорошо растворимы в воде. Хорошо растворимы почти все нитраты, нитриты и многие галогениды (кроме галогенидов серебра, ртути, свинца и таллия) и сульфаты (кроме сульфатов щелочноземельных металлов, серебра и свинца). Для переходных металлов характерна небольшая растворимость их сульфидов, фосфатов, карбонатов и некоторых других солей.
Растворимость газов в жидкостях также зависит от их природы. Например, в 100 объемах воды при 20 o С растворяется 2 объема водорода, 3 объема кислорода. В тех же условиях в 1 объеме Н2О растворяется 700 объемов аммиака.
Влияние температуры на растворимость газов, твердых веществ и жидкостей*
Растворение газов в воде вследствие гидратации молекул растворяемого газа сопровождается выделением теплоты. Поэтому при повышении температуры растворимость газов понижается.
Влияние давления на растворимость газов, твердых веществ и жидкостей*
На растворимость твердых и жидких веществ в жидкостях давление практически не оказывает влияния, так как изменение объема при растворении невелико. При растворении газообразных веществ в жидкости происходит уменьшение объема системы, поэтому повышение давления приводит к увеличению растворимости газов. В общем виде зависимость растворимости газов от давления подчиняется закону У. Генри (Англия, 1803 г.): растворимость газа при постоянной температуре прямо пропорциональна его давлению над жидкостью.
Закон Генри справедлив лишь при небольших давлениях для газов, растворимость которых сравнительно невелика и при условии отсутствия химического взаимодействия между молекулами растворяемого газа и растворителем.
Влияние посторонних веществ на растворимость*
В присутствии в воде других веществ (солей, кислот и щелочей) растворимость газов уменьшается. Растворимость газообразного хлора в насыщенном водном растворе поваренной соли в 10 раз меньше. Чем в чистой воде.
Эффект понижения растворимости в присутствии солей называется высаливанием. Понижение растворимости обусловлено гидратацией солей, что вызывает уменьшение числа свободных молекул воды. Молекулы воды, связанные с ионами электролита, уже не являются растворителем для других веществ.
Примеры задач на растворимость
Задача 1. Массовая доля вещества в насыщенном растворе равна 24% при некоторой температуре. Определите коэффициент растворимости этого вещества при данной температуре.
Решение:
Для определения растворимости вещества примем массу раствора равной 100 г. Тогда масса соли равна:
mводы = mр-ра – mр.в. = 100 — 24 = 76 г
χ = mр.в./mр-ля⋅100 = 24/76⋅100 = 31,6 г вещества на 100 г воды.
Еще несколько аналогичных задач:
2. Массовая доля соли в насыщенном растворе при некоторой температуре равна 28,5%. Определите коэффициент растворимости вещества при этой температуре.
3. Определите коэффициент растворимости нитрата калия при некоторой температуре, если массовая доля соли при этой температуре равна 0,48.
4. Какая масса воды и соли потребуется для приготовления 500г насыщенного при некоторой температуре раствора нитрата калия, если его коэффициент растворимости при этой температуре равен 63,9г соли в 100г воды?
Ответ: 194,95 г
5. Коэффициент растворимости хлорида натрия при некоторой температуре составляет 36г соли в 100г воды. Определите молярную концентрацию насыщенного раствора этой соли, если плотность раствора 1,2 г/мл.
6. Какая масса соли и 5% раствора её потребуется для приготовления 450г насыщенного при некоторой температуре раствора сульфата калия, если его коэффициент растворимости при этой температуре равен 439г/1000г воды?
7. Какая масса нитрата бария выделится из раствора, насыщенного при 100ºС и охлаждённого до 0ºС, если во взятом растворе было 150мл воды? Коэффициент растворимости нитрата бария при температурах 0ºС и 100ºС равен соответственно 50г и 342г в 100г воды.
8. Коэффициент растворимости хлорида калия при 90ºС равен 500г/л воды. Сколько граммов этого вещества можно растворить в 500г воды при 90ºС и какова его массовая доля в насыщенном растворе при этой температуре?
9. В 500г воды растворено при нагревании 300г хлорида аммония. Какая масса хлорида аммония выделится из раствора при его охлаждении до 50ºС, если коэффициент растворимости соли при этой температуре равен 50г/л воды?
Произведение растворимости
Материалы портала onx.distant.ru
Теоретическое введение
Примеры решения задач
Задачи для самостоятельного решения
Теоретическое введение
В насыщенных водных растворах малорастворимых соединений устанавливается равновесие:
PbCl2(кристалл.) ↔Pb 2+ (насыщ.р-р) + 2 Cl – (насыщ.р-р)
ПР = [Pb 2+ ] [Cl – ] 2
Понятие ПР используется только при описании гетерогенных равновесий в насыщенных растворах малорастворимых сильных электролитов и их твердых фаз. Растворимость вещества равна его концентрации в насыщенном растворе. Насыщенный раствор находится в равновесии с кристаллической фазой.
ПР связано с изменением энергии Гиббса процесса уравнением:
ΔG о T = – RT lnПР (1)
которое используется для расчетов ПР по термодинамическим данным.
Из определенной опытным путем растворимости соединения можно рассчитать ПР и, наоборот, зная ПР соединения, можно рассчитать его растворимость в воде.
Рассмотрим растворение малорастворимого электролита КnАm. В насыщенном растворе этого электролита имеет место равновесие:
КnАm (к) + aq ↔ n К m+ (насыщ.р-р) + m A n- (насыщ.р-р)
Произведение растворимости КnАm запишется в виде:
ПР = [К m+ ] n [A n- ] m (2)
Если обозначить растворимость электролита буквой Р, то концентрации катионов и анионов в насыщенном растворе составят:
[К m+ ] = nP; [A n- ] = mP
В результате для величины ПР получаем
ПР = [nP] n [mP] m = n n m m P n+m (3)
Растворимость симметричных электролитов (содержащих равнозарядные ионы, например, AgCl, BaSO4, AlPO4) рассчитывается как корень квадратный из ПР.
Добавление в раствор малорастворимого электролита, например, AgCl, веществ, содержащих одноименные ионы, в частности, BaCl2 или AgNO3, приводит к уменьшению растворимости этого электролита.
Примеры решения задач
Решение. М(BaCO3) = 197 г/моль. Растворимость Р карбоната бария равна:
В насыщенном растворе карбоната бария:
концентрации ионов бария и карбонат-ионов равны. Следовательно,
[Ba 2+ ] = [СO3 2- ] = 7× 10 –5 моль/л
Таким образом, растворимость Р карбоната бария равна 7·10 –5 моль/л. Величина ПР составит:
PbCl2(к) + aq ↔ Pb 2+ (насыщ.р-р) + 2 Cl — (насыщ.р-р)
Пусть Р (моль/л) — растворимость PbCl2. Тогда концентрации ионов соли в растворе составят:
[Pb 2+ ] = Р; [Cl – ] = 2[Pb 2+ ] = 2P.
Р(PbCl2) = 278× 1,6× 10 –5 = 4,4× 10 –3 г/л, где 278 — М(PbCl2) (г/моль)
Задача 3. Вычислите растворимость (моль/л) PbCl2 в 0,1 М растворе KCl, если ПР (PbCl2) = 1,6× 10 –5 при 298 К.
Решение. Суммарная концентрация хлорид-ионов составляет
[Cl – ] = (2Р + 0,1) моль/л
Хлорид-ионы образуются при диссоциации PbCl2. В его насыщенном растворе:
PbCl2(к) + aq ↔ Pb 2+ (насыщ.р-р) + 2 Cl — (насыщ.р-р)
а также за счет диссоциации неассоциированного электролита KCl в его 0,1М растворе:
KCl → K + + Cl —
В воде растворимость PbCl2 равна 1,6× 10 –2 моль/л (см. предыдущую задачу), в растворе KCl растворимость PbCl2 уменьшилась и составила 1,6× 10 –3 моль/л.
Решение. Осадок выпадет, если [Сu 2+ ][S 2– ] > ПР(СuS), т.е. если произведение концентраций ионов Сu 2+ и S 2– в растворе будет больше ПР, то раствор окажется пересыщенным и из него будет выпадать осадок.
Молярные концентрации растворов равны:
См (СuCl2) = 1/2× 0,01 = 0,005M
См (Na2S) = 1/2× 0,1 = 0,05M
До смешения растворов: [Сu 2+ ] = 0,005 M, [S 2– ] = 0,05М.
После смешения растворов концентрации ионов изменятся и станут равными:
[Сu 2+ ] = 0,005× 0,1:0,4 = 0,00125M
[S 2– ] = 0,05× 0,3:0,4 = 0,0375М
Следовательно, произведение концентраций ионов равно:
[Сu 2+ ][S 2– ] = 0,00125× 0,0375 = 4,7× 10 –5 (моль/л) 2
Решение.
Примем растворимость BaSO4 за Р моль/л.
Растворимость BaSO4 равна концентрации ионов Ba 2+ и SO4 2– в растворе: [Ba 2+ ] = [SO4 2– ].
где 233 — М(BaSO4) (г/моль).
Следовательно, 1 г BaSO4 растворяются в 1/2,33× 10 –3 = 429,2 л воды.
Задачи для самостоятельного решения
3. При некоторой температуре в 10 л воды растворяется 1,112 г хлорида свинца. Рассчитайте ПР этой соли.
4. При некоторой температуре рН насыщенного раствора гидроксида кальция составляет 13. Рассчитайте величину ПР этого основания.
1,4× 10 –2 моль/л; 4,4 г/л.
7. Вычислить растворимость (моль/л) Ni(OH)2 в 0,15 М растворе Ni(NO3)2, если ПР(Ni(OH)2) = 1,2× 10 –16 при 298 К.
10. При 298 К растворимость PbS в 0,015 М водном растворе K2S равна 4,1× 10 –26 моль/л. Определить G o 298 процесса растворения PbS.
Зачем нужна таблица растворимости
Когда химические вещества вступают во взаимодействие, химические связи между их атомами разрушаются и образуются новые, уже в других сочетаниях. В результате одни вещества превращаются в другие.
Рассмотрим реакцию горения метана, происходящую в конфорке газовой плиты:
Молекула метана (CH₄) и две молекулы кислорода (2O₂) вступают в реакцию, образуя молекулу углекислого газа (CO₂) и две молекулы воды (2H₂O). Связи между атомами углерода (С) и водорода (H) в метане, а также между атомами кислорода (O) разрываются, и образуются новые связи между атомами углерода и кислорода в молекуле углекислого газа (CO₂) и между атомами водорода и кислорода в молекуле воды (H₂O).
Картинка даёт наглядное представление о том, что произошло в ходе реакции. Но зарисовывать сложные химические процессы такими схемами неудобно. Вместо этого учёные используют уравнения химических реакций.
Химическое уравнение — это условная запись химической реакции с помощью формул и символов.
Их записывают в виде схемы, в которой отражён процесс превращения. В левой части располагаются формулы реагентов — веществ, вступающих в реакцию. Завершается уравнение продуктами реакции — веществом или веществами, которые получились в результате.
Новые вещества образуются потому, что изменяются связи между атомами, но сами атомы не возникают из ниоткуда и не исчезают в никуда. На рисунке видно, что атом углерода из состава метана перешёл в состав углекислого газа, атом водорода — в состав воды, а атомы кислорода распределились между молекулами углекислого газа и воды. Число атомов не изменилось.
Согласно закону сохранения массы, общая масса реагентов всегда равна общей массе продуктов реакции. Именно поэтому запись химической реакции называют уравнением.
Виды химических реакций
Вещества вступают в реакции по-разному, можно выделить четыре наиболее частых варианта:
Сложное вещество негашёная известь соединяется с водой, и образуется новое сложное вещество — гашёная известь:
Стрелка вверх означает, что образовался газ. Он улетучивается и больше не участвует в реакции.
В примере атомы цинка замещают атомы водорода в составе хлороводорода, и образуется хлорид цинка:
Стрелка вниз означает, что вещество выпало в осадок, поскольку оно нерастворимо.
Коэффициенты в уравнениях химических реакций
Чтобы составить уравнение химической реакции, важно правильно подобрать коэффициенты перед формулами веществ.
Коэффициент в химических уравнениях означает число молекул (формульных единиц) вещества, необходимое для реакции. Он обозначается числом перед формулой (например, 2NaCl в последнем примере).
Коэффициент не следует путать с индексом (числом под символом химического элемента, например, О₂). Индекс обозначает количество атомов этого элемента в молекуле (формульной единице).
Чтобы узнать общее число атомов элемента в формуле, нужно умножить его индекс на коэффициент вещества. В примере на картинке (2H₂O) — четыре атома водорода и два кислорода.
Подобрать коэффициент — значит определить, сколько молекул данного вещества должно участвовать в реакции, чтобы она произошла. Далее мы расскажем, как это сделать.
Алгоритм составления уравнений химических реакций
Для начала составим схему химической реакции. Например, образование оксида магния (MgO) в процессе горения магния (Mg) в кислороде (O₂). Обозначим реагенты и продукт реакции:
Чтобы схема стала уравнением, нужно расставить коэффициенты. В левой части схемы два атома кислорода, а в правой — один. Уравняем их, увеличив число молекул продукта:
Теперь число атомов кислорода до и после реакции одинаковое, а число атомов магния — нет. Чтобы уравнять их, добавим ещё одну молекулу магния. Когда количество атомов каждого из химических элементов в составе веществ уравнено, вместо стрелки можно ставить равно:
Уравнение химической реакции составлено.
Рассмотрим реакцию разложения. Нитрат калия (KNO₃) разлагается на нитрит калия (KNO₂) и кислород (О₂):
В обеих частях схемы по одному атому калия и азота, а атомов кислорода до реакции 3, а после — 4. Необходимо их уравнять.
Для начала удвоим коэффициент перед реагентом:
Теперь в левой части схемы шесть атомов кислорода, два атома калия и два атома азота. В левой по-прежнему по одному атому калия и азота и четыре атома кислорода. Чтобы уравнять их, в правой части схемы нужно удвоить коэффициент перед нитритом калия.
Снова посчитаем число атомов каждого химического элемента в составе веществ до и после реакции: два атома калия, два атома азота и шесть атомов кислорода. Равенство достигнуто.
Химические уравнения не только позволяют предсказать, что произойдёт при взаимодействии тех или иных веществ, но и помогают рассчитать их количественное соотношение, необходимое для реакции.
Учите химию вместе с домашней онлайн-школой «Фоксфорда»! По промокоду CHEMISTRY892021 вы получите бесплатный недельный доступ к курсам химии за 8 класс и 9 класс.
У нас вы сможете учиться в удобном темпе, делать упор на любимые предметы и общаться со сверстниками по всему миру.

Интересное по рубрике
Найдите необходимую статью по тегам
Подпишитесь на нашу рассылку
Мы в инстаграм
Домашняя онлайн-школа
Помогаем ученикам 5–11 классов получать качественные знания в любой точке мира, совмещать учёбу со спортом и творчеством

Рекомендуем прочитать
Реальный опыт семейного обучения
Звонок по России бесплатный
Посмотреть на карте
Если вы не нашли ответ на свой вопрос на нашем сайте, включая раздел «Вопросы и ответы», закажите обратный звонок. Мы скоро свяжемся с вами.
Растворимость веществ: таблица. Растворимость веществ в воде
В повседневной жизни люди редко сталкиваются с чистыми веществами. Большинство предметов представляют собой смеси веществ.
Растворимость веществ: что это и зачем нужно
О чем говорит мера растворимости вещества
Что такое коэффициент растворимости
Растворители
В данном процессе участвуют растворитель и растворенное вещество. Первый отличается тем, что изначально он пребывает в таком же агрегатном состоянии, что и конечная смесь. Как правило, он взят в большем количестве.
Однако многие знают, что в химии вода занимает особое место. Для нее существуют отдельные правила. Раствор, в котором присутствует H2O называется водным. Когда говорится о них, жидкость является экстрагентом и тогда, когда она в меньшем количестве. В пример можно привести 80%-ный раствор азотной кислоты в воде. Пропорции здесь не равны Хоть доля воды меньше, чем кислоты, вещество называть 20%-ным раствором воды в азотной кислоте некорректно.
Виды растворов по степени насыщенности
Как отличить насыщенный раствор от ненасыщенного?
Теории взаимодействия компонентов растворов
Факторы, влияющие на растворимость веществ
Температура. Чтобы увеличить растворимость твердых веществ в жидкостях, нужно увеличить температуру экстрагента (работает в большинстве случаев). Можно продемонстрировать такой пример. Если положить щепотку хлорида натрия (соль) в холодную воду, то данный процесс займет много времени. Если проделать то же самое с горячей средой, то растворение будет проходить гораздо быстрее. Это объясняется тем, что вследствие повышения температуры возрастает кинетическая энергия, значительное количество которой часто тратится на разрушение связей между молекулами и ионами твёрдого вещества. Однако, когда повышается температура в случае с солями лития, магния, алюминия и щелочами, их растворимость понижается.
Давление. Этот фактор влияет только на газы. Их растворимость увеличивается при повышении давления. Ведь объём газов сокращается.
Изменение скорости растворения
Не стоит путать этот показатель с растворимостью. Ведь на изменение этих двух показателей влияют разные факторы.
Степень раздробленности растворяемого вещества. Этот фактор влияет на растворимость твердых веществ в жидкостях. В цельном (кусковом) состоянии состав разводится дольше, чем тот, который разбит на мелкие куски. Приведем пример. Цельный кусок соли будет растворяться в воде намного дольше, чем соль в виде песка.
Скорость помешивания. Как известно, этот процесс можно катализировать с помощью помешивания. Его скорость также важна, потому что чем она больше, тем быстрее растворится вещество в жидкости.
Для чего нужно знать растворимость твердых веществ в воде
Прежде всего, подобные схемы нужны, чтобы правильно решать химические уравнения. В таблице растворимости есть заряды всех веществ. Их необходимо знать для правильной записи реагентов и составления уравнения химической реакции. Растворимость в воде показывает, может ли соль или основание диссоциировать. Водные соединения, которые проводят ток, имеют в своем составе сильные электролиты. Есть и другой тип. Те, которые плохо проводят ток, считаются слабыми электролитами. В первом случае компоненты представляют собой вещества, полностью ионизованные в воде. Тогда как слабые электролиты проявляют этот показатель лишь в небольшой степени.
Уравнения химической реакции
Подробная таблица помогает узнать, сколько компонента нужно взять для приготовления насыщенной смеси.
Таблица растворимости
Так выглядит привычная неполная таблица. Важно, что здесь указывается температура воды, так как она является одним из факторов, о которых мы уже говорили выше.
Как пользоваться таблицей растворимости веществ
Простой пример
Заключение
Итак, мы изучили вопрос растворимости веществ в воде и не только. Без сомнений, эти знания пригодятся при дальнейшем изучении химии. Ведь растворимость веществ играет там важную роль. Она пригодится при решении и химических уравнений, и разнообразных задач.

.jpg)
.jpg)
.jpg)
.jpg)


.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)

















