Высокопоточный кислородный аппарат что это
Высокопоточный кислородный аппарат что это
Пациент А., 49-ти лет, поступил в ФГБУ «НМИЦ Кардиологии» МЗ РФ Центр COVID-19 с жалобами на кашель с трудноотделяемой мокротой, одышку, нехватку воздуха, боль в груди, головную боль и повышение температуры до 39,4 о С, SpO2 93-94% на атмосферном воздухе. У пациента был положительный назофаренгеальный мазок на SARS-CoV-2.
В течение нескольких дней у пациента нарастала симптоматика дыхательной недостаточности, по данным компьютерной томографии увеличился процент поражения легких до 90% (КТ-4).
Пациент находился на антибактериальной терапии, антикоагулянтной терапии, специфической терапии: гидроксихлорохином, азитромицином, лопинавир-ритонавиром. В последующем, в связи с развитием цитокинового «шторма» больному вводился тоцилизумаб.
Пациент пробыл в блоке интенсивной терапии 6 дней и в дальнейшем учитывая стабилизацию клинического состояния – отсутствие необходимости в проведении респираторной поддержки с применением СРАР – терапии, пациент был переведен в отделение.
При контрольном КТ исследовании: выраженная положительная динамика в виде частичного разрешения вирусной пневмонии, новых участков инфильтрации в паренхиме легких не определяется. Средне-тяжелая степень, процент поражения легочной ткани – 50-60% (КТ2).
Учитывая стабилизацию состояния, отсутствие признаков дыхательной недостаточности и хорошее самочувствие, пациент был выписан из стационара.
Во время проведения СРАР – терапии врачами и медицинским персоналом применялись следующие защитные средства: респиратор FFP3, очки, щиток, костюм индивидуальной защиты влагонепроницаемый, перчатки (2-3 пары). За время использования пациентом СРАР – терапии и в течение 14 дней после ни один сотрудник не заболел, положительных назофаренгиальных мазков на SARS-CoV-2 так же зафиксировано не было.
После выписки пациент выразил благородность всему коллективу ФГБУ «НМИЦ кардиологии».
Полностью клинический пример планируется к публикации в журнале «Анестезиология и реаниматология», ссылка на номер будет размещена на сайте.
Случай предоставлен Литвиным Александром Юрьевичем и Елфимовой Евгенией Михайловной.
Высокопоточная оксигенотерапия при лечении острой дыхательной недостаточности различного генеза

По разным оценкам, в США регистрируется до 137 случаев тяжелой ОДН на 100 тысяч человек, из которых 31-дневная летальность составляет 31,4 %. В странах Европы распространенность тяжелой ОДН составляет от 77,6 до 88,6 случая на 100 тысяч человек в год, для острого респираторного дистресс-синдрома (ОРДС) эти цифры колеблются в пределах 12-28 случаев на 100 тысяч человек в год.
В России, по разным данным, в год в среднем регистрируются 15 тысяч случаев ОРДС, с более частым развитием тяжелой ОДН в отделениях реанимации (ОР), в зависимости от характера заболеваний, повреждений и травм, в среднем от 18 до 56% от всех больных в ОР.
У подавляющего числа живых организмов все процессы метаболизма протекают с участием кислорода. Как отмечал великий химик Я. Берцелиус, «Кислород — это вещество, вокруг которого вращается вся земная химия». Гипоксемия и гипоксия, развивающиеся при дыхательной недостаточности (ДН), вне зависимости от их этиологии, ведут к развитию каскада тяжелых субклеточных, клеточных, органных и системных, часто необратимых, функциональных нарушений.
Поэтому принципиальным является профилактика развития, своевременная диагностика и адекватное лечение ДН у самого разного контингента больных, пострадавших и раненых.
Основным методом лечения ОДН и временного протезирования функции внешнего дыхания является респираторная терапия (РТ), начиная от оксигенотерапии и неинвазивных методов искусственной вентиляции легких (НИВЛ) и заканчивая инвазивными и агрессивными методами полностью управляемой искусственной вентиляции легких (ИВЛ).
Оксигенотерапия — это метод лечения с применением кислорода. Оксигенотерапия является компонентом респираторной терапии (РТ), которая включает в себя комплекс мероприятий, направленных на восстановление вентиляционной и газообменной функций легких. Основными показаниями для ингаляционной оксигенотерапии являются легкие формы паренхиматозной, циркуляторной, гемической и цитотоксической гипоксии.
Среди большого разнообразия способов реализации оксигенотерапии в повседневной клинической практике наиболее часто используется инсуфляция увлажненного кислорода через носовые канюли, назальные или лицевые маски (с клапаном Вентури или без него).
Однако оксигенотерапия, проводимая традиционными методами, не всегда может быть достаточной для больного с ОДН, когда вследствие нарушения вентиляционно-перфузионных отношений в легких простое увеличение фракции кислорода во вдыхаемом газе не приводит к улучшению артериальной оксигенации. Кроме того, эта методика имеет ряд ограничений:
Согласно современным представлениям, при лечении тяжелой ОДН целесообразно использовать не только РТ, но и комплекс нереспираторных и фармакологических методов как с целью воздействия на разные механизмы патогенеза ОДН, так и для снижения агрессивности ИВЛ и профилактики развития вентилятор-ассоциированного повреждения легких (VALI).
Действительно, используемая при тяжелой ОДН инвазивная ИВЛ с агрессивными параметрами, с одной стороны, позволяет корректировать тяжелые нарушения газообмена, с другой, имеет ряд немедленных и отстроченных отрицательных эффектов на органы и системы: гиперинфляция, баротравма, волюмотравма, ателектотравма, биотравма, региональные нарушения вентиляции / перфузии, респиратор-ассоциированные трахеобронхит и пневомния, внелегочные гнойно-септические осложнения, нарушения кардиогемодинамики и т. д.
Поэтому в последние годы получила развитие концепция безопасной или щадящей ИВЛ. Одним из принципов этой концепции является сохранение и поддержание спонтанного дыхания больного даже в условиях инвазивной ИВЛ, что обеспечивает:
Наиболее полно эти эффекты могут быть реализованы при использовании НИВЛ, которая имеет ряд преимуществ:
НИВЛ позволяет эффективно корректировать различные нарушения газообмена в легких, снижает потребность в интубации, дает возможность более ранней экстубации. Существуют много методов НИВЛ и способов соединения респиратора с ДП больного.
Однако при больших безопасности и комфорте для больного НИВЛ более сложна и трудоемка для врача, так как необходимо непрерывно «адаптировать» различные параметры НИВЛ под постоянные изменения респираторного паттерна больного. Кроме неоспоримых преимуществ, НИВЛ имеет и ряд недостатков:
Высокопоточная оксигенотерапия (ВПО) является разновидностью НИВЛ, имеет несомненные преимущества перед традиционной оксигенотерапией, более комфортна, лишена многих недостатков НИВЛ и, как показывают результаты исследований, может быть эффективной альтернативой НИВЛ при ОДН различного генеза.
Оборудование
Высокопоточная оксигенотерапия реализуется посредством генератора высокоскоростного потока газа (до 60 л в минуту и более), системы для эффективного увлажнения и согревания газовой смеси с возможностью пошаговой регуляции скорости потока и температуры, точной установки фракции кислорода, а также специального контура из полупроницаемого материала, не допускающего образования конденсата, и оригинальной носовой или трахеостомической канюли.
На сегодняшний день оборудование для высокопоточной оксигенотерапии представлено двумя компаниями: Fisher and Paykel (Airvo-2, Optiflow, Новая Зеландия) и Vapotherm (High Velocity Nasal Insufflation, США).
Механизмы клинической эффективности высокопоточной оксигенотерапии
В основе клинической эффективности ВПО лежит возможность создания высокой скорости потока газа (до 60 л/мин.), что обеспечивает:
Действительно, было показано, что высокая скорость потока газа при ВПО снижает сопротивление в носоглотке, ВДП и, таким образом, уменьшает работу дыхания больного. Положительное давление в ВДП (2-5-7 см вод. ст.), создаваемое высокоскоростным потоком газа (CPAP- like effect), было измерено R. Parke и соавт. Эти авторы доказали зависимость величины генерируемого положительного давления от скорости потока — его существенный рост в среднем с 35 л/мин.
В исследованиях на здоровых добровольцах N. Groves и соавт. выявили зависимость величины положительного давления, генерируемого в ВДП при ВПО, от дыхания больного с закрытым или открытым ртом и значимую роль утечки газа вследствие несоответствия размера носовых канюль и носовой полости больных, а также ввиду индивидуальных особенностей анатомии верхних дыхательных путей.
Адекватное увлажнение и согревание газа при любом способе РТ является принципиальным вопросом защиты легких и безопасности ИВЛ. Стандартные тепловлагообменные одноразовые фильтры не в состоянии выполнить эти задачи как при инвазивной ИВЛ, так и при НИВЛ. Следует помнить, что при дыхании согревание и увлажнение воздуха в ВДП являются энергозависимым процессом (до 156 кал/мин), и расход энергии прогрессивно возрастает при ОДН.
Поэтому эффективное увлажнение и согревание газовой смеси в условиях РТ обеспечивает:
Важным условием функционирования ВПО является использование оригинального полупроницаемого материала дыхательного контура, что предотвращает образование в нем конденсата и снижает риск развития нозокомиальной инфекции.
Вышеперечисленные особенности ВПО позволяют предположить возможность более физиологического протезирования функции внешнего дыхания посредством этого метода.
Таким образом, принципиальным механизмом, определяющим клиническую эффективность ВПО, является создание потока газа, существенно превышающего инспираторный поток больного и генерирование положительного давления в ВДП. При этом следует отметить, что эффективность ВПО обусловлена совокупностью всех перечисленных факторов.
С другой стороны, в разных клинических ситуациях, в зависимости от доминирования того или иного механизма патогенеза ОДН, сложно определить, что в большей степени определяет эффективность этого метода. Поэтому необходимы дальнейшие исследования для определения оптимального алгоритма применения ВПО при ОДН различного генеза.
Клиническая эффективность высокопоточной оксигенотерапии при развитии ДН различного генеза
Традиционно до широкого внедрения в клиническую практику неинвазивной масочной вентиляции при развитии ОДН основным вопросом были своевременная интубация трахеи и начало ИВЛ. При паренхиматозной ОДН в основе нарушения оксигенирующей функции легких лежат регионарные нарушения вентиляции / перфузии в легких, поэтому в данной ситуации увеличение фракции кислорода во вдыхаемом газе при традиционной низкопоточной оксигенотерапии неэффективно.
Кроме того, при традиционной низкопоточной оксигенотерапии скорость потока кислорода составляет 10-15 л/мин. (с невысоким объемом потока газа). Тогда как скорость пикового потока газа во время обычного вдоха взрослого человека в среднем составляет 20-40 л/мин. и значимо возрастает при развитии ОДН. В результате этой разницы во время дыхания больного к подаваемому таким образом потоку кислорода примешивается комнатный воздух и реальная фракция кислорода в потоке газа снижается.
Кроме того, при оксигенотерапии невозможно адекватное увлажнение и согревание кислородно-воздушной смеси. Все это обусловливает низкую эффективность традиционной низкопоточной оксигенотерапии и ставит вопрос о целесообразности ее применения при манифестации ОДН. Широкое внедрение в клиническую практику неинвазивных методов респираторной поддержки позволяет эффективно протезировать функцию внешнего дыхания при ДН различного генеза и во многих ситуациях избежать интубацию трахеи.
Несмотря на относительную новизну метода, ВПО показала свою эффективность при использовании у разного контингента больных при манифестации ДН различного генеза. Ряд исследований показали высокую клиническую эффективность ВПО при манифестации ОДН и возможность использования этого метода как альтернативы не только традиционной оксигенотерапии, но и неинвазивной масочной ИВЛ.
Roca с соавт. одними из первых показали клиническую эффективность ВПО при лечении больных с ОДН. При сравнении клинической эффективности этого метода с традиционной оксигенотерапией у больных с ОДН (SatО2
Оксигенотерапия повреждает микробиом легких: новое звено патогенеза Covid-19
Несмотря на то, что легкие считаются относительно «чистыми и свободными» от бактерий, в них существует определенный баланс микробиоты, который может нарушаться при проведении оксигенотерапи
Одним из ключевых признаков Covid-19 является одышка, которая вызывается значительным снижением уровня кислорода в крови. Во время госпитализации такие пациенты получают оксигенотерапию для нормализации уровня кислорода.
Несмотря на то, что легкие считаются достаточно «чистыми и свободными» от бактерий, в них существует определенный баланс микробиоты. Новое исследование указывает на то, что оксигенотерапия может негативным образом воздействовать на этот баланс.
«Кислород в избыточном виде является токсином. Если поместить лабораторное животное в среду с 100% кислородом, то оно погибнет в течение 5 дней, при этом будут развиваться повреждения легких, схожих с таковыми при Covid-19 или легочной недостаточности другой этиологии», – рассуждают авторы исследования.
Пациенты в интенсивной терапии получают высокие дозы кислорода на протяжении длительного времени. Ученые решили исследовать, как при этом меняется состав и жизнедеятельность микроорганизмов легких. Различные бактерии достаточно слабо различаются в том, как они реагируют на высокие дозы кислорода.
Была проведена серия экспериментов на здоровых лабораторных мышах. Изменения оказались ровно такими, как предполагали ученые: кислород-толератные бактерии, такие как стафилококки, распространялись в этой среде куда активнее остальных.
Следующий вопрос заключался в том, какое из изменений происходит первым – повреждение легочной ткани или изменения микробиомных взаимоотношений? Оказалось, что микробиом реагировал на оксигенотерапию уже в течение первого дня, в то время как повреждения легких развивались только после 3 дня.
В последнем эксперименте ученые сравнили 2 группы генетически идентичных мышей, получавших оксигенотерапию: со стерильными легкими и с обычным легочным микробиомом. Первая группа не демонстрировала легочных повреждений, характерных для второй группы с естественной микрофлорой в легких.
Это исследование указывает на то, что в патогенезе легочных повреждений при Covid-19 у пациентов, получающих оксигенотерапию, по-видимому, определенную роль играет легочный микробиом.
Тем не менее, результаты использования антибиотиков оказались неожиданными: применение ванкомицина, обладающего эффективностью против грамположительных стафилококков, не повлияло на возникновение легочных повреждений, в отличие от цефтриаксона, направленного на грамотрицательные бактерии.
Авторы работы настаивают на том, чтобы на основании их данных не проводилось никаких изменений актуальных протоколов лечения, в особенности оксигенотерапии. Необходимо проведение рандомизированных контролируемых исследований для получения уверенных клинических рекомендаций.
Как разобраться в расходных материалах для кислородной терапии
Время чтения: 4 мин.
Распространенная ситуация: пациенту назначена респираторная терапия или терапия по удалению мокроты на дому (ИВЛ, аспиратор). Его должны обеспечить всем необходимым. Больница или поликлиника выдает, что указал врач, а потом оказывается, что расходных материалов нет!
Почему так происходит? Дело в том, что обычно врач не разбирается в специфике комплектации оборудования. Пациент или его родственники — тем более. Больница же выдает только то, что попросили. В итоге получается замкнутый круг: не выдали, потому что не просили. Не просили, потому что не знали, что просить.
Что такое расходные материалы
Чтобы в итоге человек получил назначенную кислородную терапию, в вопросе должны разбираться и врачи и сотрудники, ответственные за закупку оборудования в медицинских учреждениях. Тогда врач даст полную выписку, закупщик составит полное техническое задание, пациент получит всё и оно будет работать.
Какие бывают интерфейсы
В обычном вдыхаемом воздухе содержится примерно 21% кислорода. Медицинский кислородный концентратор вырабатывает 90-96-процентный кислород.
Какое количество этого кислорода «дойдет» до пациента зависит от интерфейса (приспособления между источником кислорода и пациентом), с помощью которого он ему подается.
Кислородная канюля
Это трубка специальной конструкции, имеющая два патрубка (зубца) со стороны пациента, которые вставляются в ноздри. Кислородные носовые канюли чаще всего изготовлены из ПВХ или полипропилена. Они различаются по размерам: неонатальные, детские, взрослые (разный диаметр и расстояние между носовыми зубцами).
Конструкция зубцов у разных производителей может отличаться, как и у различных моделей — с прямыми или изогнутыми зубцами, цилиндрическими или расширяющимися и др.
Как правило длина канюли (трубки) составляет около 2 метров (редко 5 метров). Если вам необходимо использовать кислородный концентратор на большем расстоянии от пациента, придется присоединять дополнительную кислородную линию (трубку).
При использовании кислородной канюли и кислородного концентратора при потоках до 6 л/мин концентрация кислорода во вдыхаемом воздухе обычно около 30% (в некоторых источниках приводят диапазон 24-44 %).
При подаче кислорода от стационарных кислородных концентраторов или портативных в режиме постоянного потока не забывайте контролировать наличие воды в увлажнителе. Поток сухого воздуха очень быстро высушивает слизистую оболочку носа и причиняет дискомфорт пациенту в местах прилегания канюли.
Кислородную канюлю следует менять один раз в месяц при использовании 24/7. При постоянном использовании зубцы канюли становятся жесткими и травмируют места прилегания к ноздрям.
Существует множество производителей кислородных носовых канюль. Некоторые делают мягкие утолщения в местах прилегания к ушам.
Канюля — один из самых дешевых интерфейсов для передачи кислорода от кислородного концентратора к пациенту.
Кислородная маска
Специальная маска, которая покрывает нос и рот пациента. Поток кислорода, который идет от маски значительно меньше раздражает слизистую носа. Использовать маску предпочтительнее, когда пациент дышит ртом. Выдох происходит через специальные отверстия в маске.
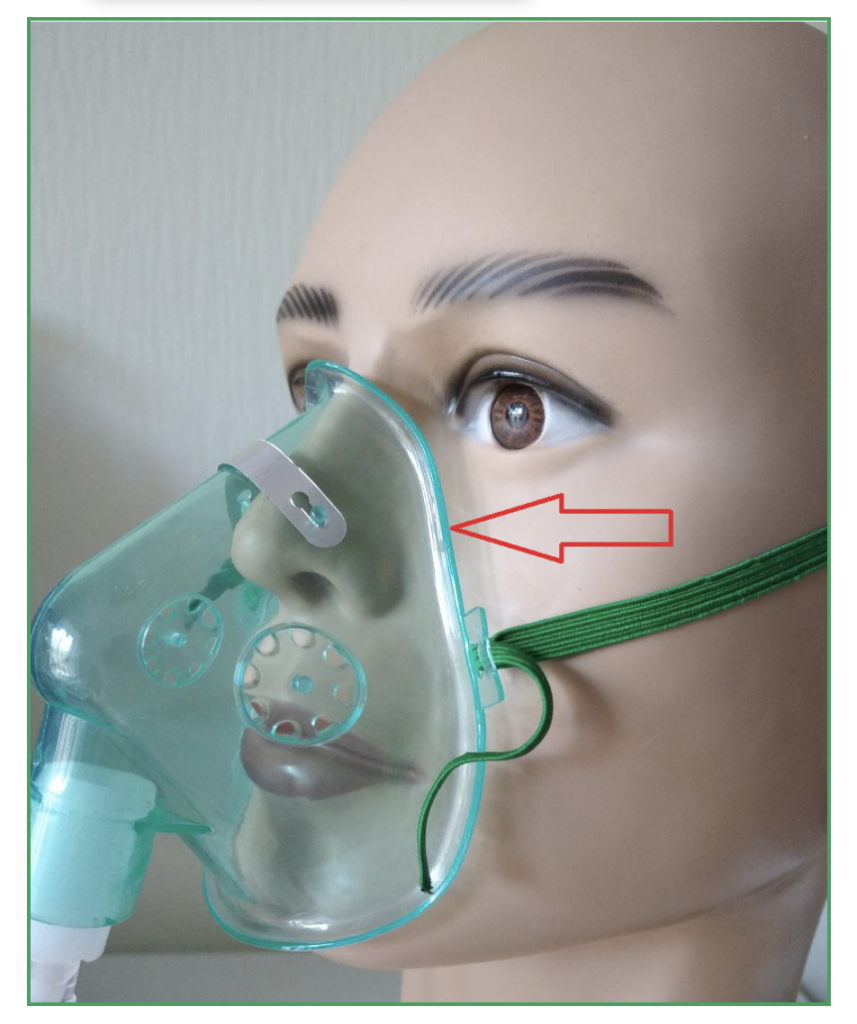
Также маски отличаются друг от друга конструктивно — с металлическим носовым зажимом и без, с мягким уплотнением в месте прилегания к лицу, специальной анатомической формы.
Кислородные маски, как и маски НИВЛ, желательно подбирать по форме лица каждого человека и смотреть удобно ли ему. Обязательно проследите, чтобы не было утечек кислорода, особенно в области глаз и в местах расположения держателя.
Использование кислородной маски позволяет увеличить концентрацию кислорода во вдыхаемой смеси в среднем до 45-55 %.
Маски следует ежедневно обрабатывать мыльным раствором и заменять на новые один раз в 3 месяца при использовании 24/7.
На сайте Паллиатив.рф можно скачать файл с примерными сроками замены расходных материалов для домашнего использования.
У некоторых производителей кислородные маски снабжены вирусобактериальными фильтрами на выдохе. Использование таких кислородных масок убережет работников больниц, ухаживающий персонал от возможного заражения от пациента, находящегося на кислородной поддержке. Это особенно актуально в период пандемии COVID-19.
Кислородная маска высокой концентрации
Если концентрация кислорода во вдыхаемой смеси должна быть выше, чем обеспечивает простая кислородная маска (маска средней концентрации), используют кислородную маску высокой концентрации. Эта маска конструктивно схожа с обычной кислородной маской, но снабжена мешком, в котором накапливается кислород от аппарата во время выдоха пациента.
Такие маски имеют специальное устройство с клапаном, который обеспечивает поступление кислорода к пациенту и в резервный мешок, а также клапанами выдоха и безопасности.
Использование кислородной маски высокой концентрации повышает процент кислорода во вдыхаемой смеси до 80-85%. Наиболее эффективно их использовать при потоке выше 10 л/мин.
Тепловлагообменные фильтры
Если кислородозависимый пациент дышит через трахеостомическую трубку (без ИВЛ), подачу кислорода как правило осуществляют через тепловлагообменный фильтр (официациальное название — термовент дыхательный, неофициальное — искусственный нос). Такие фильтры присоединяются к трахеостомической трубке. Для подачи кислорода они снабжены специальным входом, к которому подключается кислородная линия.
Подача кислорода через такие фильтры наиболее комфортна и безопасна для пациента. Единственный минус: понять конкретную концентрацию кислорода во вдохе невозможно.
Для трахеостомированных пациентов существуют также специальные аэрозольные маски, прилегающие к трахеостомической трубке, через которые можно подавать увлажненный кислород.
Кислородная линия
Для увеличения расстояния между кислородным концентратором и пациентом используют специальную трубку — кислородную линию (кислородные концентраторы могут работать с линией до 15 м). Кислородная линия может быть изготовлена из ПВХ, из материалов не содержащих ПВХ, из силикона и др.
Они могут быть толстостенными, с внутренним армированием (ребрами жесткости), переменного сечения. Трубки переменного сечения наиболее удобны в использовании — они продаются бухтами по 50 и более метров (всегда можно отрезать кусок нужной длины), имеют изменение диаметра от 4 до 8 мм с шагом около 80 см (минимальный диаметр подходит для наконечников ТВО-фильтров).
Примерная комплектация закупки
Чтобы обеспечить кислородной поддержкой на дому 5 пациентов больнице нужно закупить:
Материал подготовлен с использованием гранта Президента Российской Федерации, предоставленного Фондом президентских грантов.
Использовано стоковое изображение от Depositphotos.
Опыт успешного применения новой методики лечения тяжелой формы COVID-19
Полный текст
Аннотация
COVID-19, ранее коронавирусная инфекция 2019-nCoV, — потенциально тяжелая острая респираторная инфекция, вызываемая коронавирусом SARS-CoV-2 (2019-nCoV). Представляет собой опасное заболевание, которое может протекать как в форме острой респираторной вирусной инфекции легкого течения, так и в тяжелой форме с развитием двусторонней полисегментарной пневмонии, специфические осложнения которой могут включать острый респираторный дистресс-синдром, влекущий за собой острую дыхательную недостаточность с высоким риском смерти. В связи с отсутствием этиотропной терапии коронавирусной инфекции на первый план выходит патогенетическое лечение. Нами представлен клинический случай тяжелой формы COVID-19 у 33-летнего мужчины, которому была применена новая, основанная на иммуносупрессивной терапии с последующим терапевтическим плазмообменом и введением неспецифического иммуноглобулина человека методика патогенетического лечения.
Ключевые слова
Полный текст
ОБОСНОВАНИЕ
В большинстве (примерно в 80%) случаев COVID-19 какого-либо специфического лечения не требуется, а выздоровление происходит само по себе [1]. Тяжелые формы болезни с большей вероятностью могут развиться у пожилых людей и у лиц с определенными сопутствующими заболеваниями, включающими астму, диабет и сердечные заболевания [2]. В тяжелых случаях применяются средства для поддержания функций жизненно важных органов [3].
Примерно в 15% случаев заболевание протекает в тяжелой форме с необходимостью применения кислородной терапии, еще в 5% — состояние больных критическое. В целом по миру летальность заболевания оценивается примерно в 6,5% [4].
Вопросы лечения новой коронавирусной инфекции имеют острейшую актуальность. На сегодняшний день не существует доказанной этиотропной терапии, эффективных методов профилактики заболевания, при этом тяжелые формы болезни имеют высочайшие риски неблагоприятного исхода [5].
Теория цитокинового шторма, объясняющая повреждение практически всех систем организма, и в первую очередь тяжелейшее повреждение легочной ткани, позволяет предположить гиперергическую реакцию иммунной системы на провоцирующий агент, при этом нельзя исключить наличие аутоиммунного компонента в патогенезе цитокинового шторма и синдрома гиперактивации макрофагов. Кроме того, развивается связанная с повреждением эндотелия сосудов агрессивная гиперкоагуляция. Все это определило три основных направления — гипоксемию, гиперергическую иммунную реакцию организма, агрессивную гиперкоагуляцию — для патогенетической терапии тяжелых форм болезни [1, 5].
Применение плазмообмена обосновано возможностью удаления цитокинов, связанных с патогенезом цитокинового шторма при COVID-19 [6]. Применение иммуноглобулина повышает неспецифическую резистентность организма после проведения иммуносупрессивной терапии, показано при всех тяжелых вирусных и бактериальных инфекциях. Необходимо также учесть потери иммуноглобулинов при проведении плазмообмена [7].
ОПИСАНИЕ КЛИНИЧЕСКОГО СЛУЧАЯ
О пациенте
Пациент П., возраст 33 года, поступил в Федеральный медицинский биофизический центр имени А.И. Бурназяна (далее ФМБЦ им. А.И. Бурназяна) 21.04.2020 по каналу скорой медицинской помощи с направительным диагнозом «Двусторонняя пневмония» (по данным компьютерной томографии, выполненной на догоспитальном этапе).
Из анамнеза заболевания. Считает себя больным с 14.04.2020, когда появились слабость и головная боль. С 15.04.2020 — повышение температуры тела до 39,5°С. Принимал жаропонижающие препараты (парацетамол, Нурофен) — без эффекта. Бригадой скорой медицинской помощи, вызванной 18 апреля, проведены общие мероприятия по нормализации температуры тела (жаропонижающие препараты); оставлен под наблюдение врача поликлиники. 19.04.2020 осмотрен участковым врачом-терапевтом из поликлиники, по рекомендации которого выполнена компьютерная томография (КТ) органов грудной клетки: выявлена двусторонняя пневмония. Назначено лечение: Сумамед, Тамифлю.
Пациент строго соблюдал режим самоизоляции, выходил только в магазин за продуктами, всегда использовал медицинскую маску. В течение 3 мес, предшествовавших заболеванию, пределы России не пересекал. Операций, гемотрансфузий, внутримышечных или внутривенных инъекций, лечения зубов в последние 6 мес не проводилось.
21.04.2020 в связи с отсутствием эффекта от проводимой терапии бригадой скорой медицинской помощи госпитализирован в ФМБЦ им. А.И. Бурназяна.
Заключение по результатам КТ от 21.04.2020: Двусторонняя полисегментарная пневмония. Оценка тяжести пневмонии — КТ3.
Наследственных и хронических заболеваний не имеет. Вредных привычек нет.
Предъявляет жалобы на общую слабость, повышение температуры тела до 39°С, головокружение, снижение аппетита.
Исследования при поступлении
Физикальное исследование. Общее состояние тяжелое. Телосложение правильное. Конституция нормостеническая. Рост 184 см, масса тела 96 кг, индекс массы тела 28,4. Кожа и слизистые оболочки физиологической окраски и влажности, теплые. Видимые слизистые — влажные, чистые. Подкожная жировая клетчатка развита несколько избыточно.
Область сердца не изменена. Аускультация сердца невыполнима. Артериальное давление 105/70 мм рт.ст. Частота пульса 106/мин.
Аускультация легких невыполнима. Частота дыхательных движений 24/мин. Насыщение (сатурация) крови кислородом (blood oxygen saturation, SpO2) 90% на фоне инсуффляции увлажненного кислорода 4 л/мин.
Язык влажный. Живот симметричный, при пальпации — мягкий, безболезненный, равномерно участвует в акте дыхания. Печень у края реберной дуги. Стул 20.04.2020, оформленной консистенции, без патологических примесей. Дизурических явлений нет. Симптом поколачивания отрицательный с обеих сторон.
Нервная система и органы чувств: сознание ясное, ориентирован во времени, месте, собственной личности. Адекватен. Чувствительность сохранена, симметрична. Мышечная сила конечностей D = S, удовлетворительная. Координаторные пробы выполняет удовлетворительно. В позе Ромберга устойчив. Менингеальной, патологической неврологической симптоматики нет.
Локальный статус: при осмотре гиперемия, отечность слизистой зева, выделения слизистого характера из носовых ходов.
Оценка по шкале органной недостаточности (quick Sequential Organ Failure Assessment, qSOFA) 1 балл. Пациент госпитализирован в инфекционное отделение № 1, где начата терапия по принятым клиническим рекомендациям.
Лабораторное исследование. Выраженная протеинурия (до 1 г/л), небольшая гипергликемия (до 7,8 ммоль/л), уровень С-реактивного белка 44,6 мг/л, ферритин 2540 мг/мл, D-димер 1,41 мг/л, прокальцитонин менее 0,5 нг/мл. Тест на COVID-19 (методом полимеразной цепной реакции) от 22.04.2020 — положительный. Остальные показатели лабораторного спектра в пределах референсных значений.
Инструментальное исследование. Электрокардиография: синусовая тахикардия с частотой сердечных сокращений 100 уд./мин. Умеренные изменения миокарда. Снижен вольтаж зубца R в грудных отведениях. Группа крови АВ (IV) Rh+.
23.04.2020, несмотря на проводимую терапию, состояние продолжало ухудшаться, нарастала одышка до 30/мин, SpO2 на фоне оксигенотерапии 5 л/мин, не более 88% в прон-позиции. Повторно выполнена КТ легких: признаки двусторонней полисегментарной пневмонии, высокая вероятность COVID-19, КТ4.
Учитывая значительную отрицательную динамику состояния, 23.04.2020 пациент переведен в отделение реанимации и интенсивной терапии (ОРИТ).
Несмотря на молодой возраст и отсутствие сопутствующей патологии, у данного пациента отмечалось резкое прогрессирование болезни (индекс PaO/FiO
Рис. 1. Компьютерная томография легких от 24.04.2020: увеличение распространенности и интенсивности патологических изменений с субтотальным поражением легочной паренхимы, КТ4
По данным ультразвукового мониторинга легочной ткани выявлено большое количество В-линий во всех отделах легких, при этом С-линий не обнаружено. Лабораторно отмечено снижение уровня С-реактивного белка до 15 мг/л, ферритина до 1140 мг/мл, а также значительное снижение протеинурии до 0,5 г/л, отсутствие лихорадки. Терапия продолжена. 25.04.2020 отмечалось значительное улучшение легочной биомеханики, при прежних параметрах ИВЛ дыхательный объем достиг 700 мл. Седация прекращена, режим вентиляции изменен на вспомогательный — спонтанный (SPONT) с параметрами постоянного положительного давления (constant positive airway pressure, CPAP) 12 mbar, FiO2 45%, поддержкой давлением (pressure support, Ps) 14 mbar, дыхательным объемом до 650 мл, частотой дыхательных движений 12–14/ мин, минутным объемом дыхания до 9,5 л/мин, etCO2 42–46. Также значительно улучшились показатели оксигенации: SpO2 94%, индекс PaO/FiO 160. С целью облегчения активизации пациента, обеспечения самостоятельного питания и создания комфорта выполнена ранняя пункционно-дилатационная трахеостомия. В течение последующих 2 сут состояние постепенно улучшалось, была значимо снижена респираторная поддержка, но сохранялась необходимость в СРАР не менее 11 mbar, т.к. на более низких значениях отчетливо увеличивалась работа дыхания, снижался дыхательный объем, появлялись тахипноэ и тахикардия. 27.04.2020 появилась гипертермия до 38,6°С, которая не отмечалась с 24.04.2020; уровень прокальцитонина соответствовал > 2 нг/ мл, наблюдался резкий рост лейкоцитоза до 16,9 со сдвигом формулы влево, что соответствовало бактериальной сперинфекции.
По данным КТ легких, на фоне улучшения состояния легочной ткани отмечалось развитие правосторонней нижнедолевой бронхопневмонии (рис. 2).
Рис. 2. Компьютерная томография легких от 29.04.2020: на фоне улучшения состояния легочной ткани отмечается развитие правосторонней нижнедолевой бронхопневмонии
Антибактериальная терапия изменена на меропенем в дозе 2 г по 3 раза/сут. По данным микробиологического исследования выявлен Acinetobacter baumannii. В течение 3 дней лихорадка, лабораторные признаки воспаления и уровень прокальцитонина были нормализованы. Индекс PaO/FiO достиг 300, SpO2 98–99%. Оценка по SOFA 0 баллов. С 30.04.2020 пациент приступил к тренировкам самостоятельного дыхания, а со 02.05.2020 механическая вентиляция легких прекращена полностью, выполнена деканюляция трахеи. Респираторная терапия в объеме оксигенотерапии через назальные канюли 4 л/мин. Тест на COVID-19 (методом полимеразной цепной реакции) от 01.05.2020 положительный. КТ от 02.05.2020 с дальнейшей положительной динамикой (рис. 3).
Рис. 3. Компьютерная томография легких 02.05.2020: положительная динамика на фоне лечения
Исход
К 05.05.2020 терапия деэскалирована практически полностью, продолжается только антикоагулятная профилактика, в оксигенотерапии не нуждается. Лабораторно все показатели в пределах референсных значений. Переведен для дальнейшего лечения и реабилитации в 1-е инфекционное отделение. 12.05.2020 выписан из стационара после получения отрицательного результата от 10.05.2020 теста на COVID-19.
Длительность пребывания в ОРИТ составила 11 дней, общая длительность госпитализации — 21 день.
ОБСУЖДЕНИЕ
Успешный опыт в нашем случае показывает, что стоит попробовать своевременное патогенетическое лечение, особенно у пациентов в критическом состоянии с инфекцией COVID-19, поскольку это может значительно улучшить прогноз. Наш отчет о болезни дает новый взгляд на стратегию лечения этого потенциально смертельного заболевания.