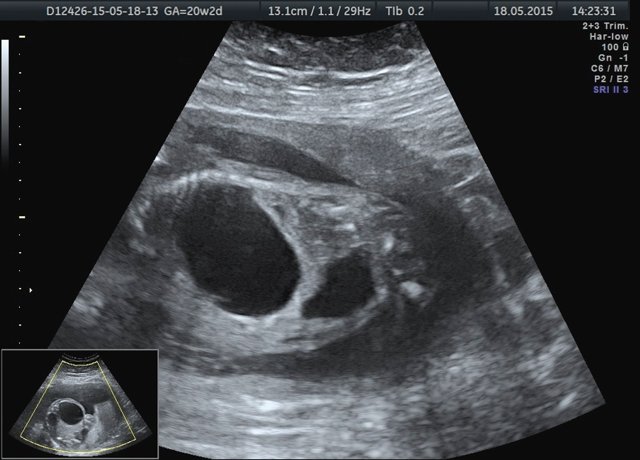
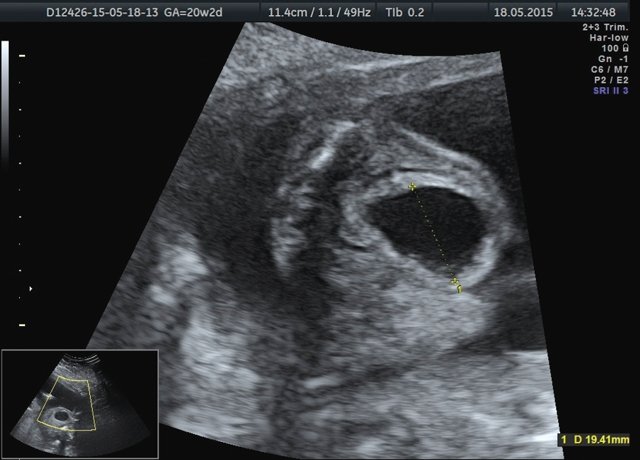
Впр узи плода что это
Исследование плода и плаценты при врожденных пороках развития, несовместимых с жизнью
Целью исследования было выявить структуру врожденных пороков развития плода, несовместимых с жизнью, приведших к индуцированному прерыванию беременности по медицинским показаниям, структурные изменения в последе при наличии пороков развития. Проведено ран
The aim of the study was to reveal the structure of fatal congenital malformations of the fetus, leading to the induced interruption of pregnancy due to medical indications, structural changes in the afterbirth in the presence of malformations. The randomized comparative study was conducted in 2 stages (retrospective and prospective).
Врожденные пороки развития (ВПР) плода считают важнейшей медицинской и социальной проблемой, поскольку они занимают ведущее место в структуре причин перинатальной, неонатальной и младенческой заболеваемости, смертности и инвалидности [1]. Также актуальной является проблема прерывания беременности в поздние сроки по медицинским показаниям со стороны плода, так как на ее долю приходится около 20% от общего числа абортов, а количество осложнений возрастает в 3–4 раза при прерывании беременности во втором триместре по сравнению с первым [2]. Согласно данным ВОЗ, ВПР отмечают у 4–6% детей. В России ежегодно более 50 000 детей рождаются с ВПР, число пациентов с ВПР превышает 1,5 млн человек. При наличии у плода ВПР, несовместимых с жизнью, или сочетанных пороков с неблагоприятным прогнозом для жизни и здоровья, при ВПР, приводящих к стойкой потере функций вследствие тяжести и объема поражения при отсутствии методов эффективного лечения, женщине предоставляется информация о возможности искусственного прерывания беременности по медицинским показаниям [3]. При отказе женщины прервать беременность из-за наличия ВПР, несовместимых с жизнью, или иных сочетанных пороков беременность ведется в соответствии с разделом I настоящего порядка. Высокие затраты на лечение, уход и реабилитацию детей с ВПР обусловливают необходимость разработки и совершенствования не только методов контроля, диагностики и профилактики ВПР у детей, но и изучения патоморфологии плода и последа [4].
В последние десятилетия интенсивно изучаются многочисленные антенатальные факторы, приводящие к повреждению нервной системы плода — внутриутробные инфекции, генетические дефекты, проблемы резус-конфликта, воздействие на плод лекарственных веществ и целый ряд других факторов. Нередко причинами врожденных пороков развития плода и последа являются инфекционные причины: инфекционные фетопатии формируются с 16-й недели, когда происходит генерализация инфекции у плода, вследствие чего могут возникать такие пороки развития, как фиброэластоз эндокарда, поликистоз легких, микро- и гидроцефалия (ранние фетопатии) [5].
Большое количество работ посвящено методам прерывания беременности в позднем сроке по медицинским показаниям со стороны плода — врожденным порокам развития плода, реабилитации женщин после элиминации плода [6–11]. В то же время недостаточно описаны результаты патологоанатомического исследования плода и плаценты при врожденных пороках, несовместимых с жизнью. Наше исследование посвящено прерыванию беременности во втором триместре по медицинским показаниям со стороны плода. Данная публикация посвящена вопросам патологоанатомического исследования плода и последа.
Целью данного исследования было выявить структуру врожденных пороков развития плода, несовместимых с жизнью, приведших к прерыванию беременности по медицинским показаниям, их сочетания со структурными изменениями в последе.
Материалы и методы исследования
Исследование одобрено локальным этическим комитетом ФГБОУ ВО ОмГМУ МЗ РФ, Омск (№ 63 от 09.10.2014 г.) и выполнено на базе БУЗОО ГКПЦ, Омск. Прерывание беременности во II триместре по медицинским показаниям проводилось согласно Распоряжению Министерства здравоохранения Омской области № 308-р от 17.09.2013 г. в указанном учреждении, где был создан центр по прерыванию беременности второго триместра и женщине выдавалось заключение перинатального консилиума специалистами (акушер-гинеколог, перинатолог, неонатолог и др.). Гистологическое исследование элиминированных плодов и плацент проведено согласно рекомендациям А. П. Милованова и осуществлялось в патологоанатомическом отделении БУЗОО ОДКБ, Омск.
Основным показанием к прерыванию беременности на всех этапах являлись ВПР плода, несовместимые с жизнью. При наличии у плода ВПР, несовместимого с жизнью, или наличии сочетанных пороков с неблагоприятным прогнозом для жизни и здоровья, при ВПР, приводящих к стойкой потере функций вследствие тяжести и объема поражения при отсутствии методов эффективного лечения, предоставлялась информация о возможности искусственного прерывания беременности по медицинским показаниям. Искусственное прерывание беременности проводилось при наличии информированного добровольного согласия женщины.
На первом ретроспективном этапе (до внедрения в практику регламентирующих документов [3, 12]) проведен анализ гистологического исследования плацент после прерывания беременности у 150 женщин, которые в зависимости от метода прерывания были разделены на две группы: группу А составили 75 женщин, которым проведено прерывание беременности в поздние сроки методом трансвагинального трансцервикального амниоцентеза: амниоинфузия 10% раствором хлорида натрия. Группу Б составили 75 женщин, которым с целью прерывания беременности в поздние сроки для возбуждения и стимуляции родовой деятельности использовали гель динопростон для эндоцервикального введения. Более подробно методы прерывания беременности, их эффективность и исходы описаны в наших предыдущих публикациях [13–15]. Критериями включения пациенток в группы А и Б были следующие: срок беременности 18–21 неделя 6 дней, возможность родоразрешения через естественные родовые пути и отсутствие противопоказаний к применению гипертонического раствора хлорида натрия (10% NaCl) и простагландинов. Пациентки обеих групп были идентичны по возрасту, особенностям менструальной функции, наличию экстрагенитальных и гинекологических заболеваний, паритету. Все пациентки были консультированы в медико-генетическом отделе.
На втором этапе под проспективным наблюдением было 195 беременных, разделенных на две группы. Основную группу составили 98 женщин, которым проведено прерывание беременности в поздние сроки следующим комбинированным методом: мифепристон перорально и введение ламинарий в цервикальный канал. В группу сравнения были включены 97 женщин, прерывание беременности которым проводилось по схеме ВОЗ. Критерии включения в группы: пациентки, которым дано заключение консилиума врачей для прерывания беременности по медицинским показаниям со стороны плода в сроки гестации 18–21 неделя согласно приказам МЗСР РФ № 736 от 03 декабря 2007 г. [16] и № 572н от 01.11.2012 [3].
На проспективном этапе исследования материалом для изучения послужили результаты патоморфологического исследования плодов (аутопсийного материала) и последов (макроскопическое и микроскопическое). В работе использованы антропометрические, органометрические, гистологические методы. С целью уточнения гестационного возраста плода и дополнительных скрытых аномалий развития в соответствии с имеющимися стандартами использовали антропометрические и органометрические исследования [17–20]. Гистологические исследования органов плода, плодных оболочек, пуповины и плаценты проводили на парафиновых срезах, изготовленных по общепринятой методике и окрашенных гематоксилином и эозином, а также избирательно пикрофуксином по методу Ван Гизона. Для гистологического исследования предварительно материал фиксировали в 10% нейтральном формалине, после промывки и стандартной проводки заливали в парафин. Парафиновые срезы толщиной 3–5 мкм окрашивали гематоксилином и эозином. Элементы соединительной ткани определяли пикрофуксином по методу Ван-Гизона. Методы гистологического исследования выполнялись по прописям, изложенным в классических руководствах по гистологической технике и гистохимии. Обследование элиминированных плодов включало тщательную визуальную оценку имеющихся стигм эмбриогенеза, врожденных пороков. Для гистологического исследования отбирали фрагменты органов с целью изучения их гистоархитектоники [17].
Использовался способ статистической обработки результатов по критерию t таблиц Стьюдента, позволяющий вычислить степень достоверности различий при небольшом числе наблюдений. Перед каждым вычислением достоверности различий между количественными признаками, а также для выбора критерия корреляции оценивали нормальность их распределения по критерию Колмогорова–Смирнова. В случае ненормального распределения количественных признаков или неравенстве дисперсий применялся U-критерий Манна–Уитни. Для факторов, имеющих биноминальное распределение, дополнительно были рассчитаны 95% доверительные интервалы.
Результаты исследования
Пациентки всех групп были идентичны по возрасту, особенностям менструальной функции, наличию экстрагенитальных и гинекологических заболеваний, паритету. Эффективность прерывания беременности в поздние сроки методом амниоцентеза составила 93,3%, при применении простагландинов — 92%, на проспективном этапе не имела достоверных различий и составила 99,0% в основной группе и 96,9% — в группе сравнения.
В структуре выявленных ВПР плода на первом месте в основной группе были врожденные пороки сердечно-сосудистой системы (34 наблюдения — 34,7%), на втором — пороки центральной нервной системы (ЦНС) (29 наблюдений — 29,6%), на третьем — множественные пороки развития (13–13,3%), на четвертом — пороки мочевыводящей системы (9–9,2%) (табл. 1). В остальных наблюдениях выявлены ВПР опорно-двигательного аппарата (7–7,1%) и другие (6–6,1%): кожи и мышц, желудочно-кишечного тракта, легких, шеи и лица, прочие. В группе сравнения на первом месте также были врожденные пороки сердечно-сосудистой системы (32 наблюдения — 33,0%), на втором — пороки ЦНС (30 наблюдений — 30,9%), на третьем — множественные пороки развития (15–15,5%), на четвертом — пороки мочевыводящей системы (10–10,3%). В остальных наблюдениях выявлены ВПР опорно-двигательного аппарата (8–8,2%) и другие (2–2,1%): кожи и мышц, желудочно-кишечного тракта, легких, шеи и лица, прочие.
Среди пороков сердечно-сосудистой системы в обеих группах чаще наблюдались транспозиция магистральных сосудов, дефекты межжелудочковой и межпредсердной перегородок, общий артериовенозный канал, тетрада Фалло, сочетанные пороки сердца, аномалии Эбштейна, гипоплазия левого отдела, прочие врожденные пороки сердечно-сосудистой системы.
В структуре пороков ЦНС чаще наблюдалась гидроцефалия, анэнцефалия, синдром Арнольда–Киари и Денди–Уокера, микроцефалия, агенезия мозолистого тела, акрания, spina bifida (спинномозговая грыжа). Гидроцефалия — заболевание, характеризующееся избыточным накоплением цереброспинальной жидкости в желудочках и подоболочечных пространствах головного мозга, сопровождающееся их расширением и атрофией мозгового вещества.
В ходе ретроспективной оценки исследования последов в группе А в подавляющем большинстве наблюдений (78,7%) определялись серозно-гнойный и гнойно-некротический децидуит и лишь в небольшом проценте случаев (21,3%) наблюдался серозный децидуит. Также в этой группе отмечалось наличие дисциркуляторных нарушений (выраженный отек стромы ворсин, тромбоз межворсинчатого пространства, ретроплацентарные гематомы). В группе Б серозный париетальный децидуит определялся в большинстве случаев (54,7%), воспалительные изменения не определялись в 38,7% наблюдений, серозно-гнойный париетальный децидуит обнаружен в 6,6% случаев.
На ретроспективном этапе при исследовании последа в большей степени были обнаружены патологическое строение и пороки развития пуповины, чем в плаценте. Так, на первом месте среди признаков патологического строения пуповины была тощая пуповина: 19 наблюдений в основной группе (19,4%) и 21 (21,6%) в группе сравнения (табл. 2). На втором месте определялись ложные узлы пуповины: 16 (16,3%) и 17 (17,5%) соответственно исследуемым группам, на третьем месте — истинные узлы пуповины: 14 (14,2%) и 15 (15,5%). Нередко в структуре патологических вариантов строения пуповины было оболочечное прикрепление пуповины: 12 (12,2%) и 9 (9,3%) соответственно. Реже были выявлены гипо- и гиперизвитая пуповина: 8 (8,2%) и 7 (7,2%) соответственно исследуемым группам; единственная артерия пуповины: 6 (6,1%) и 4 (4,1%); гематома пуповины: 1 (1,0%) в основной группе и 2 (2,1%) в группе сравнения. Всего при исследовании нарушения строения пуповины были выявлены в 76 случаях основной группы и в 75 — группы сравнения, в целом в исследовании — в 77,4% наблюдениях.
При гистологическом исследовании плаценты отмечалась относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения (23 наблюдения — 23,5% в основной группе и 29–30,0% в группе сравнения). Серозный париетальный децидуит определялся в 17,3% наблюдений основной группы и 16,5% группы сравнения. Такие скудные изменения в плаценте, выявленные при исследовании, свидетельствуют о том, что ВПР плода, несовместимые с жизнью, чаще сочетаются с патологией строения пуповины, чем с нарушениями строения и пороками развития плаценты. Также относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения указывают на то, что прерывание беременности проводилось современным медикаментозным способом, который имитирует спонтанную сократительную деятельность матки и не вызывает грубых изменений в плаценте.
Таким образом, в структуре выявленных ВПР плода, несовместимых с жизнью, в исследуемых группах на первом месте были врожденные пороки сердечно-сосудистой системы, на втором — пороки ЦНС, на третьем — множественные пороки развития, на четвертом — пороки мочевыводящей системы. В остальных наблюдениях выявлены ВПР опорно-двигательного аппарата и другие: желудочно-кишечного тракта, дыхательной системы, шеи и лица, прочие.
При гистологическом исследовании плаценты ретроспективного этапа (до внедрения в акушерскую практику современных методов производства позднего индуцированного аборта) при проведении амниоинфузии гипертоническим раствором в подавляющем большинстве определялись серозно-гнойный и гнойно-некротический мембранит, при применении динопростона чаще наблюдался серозный париетальный децидуит. После внедрения в работу акушерско-гинекологической службы регламентирующего Приказа 572н при гистологическом исследовании плаценты у пациенток второго этапа обеих групп отмечалась относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения.
При исследовании последа чаще встречались пороки развития пуповины, чем плаценты. На первом месте среди признаков патологического строения пуповины была тощая пуповина, на втором месте — ложные узлы пуповины, на третьем — истинные узлы. Реже определялось оболочечное прикрепление пуповины. Значительно реже были выявлены гипо- и гиперизвитая пуповина, единственная пупочная артерия; гематома пуповины. При гистологическом исследовании плаценты отмечалась относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения. Скудные изменения в плаценте (в сравнении с изменениями в пуповине), выявленные при исследовании, свидетельствуют о том, что врожденные пороки развития плода, несовместимые с жизнью, чаще сочетаются с патологией строения пуповины, чем с плацентарными пороками. Также относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения указывают на то, что прерывание беременности проводилось современным медикаментозным способом, который имитирует спонтанную сократительную деятельность матки и не вызывает грубых изменений в плаценте.
Литература
* ФГБОУ ВО ОмГМУ МЗ РФ, Омск
** БУЗОО ОДКБ, Омск
Пренатальная диагностика уриномы как осложнения обструктивной уропатии
УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Введение
Врожденные пороки развития (ВПР) мочеполовой системы относятся к наиболее частым ВПР, выявляемым во время беременности (1-4 на 1000 беременностей [1]), и составляют 15-20 % в структуре пренатально диагностируемых ВПР [2]. Подавляющее большинство ВПР мочеполовой системы представлено обструктивными уропатиями. Это группа заболеваний, которые характеризуются наличием структурного или функционального препятствия нормальному оттоку мочи, приводящего к нарушению функции почек. При затруднении оттока мочи развивается расширение почечной лоханки (пиелоэктазия) или расширение не только лоханки, но и чашечек (гидронефроз).
Частота гидронефроза составляет 2,5-2,8 на 1000 плодов [3]. В подавляющем большинстве случаев подобные изменения являются преходящими (до 48 %) или физиологическими (до 15 %) и только около трети случаев врожденного гидронефроза вызваны наличием патологии мочевыводящих путей, к которой относится обструктивное поражение лоханочно-мочеточникового или пузырно-мочеточникового соустья, мегауретер, дисгенезия клоаки, пузырно-мочеточниковый рефлюкс, задние уретральные клапаны, мегацистис-микроколон-интестинальный гипоперистальтический синдром и др. Степень выраженности гидронефроза обусловлена его этиологией: чем выше уровень обструкции, тем выраженнее гидронефротическая трансформация почки. Дополнительными факторами при прогнозировании работы почки являются срок беременности, при котором возникла обструктивная уропатия, а также причины гидронефроза.
При обструкции на уровне лоханочномочеточникового соустья (ОЛМС) функция почки страдает в большей степени, нежели при других причинах гидронефроза. Характерными ультразвуковыми признаками обструкции высокого уровня являются расширение лоханки свыше 15 мм при отсутствии расширенного мочеточника и нормальные размеры мочевого пузыря.
ОЛМС практически всегда сопровождается выраженным гидронефрозом и развитием осложнений. Одним из таких осложнений является разрыв почечной лоханки и формирование уриномы или мочевого асцита.
Уринома представляет собой инкапсулированное скопление жидкости, вызванное экстравазацией мочи через периренальные пространства или разрывом почки и ее фасции. Наиболее частой причиной возникновения урином являются ОЛМС или задние уретральные клапаны. Дополнительными причинами являются мегауретер или (редко) пузырно-мочеточниковый рефлюкс [4]. Предполагается, что возникновение уриномы является защитным механизмом от повышения внутрипочечного давления, вызванного затруднением оттока мочи. Экстравазация мочи под почечную фасцию или в забрюшинное пространство способствует снижению давления, тем самым предохраняя почку от диспластических изменений. Существует и альтернативная гипотеза: наличие уриномы уже отражает тот факт, что развивающаяся почка подверглась воздействию высокого давления (достаточно высокого, чтобы привести к разрыву собирательной системы почки), и является одним из факторов, обусловливающих дисплазию почки и нарушение ее работы. Изолированная уринома, вызванная ОЛМС, почти всегда приводит к необратимому повреждению ипсилатеральной почки [5].
Ультразвуковым признаком уриномы является кистозное образование эллипсоидной формы или в виде полумесяца, прилегающее к почке или позвоночнику. Уриномы больших размеров могут принимать различные формы, растягивая и смещая почку. При этом направление смещения почки указывает на то, исходит ли уринома из переднего или заднего паранефрального пространства. Уриномы небольших размеров могут имитировать расширенную чашечку или лоханку, однако тщательная оценка коры почки помогает в проведении дифференциального диагноза.
Клиническое наблюдение 1
Пациентка Б., 32 лет, проходила плановое скрининговое обследование в 21-22 нед беременности, во время которого было обнаружено образование брюшной полости плода и назначен контрольный осмотр в срок 22-23 нед. После контрольного осмотра женщина была направлена в медико-генетическое отделение МОНИИАГ с диагнозом: «Киста левой почки? Образование в брюшной полости?».
Настоящая беременность от первого брака, по счету вторая. Супруги соматически здоровы, профессиональных вредностей не имеют, наследственность не отягощена. В анамнезе одни нормальные роды, ребенок здоров. На учете в женской консультации пациентка состояла с 7 нед. Беременность протекала без осложнений. Результаты скрининга I триместра патологии не выявили.
При ультразвуковом исследовании обнаружен один живой плод. Гестационный срок составил 22,1 нед. Фетометрические показатели соответствовали данному сроку. Патологических изменений плаценты и околоплодных вод не было выявлено.
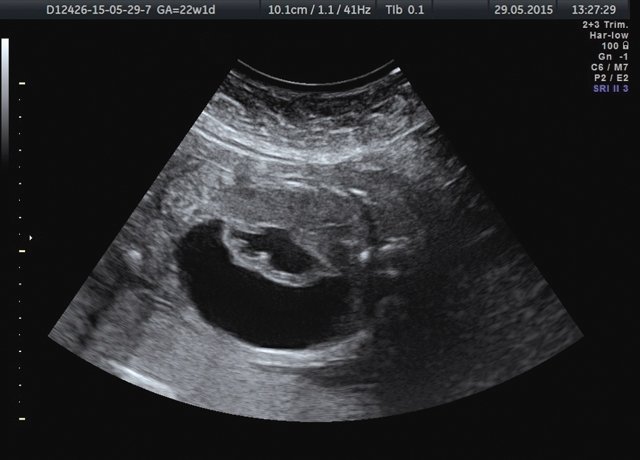
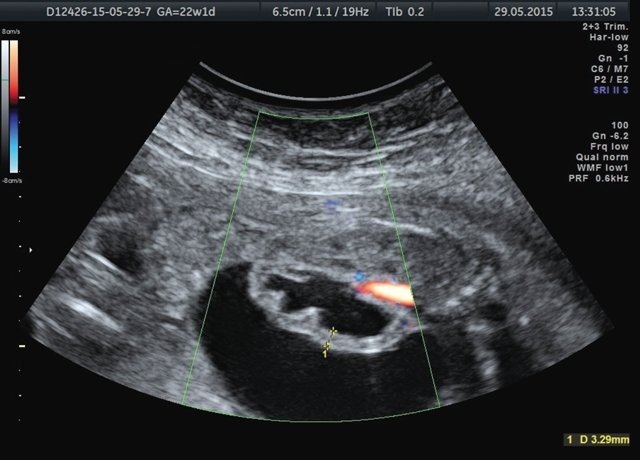
Лоханка правой почки была расширена до 13 мм, паренхима истончена и гиперэхогенна, кортикомедуллярная дифференцировка отсутствовала. При ЦДК кровоток в паренхиме не визуализировался. Вокруг правой почки по всему ее периметру определялось анэхогенное образование размером 56×20×26 мм (рис. 1, 2). Мочеточники с обеих сторон не визуализировались. Изменения левой почки отсутствовали. Мочевой пузырь был удовлетворительного наполнения и опорожнения. Оба надпочечника визуализировались.
Рис. 1. Образование вокруг правой почки плода.
Рис. 2. Истончение паренхимы правой почки плода с отсутствием кровотока в режиме ЦДК.
Изменений по остальным органам и системам не выявлено.
Клиническое наблюдение 2
Пациентка Х., 39 лет, после проведения планового скринингового исследования в 19-20 нед беременности по месту жительства обратилась в медико-генетическое отделение МОНИИАГ с направляющим диагнозом: «Киста забрюшинного пространства».
Настоящая беременность от первого брака, по счету третья. Супруги соматически здоровы, профессиональных вредностей не имеют, наследственность не отягощена. В анамнезе двое нормальных родов, оба ребенка здоровы. На учете в женской консультации пациентка состояла с 10 нед. Беременность протекала без осложнений. Результаты скрининга I триместра отклонений не выявили.
При ультразвуковом исследовании обнаружен один живой плод мужского пола. Гестационный срок составил 20,2 нед. Фетометрические показатели соответствовали данному сроку. Патологических изменений плаценты и околоплодных вод не было выявлено.
Рис. 3. Кистозное образование у верхнего полюса левой почки плода.
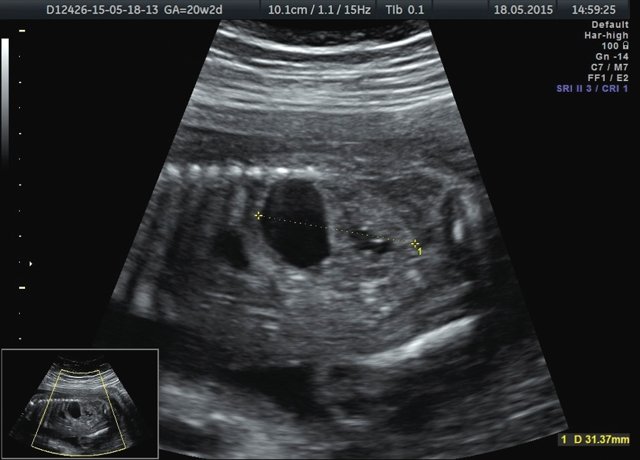
Область правой почки занимало округлое тонкостенное анэхогенное образование до 36 мм в диаметре. Правая почка была уменьшена в размерах до 17×9×20 мм, смещена и располагалась, распластываясь в виде полумесяца по задней поверхности образования (рис. 4). Правый мочеточник не визуализировался. Паренхима обеих почек была повышенной эхогенности, кортикомедуллярная дифференцировка почечных слоев нечеткая.
Рис. 4. Образование возле правой почки и расширенный мочевой пузырь плода.
Надпочечники с обеих сторон были интактны. Мочевой пузырь был увеличен до 20 мм в диаметре, с утолщенными стенками и в процессе динамического осмотра не опорожнялся (рис. 5). Изменений по остальным органам и системам не было выявлено.
Рис. 5. Расширенный мочевой пузырь плода.
Обсуждение
В представленных клинических наблюдениях надпочечники были интактны, а выявленные образования визуализировались непосредственно рядом с почками. В наблюдении 1 контуры образования повторяли контуры капсулы почки, а в наблюдении 2 образование слева имело общую с почкой капсулу. В связи с этим мы сделали вывод о том, что данные образования исходят из почек и являются следствием обструктивной уропатии.
В первом наблюдении, принимая во внимание контуры образования и его локализацию, расширение лоханки и изменения почечной паренхимы, был поставлен диагноз: «Беременность 22,1 нед. ВПР мочеполовой системы: УЗ-признаки уриномы правой почки на фоне обструктивной уропатии». Поскольку изменения второй почки и мочевого пузыря отсутствовали, правосторонняя обструктивная уропатия была наиболее вероятной причиной возникновения уриномы.
Во втором наблюдении поражение почек было двусторонним. Изменения левой почки были характерными ультразвуковыми проявлениями уриномы. Наличие кистозного образования, тесно прилегающего к почке, незначительное расширение лоханки и нечеткая кортикомедуллярная дифференцировка свидетельствовали о воздействии на почку высокого давления из-за нарушения оттока мочи с последующим разрывом почечной паренхимы и формированием уриномы.
Ультразвуковые изменения правой почки были более выраженными. По заднему краю образования диаметром 36 мм была распластана сама почка. Мочеточники с обеих сторон не визуализировались ни на одном из своих участков вплоть до места впадения в мочевой пузырь. Нормальное количество околоплодных вод, мужской пол плода, отсутствие расширенных мочеточников на фоне относительно небольшого увеличения размеров мочевого пузыря позволили нам исключить атрезию уретры, синдром задних уретральных клапанов и мегацистис-микроколон-интестинальный гипоперистальтический синдром и предположить наличие обструктивного поражения мочевыводящих путей на высоком уровне.
Учитывая большие размеры урином как в первом, так и во втором наблюдениях, в качестве причины возникновения обструктивной уропатии мы предположили одностороннее отсутствие или атрезию мочеточника у обоих плодов.
ОЛМС встречается преимущественно у мальчиков (соотношение мальчиков и девочек составляет 3:1). До 40 % случаев поражение двустороннее, у 10 % плодов выявляются экстраренальные изменения [6]. ОЛМС может быть как функциональным (чаще всего), так и анатомическим. К последним можно отнести стеноз, атрезию мочеточника или его врожденное отсутствие (агенезию).
Агенезия мочеточника встречается крайне редко и обычно сочетается с отсутствием почки или ее дисплазией и может быть как одно-, так и двусторонней. Чаще встречается атрезия мочеточника, которая возникает вследствие нарушения или отсутствия канализации растущего мочеточникового зачатка и может локализоваться на разных уровнях: в лоханочно-мочеточниковом, пузырно-мочеточниковом сегментах или на уровне пересечения мочеточников подвздошными сосудами. Атрезия сопровождается гидронефрозом и дисплазией почки. Мочеточник чаще всего заканчивается слепо и резко расширяется выше уровня атрезии, но может иметь вид фиброзного тяжа [7].
В наблюдении 2 семья приняла решение о досрочном прекращении беременности, однако отказалась от последующего патолого-анатомического исследования плода, в связи с чем наше предположение о генезе ОЛМС осталось неподтвержденным. Двусторонняя атрезия или агенезия мочеточников является летальным пороком. При одностороннем поражении прогноз обусловлен характером осложнений. По данным J. Hutcheson и соавт. [10], развитие уриномы является менее благоприятным в отношении сохранности почечной функции, чем развитие мочевого асцита. Важными являются и размеры уриномы. При уриноме больших размеров прогноз для плода чаще всего неблагоприятный. В первую очередь это связано с потерей функции пораженной почки как результатом воздействия высокого давления на почечную ткань. Так, в случае, представленном A. Ghidini и соавт. [11], описывается правосторонняя уринома большого размера (3,5×5,5 см), которая спонтанно исчезла вскоре после родов, и ультразвуковые признаки изменения мочевыводящих путей отсутствовали, однако спустя год у ребенка была выявлена инволюция правой почки.
Дополнительным фактором, усугубляющим прогноз при уриноме больших размеров, является гипоплазия легких. Этому способствует выраженный длительный подъем купола диафрагмы в результате повышенного внутрибрюшного давления, а также развивающееся в некоторых случаях маловодие [10].
Представленные клинические наблюдения отражают разнообразие ультразвуковых проявлений уриномы: от жидкостного образования, расположенного вокруг неизмененной по форме почки и повторяющего ее контуры, до образования, растягивающего и смещающего почку в разных направлениях. Уриномы могут достигать больших размеров и быть как одно‑, так и двусторонними. Их необходимо дифференцировать с опухолями почек, надпочечников и забрюшинного пространства, кистами почек, брыжейки и желудочно-кишечного тракта. Однако выявление связи образования с почкой и оценка почечной капсулы, а также наличие наиболее вероятных причин формирования урином (ОЛМС, задние уретральные клапаны) позволяют поставить правильный диагноз.
Заключение
Причина развития ОЛМС и возникновения уриномы чаще всего недоступна для пренатальной диагностики, однако, помимо наиболее известных этиологических факторов, врачу, проводящему исследование, необходимо помнить и о таких редких врожденных пороках развития, как атрезия или агенезия мочеточника, особенно в случае больших размеров уриномы.
Литература
УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
_575.gif)