пересадка костного мозга при лейкозе последствия
Пересадка костного мозга при онкологических заболеваниях крови
Впервые сталкиваясь с таким страшным диагнозом, как, лейкоз, или лейкемия, лимфома – у человека после первого шока начинается хаос в голове из огромного количества вопросов: как, почему я, или мой ребенок, что делать, как лечить, какие шансы, нужна ли пересадка костного мозга, где найти донора…
Ниже мы выстроили систему из этих вопросов и попробуем ответить на каждый. Это и будет неким планом действий для человека, которому поставили диагноз – рак крови.
Как диагностировать рак крови?
Как лечить лейкоз, лейкемию или лимфому? Можно ли вылечить навсегда?
Какая бывает пересадка костного мозга? Где найти донора?
Как происходит пересадка костного мозга? Что делают перед ТКМ? Сколько времени занимается вся процедура пересадки?
Сколько стоит пересадка костного мозга?
Где лучше делать трансплантацию?
Какой прогноз после пересадки костного мозга?
Как определить рак крови: лейкоз, лейкемию. Как выявить лимфому?
Виды рака крови:
Как диагностировать рак крови на ранней стадии, как он проявляется и как его заметить самостоятельно?
Внимание на симптомы:
Вы заметили эти симптомы у себя? У ребенка? Если испытываете подобные симптомы больше 1-2 недель, срочно проходите первичное обследование, а именно:
Именно по общему анализу крови врач может распознать серьезные отклонения от нормы. Если это случилось, необходимо делать пункцию и проводить иммуногистохимический анализ клеток костного мозга для определения вида рака крови.
Далее, в зависимости от типа рака крови, грамотный врач должен обследовать пациента с помощью ПЭТ КТ, или МРТ, КТ, сцинтиграфии.
Как лечить лейкоз, лейкемию или лимфому? Можно ли вылечить навсегда?
Как лечится рак крови:
Ранняя стадия рака лейкоза, лейкемии или лимфомы: у 75% пациентов ремиссия наступает уже при первой линии лечения цитостатиками и химиотерапией.
Важно: первая линия лечения может длиться от 3 до 9 месяцев.
Вторая и третья стадии лимфомы, лейкемии и остром лейкозе: кроме цитостатиков и химиотерапии, применяют таргетную терапию и иммунотерапию. Комплексное лечение серьезно повышает шансы онкологического пациента на выход в ремиссию.
Важно: иммунотерапия не применяется как самостоятельный метод лечения рака крови, этот новейший метод биологического лечения является сильным вспомогательным лечением.
Четвертая, терминальная стадии, рецидив: требуется пересадка костного мозга, от донора или собственных стволовых клеток.
Важно: Некоторые виды лейкоза, лейкемии и лимфом даже на ранних стадиях предполагают впоследствии пересадку костного мозга. Поэтому если полученный диагноз по протоколу предполагает в будущем ТКМ (трансплантацию), сразу сдавайте анализы на типирование антигенов HLA сами и все ваши родные. Заранее определитесь, подходит ли кто-то из родственников как донор.
Какая бывает пересадка костного мозга? Где найти донора?
Виды трансплантации:
Как происходит пересадка костного мозга? Что делают перед ТКМ? Сколько времени занимается вся процедура пересадки?
Пересадка костного мозга является либо завершающим этапом лечения, когда предыдущие методы не дали 100% положительного результата, либо основным при рецидиве рака крови.
В случае аллогенной трансплантации забор клеток костного мозга производится у донора. Напомним, что 9 пациентам из 10 необходимо ожидать в очереди на получение донора из общей базы при совпадении антител HLA.
Если планируется пересадка собственных стволовых клеток костного мозга, то забор этих клеток делают заранее. Если от донора, то незадолго до процедуры. Особая подготовка не требуется, только обследование.
Стволовые клетки для пересадки берут из тазовой кости пункцией, однако, наиболее современный и щадящий способ – это фильтрование стволовых клеток из периферийной крови после лекарственной стимуляции выброса нужных клеток в кровь (недельный прием препарата). Болезненные последствия для донора или самого пациента отсутствуют. Не больно.
Перед процедурой необходимо буквально «убить» собственный костный мозг, который производит мутированные кровяные клетки. Для этого проводится интенсивная высокодозная химиотерапия или высокоточная лучевая терапия. Если вариант ТКМ с донором, то дополнительно применяют большие дозы иммуносупрессоров, чтобы организм сразу не отверг чужой костный мозг.
Операция по пересадке костного мозга не что иное, как переливание, ведь костный мозг выглядит просто как пакет крови для переливания.
На 2-4 недели после пересадки пациента помещают в стерильную палату клиники, так как он находится в состоянии цитопении: старый костный мозг убит и не работает, новый костный мозг еще не прижился. В этот период для пациента опасны любые возможные инфекции, даже самые незначительные.
Еще в течение 2 месяцев после выписки из стерильной палаты пациента наблюдают или стационарно или амбулаторно. Каждую неделю он сдает анализы крови, мочи, находится под контролем своего онколога.
По окончании всего этапа лечения, пациент проходит обследование каждые 3 месяца в течение 1 года. Далее еще 4 года – каждые 6 месяцев. Перешагнув 5-летний рубеж выживаемости, пациент вступает в период длительной ремиссии, что в 80% случаях означает полное излечение. Обследование раз в год!
Итак, вся процедура трансплантации костного мозга при лейкозе крови, лейкемии, при множественной миеломе (миеломной болезни), лимфоме Ходжкина и неходжкинской лимфоме занимает 3-4 месяца.
Высокодозная химиотерапия и трансплантация костного мозга у взрослых больных
Трансплантация стволовых гемопоэтических клеток нашла применение в различных областях онкологии.
Эти клетки используются после высокодозной химиотерапии для снижения длительности депрессии (угнетения) костного мозга и сокращения риска инфекционных осложнений и кровотечений.
Стволовые клетки для трансплантации получают как от самого пациента (аутологичная трансплантация), так и от иммунологически совместимого родственного или неродственного донора (аллогенная трансплантация). Непосредственным источником стволовых гемопоэтических стволовых клеток может быть костный мозг, периферическая или пуповинная кровь.
Одним из наиболее частых показаний для применения стволовых клеток в онкологии является уменьшении длительности периода угнетения кроветворения после противоопухолевой терапии.
Применение современных противоопухолевых препаратов позволяет излечить или продлить жизнь значительному количеству больных со злокачественными новообразованиями.
Однако в ряде случаев проведение стандартной химиотерапии не приводит к длительному противоопухолевому эффекту, что связано с исходной или приобретенной резистентностью (устойчивостью) опухоли к цитостатикам.
Одним из путей ее преодоления является увеличение дозы препаратов. Это увеличивает проникновение противоопухолевых препаратов в раковую клетку и позволяет преодолеть устойчивость к химиотерапии.
Резкое увеличение дозы препаратов приводит к значительному повреждению кроветворных клеток костного мозга и выключению функции кроветворения на много месяцев, что требует применения методик защиты кроветворения.
Основным методом, позволяющим преодолеть токсичность химиотерапии на кроветворение, является трансплантация кроветворной ткани. При этом стволовые клетки, полученные от донора или у самого больного, вводят после окончания химиотерапии, когда препараты полностью вывелись из организма или разрушились, что позволяет быстро восстановить кроветворение.
При пересадке аллогенного костного мозга возможно длительное приживление трансплантата только при совпадении донора и реципиента по антигенам главного комплекса гистосовместимости (иммунологической совместимости).
В противном случае развивается выраженная иммунологическая реакция «трансплантат против хозяина» (РТПХ), способная привести к гибели больного.
Наименьшее количество осложнений встречается у совместимых сибсов (родных братьев и сестер).
В то же время сибсы имеют вероятность совпасть иммунологически только в 25% случаев, что указывает на серьезную проблему подбора доноров для пересадки костного мозга. Последние годы отмечены крупные успехи в подборе неродственных доноров.
Следует отметить, что даже полная совместимость не дает абсолютной гарантии отсутствия развития РТПХ, и до 25% больных погибает от осложнений, связанных с трансплантацией.
Важно иметь в виду, что РТПХ способна оказывать и лечебное действие, когда иммунная система донора начинает распознавать опухолевые клетки хозяина и бороться с ними, т.е. проявляется реакция трансплантат против опухоли (РТПО).
При ряде заболеваний (хронический миелолейкоз, острый нелимфобластный лейкоз и др.) наличие этой реакции в значительной степени определяет общий успех лечения.
Трансплантация аутологичной (своей собственной) гемопоэтической ткани позволяет избежать возникновения РТПХ и технических сложностей, связанных с подбором донора. С другой стороны, аутологичная трансплантация не сопровождается РТПО и несет чисто вспомогательную функцию поддержки кроветворения после высокодозной химиотерапии.
В настоящее время имеется возможность сохранять собственные кроветворные клетки в жизнеспособном состоянии при низких температурах (замораживании) в течение длительного периода времени.
Долгие годы основным источником стволовых кроветворных клеток был костный мозг. Метод его получения состоит в многократных пункциях плоских костей (в основном тазовых) и получении 1-1,5 литров костно-мозговой взвеси. Такая процедура требует, как правило, общего обезболивания (наркоза).
Нужно отметить, что при опухолевом и лучевом поражении костей таза забор костного мозга может оказаться неудачным.
Костный мозг не является единственным источником кроветворных клеток.
Во взрослом организме небольшая часть стволовых клеток, как и зрелые клетки, выходит в периферическое сосудистое русло. Эти стволовые клетки способны восстанавливать полноценное кроветворение после повреждения его химиотерапией и облучением. Современная аппаратура (сепараторы крови) позволяет эффективно собирать клетки кроветворения из периферической крови даже при их низком содержании. При этом необходимость наркоза отпадает.
В условиях нормального кроветворения для получения достаточного количества стволовых клеток необходимо, как правило, 6 процедур. При каждой такой процедуре обрабатывается 10-12 литров крови.
Проблема низкого количества клеток кроветворения в периферической крови оставалась главным ограничением при использовании данного вида трансплантата. Затем было показано, что после однократного введения некоторых противоопухолевых препаратов (циклофосфамид, этопозид, фторурацил) отмечается значительное увеличение числа стволовых клеток в периферической крови. К недостаткам данного метода относятся: снижение числа лейкоцитов и тромбоцитов, значительные различия в сроках начала роста содержания стволовых клеток в периферической крови у различных больных.
Введение некоторых гемопоэтических факторов роста (нейпоген, лейкомакс и др.) вызывает значительно увеличение поступления клеток кроветворения из костного мозга в периферическую кровь.
Применение аллогенной трансплантации костного мозга
В настоящее время основными показаниями для аллогенной трансплантации стволовых клеток являются
Изучаются возможности применения данного метода у больных
Острые нелимфобластные лейкозы (ОНЛЛ)
Применение стандартной химиотерапии в первой полной ремиссии позволяет добиться длительной выживаемости в 25-35% случаев по сравнению с 45-60% при использовании аллогенной трансплантации стволовых клеток. Применение трансплантации во второй ремиссии сопровождается длительной ремиссией лишь в 20-30% случаев.
Использование аллогенной трансплантации стволовых клеток с первично резистентным (устойчивым к лечению) течением ОНЛЛ позволяет добиться длительной ремиссии в 10-20% случаев.
Острые лимфобластные лейкозы (олл)
Проведение аллогенной трансплантации стволовых клеток в первой полной ремиссии у пациентов с неблагоприятными прогностическими факторами (возраст старше 60 лет, высокий лейкоцитоз и т.д.) позволяет достичь длительной безрецидивной выживаемости в 40-60% случаев.
При отсутствии неблагоприятных факторов аллогенная трансплантация стволовых клеток обычно рекомендуется во второй полной ремиссии.
Хронический миелолейкоз
ХМЛ характеризуется несколькими фазами развития. В ранней (хронической) фазе, длящейся несколько лет, состояние больного может сохраняться относительно удовлетворительным. В фазе акселерации (обострения) в течение нескольких месяцев нарастают гематологические изменения (увеличение числа лейкоцитов, малокровие), и она переходит в фатальную (смертельную) фазу бластного криза.
Стандартные методы лечения могут вызывать длительные ремиссии у части больных, однако единственным излечивающим методом лечения в настоящее время является аллогенная трансплантация стволовых клеток. Эффективность ее зависит от возраста больного, фазы заболевания, периода времени от момента диагноза до трансплантации. Множественные курсы предшествующего лечения значительно улучшают результаты высокодозной химиотерапии и трансплантации.
Наилучшие шансы на достижение длительной ремиссии имеют молодые больные, получившие трансплантацию в хронической фазе в течение 1 года от момента диагноза. Длительная выживаемость у них составляет 75-80% по сравнению с 10-20% у больных, которым трансплантация выполнена в фазе аскселерации.
Миелодиспластический синдром
Аллогенная трансплантация стволовых клеток является единственным методом, излечивающим больных МДС. Применение этого метода позволяет добиться длительной выживаемости в 30-50% случаев. Эти результаты зависят от возраста больных, длительности заболевания и количества опухолевых клеток в костном мозге перед трансплантацией.
Аллогенная минитрансплантация
Аллогенная минитрансплантация, или трансплантация после миелоаблативных (не разрушающих костномозговое кроветворение) режимов получила распространение лишь недавно. Ее применение связано с выявлением лечебной роли РТПО и появлением новых препаратов (флударабин, антитимоцитарный иммуноглобулин), вызывающих глубокую депрессию (угнетение) иммунной системы, но не вызывающих глубокой цитопении (снижение числа клеток крови).
Применение их в комбинации с умеренными дозами бусульфана или мелфалана позволяет эффективно пересаживать донорский костный мозг. При этом РТПО полностью сохраняется. Следует отметить, что эффективность этого метода зависит от массы остаточной опухоли, которая должна быть по возможности минимальной.
Предварительные результаты применения данной методики свидетельствуют о высокой эффективности минитрансплантации при значительно меньшей токсичности в сравнении с классическим методом.
Применение аутологичной трансплантации костного мозга
Основной ролью аутологичной трансплантации костного мозга является восстановление кроветворения после химиотерапии, что позволяет многократно увеличивать разовые дозы некоторых противоопухолевых препаратов. Это дает возможность усиливать противоопухолевый эффект и достигать более высокой безрецидивной выживаемости в сравнении с результатами стандартной химиотерапии.
Наиболее часто данный метод применяется при лечении больных с прогностически неблагоприятными вариантами течения неходжкинских лимфом (лимфосарком), болезни Ходжкина (лимфогранулематоза), множественной миеломы, рака молочной железы, рака яичка и пр.
Неходжкинские лимфомы (нхл)
Применение стандартной химиотерапии у больных с НХЛ высокой и промежуточной степени злокачественности позволяет достичь 40-60% полных ремиссий. Однако у 20-30% больных этой группы отмечаются рецидивы (возврат) болезни. Применение высокодозной химиотерапии в сочетании с аутологичной трансплантацией костного мозга дало возможность значительно улучшить показатели длительной выживаемости у таких больных.
Болезнь ходжкина
У 10-30% больных с распространенными стадиями болезни Ходжкина первичная химиотерапия оказывается неэффективной, а у 40% пациентов возникает рецидив заболевания. Результаты лечения больных, малочувствительных к первичной химиотерапии и с первым ранним рецидивом (в течение первого года), неудовлетворительные.
Применение других схем стандартной химиотерапии позволяет достичь полных ремиссий не более чем у 40-45% больных, однако при этом ремиссии бывают короткими, а выживаемость низкая.
Применение высокодозной химиотерапии в сочетании с аутологичной трансплантацией стволовых клеток позволяет почти в 2 раза увеличить частоту полных ремиссий, а значит, и надежду на увеличение выживаемости.
Множественная миелома
По данным Европейской организации по аутологичным трансплантациям костного мозга, безрецидивная и общая выживаемость 5500 больных множественной миеломой, получавших высокодозную химиотерапию в сочетании с аутологичной трансплантацией стволовых клеток, составила соответственно 28 и 48 месяцев, что превышает результаты стандартной химиотерапии.
Наилучший прогноз (исход) имеют больные моложе 60 лет с I-II стадиями заболевания и уровнем бета-2 микроглобулина менее 4.
Использование высокодозной химиотерапии при других опухолях (рак молочной железы, яичка и др.) находится на этапе изучения. При этом получены обнадеживающие результаты.
Таким образом, высокодозная химиотерапия с трансплантацией аутологичных или аллогенных стволовых кроветворных клеток за последние годы стала эффективным методом лечения многих опухолей. Прогресс в биологии и иммунологии клеток кроветворения позволяет надеяться на еще более эффективное применение этого метода в будущем, в том числе и при распространенных новообразованиях, резистентных (устойчивых) к химиотерапии.
Мероприятия 2021/2022 года
Архив мероприятий
Противораковое общество РОССИИ создано по инициативе ученых-онкологов и главных врачей онкологических диспансеров, представляющих более 50 регионов России, с целью претворения в жизнь программы профилактики рака в России
Пересадка костного мозга при лейкозе последствия
Современная стратегия терапии острого миелоидного лейкоза (ОМЛ) определяется максимально возможным использованием потенциала интенсивной индукции, консолидации и поддерживающего лечения.
Во-первых, трансплантация стволовых гемопоэтических клеток всегда является этапом в лечении больных острым миелоидным лейкозом; во-вторых, всегда подразумевается отбор больных в соответствии с их возрастом и соматическим статусом, адекватностью химиотерапии, развитием рецидива до выполнения ТКМ, наличием HLA-совместимого донора (для аллогенной ТКМ); в-третьих, сравнение результатов лечения больными, которым проводят химиотерапию или выполняют трансплантацию, возможно лишь на основе анализа рандомизированных групп в рамках многоцентровых кооперированных исследований; в-четвертых, эффективность выполнения ТКМ необходимо оценивать в зависимости от цитогенетических аномалий, которые определяют течение заболевания.
К концу 2001 г. завершены 4 многоцентровых рандомизированных исследования, проведенных в Европе и США. Их цель — сравнить эффективность постремиссионной терапии острого миелоидного лейкоза, выполненной в 3 вариантах: в виде интенсивной химиотерапии, аутологичной и аллогенной ТКМ. В настоящем анализе данные отдельных исследовательских центров не учитываются.
Безрецидивная и общая выживаемость больных, которым выполнили аутологичную трансплантацию костного мозга (ТКМ) или осуществляли химиотерапию
В таблице приводится описание основных этапов лечения в рандомизированных исследованиях, проведенных итальянской исследовательской группой (GIMEMA) совместно с общеевропейской (EORTC), а также французской (GOELAM), американской (US Intergroup) и английской (MRC) группами.
Аутологичная трансплантация костного мозга является высокодозной консолидацией полной ремиссии острого миелоидного лейкоза (ОМЛ). Удалось полностью выполнить программу лечения, предусмотренного в исследованиях, по данным группы EORTC+GIMEMA, в 74,2 % случаях при запланированной аутотрансплантации и в 82,5 % — химиотерапии, во французском исследовании GOELAM в 87,2 и в 71 % соответственно, в объединенной американской группе — в 60 и 92 % соответственно и в Великобритании в 66,3 % в случае запланированной аутологичной ТКМ.
Частота развития рецидивов и смертность среди больных, которым проводили химиотерапию или выполняли аутологичную трансплантацию костного мозга (ТКМ)
Таким образом, процент выполняемости запланированной терапии достоверно отличается в зависимости от выбранной по случайному признаку программы лечения: аутологичная ТКМ — 71 %, химиотерапия — 88 %. Эти различия, по-видимому, характеризуют аутологичную ТКМ как рискованный метод лечения, требующий принятия очень ответственных решений как больным, так и врачом.
Ее долгосрочная эффективность по сравнению со стандартной консолидацией отражена в таблице. Анализ проведен по принципу «намерение лечить», т. е. в анализ включали всех больных независимо от того, выполнили ли им запланированное лечение или нет.
Безрецидивная выживаемость больных, которым выполнена аутологичная трансплантация костного мозга или проведена химиотерапия, в зависимости от группы прогноза, определенного по цитогенетическим маркерам
Результаты исследования MRC-10 целесообразно рассмотреть отдельно, поскольку в нем оценивали эффективность аутологичной ТКМ, выполняемой как пятый курс химиотерапии, в сравнении с 4 курсами химиотерапии и прекращением лечения после них. Это исследование доказало, что аутологичная трансплантация костного мозга достоверно улучшает безрецидивную выживаемость больных — 54 % в сравнении с 40 %, при этом авторы подчеркивают, что неясно, сама ли трансплантация костного мозга или дополнительный пятый курс химиотерапии сыграли принципиальную роль.
Последующее исследование MRC-12, сравнивающее эффективность 5 курсов химиотерапии и 4 в сочетании с аутологичной трансплантации костного мозга, показало отсутствие различий между двумя подходами. Общая выживаемость 1224 больных, включенных в исследование, одинакова при проведении 4 или 5 курсов. Тем не менее исследователи отмечают некоторые преимущества у больных в возрасте 15—35 лет после проведения им 5-го курса химиотерапии.
Безрецидивная выживаемость больных в зависимости от числа лейкоцитов и варианта ОМЛ по данным французского исследования
Достоверные различия по безрецидивной выживаемости у больных ОМЛ при проведении аутологичной трансплантации костного мозга получены еще в одном из приведенных в таблице исследований — EORTC+GIMEMA. При выполнении аутологичной трансплантации костного мозга безрецидивная выживаемость составила 48 % в сравнении с 30 % при химиотерапии. Предметом критики в этом исследовании стали результаты стандартной химиотерапии. Некоторые авторы расценивают 30 % безрецидивную выживаемость у больных моложе 55 лет как крайне низкий показатель, обусловленный недостаточной адекватностью химиотерапии.
Как видно из таблицы, вероятность развития рецидивов после выполнения аутологичной трансплантации костного мозга значительно меньше (притом, что аутологичная трансплантация костного мозга осуществлена лишь 70 % больных из всех рандомизированных на этот вариант терапии). Однако высокая летальность, обусловленная трансплантацией, нивелирует преимущества последней при анализе безрецидивной выживаемости.
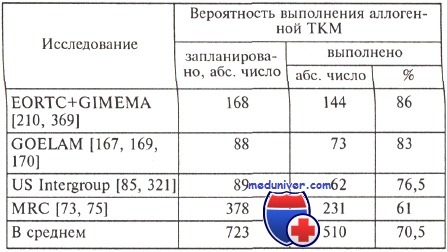
Выполняемость аллогенной трансплантации костного мозга
Анализ эффективности аутологичной трансплантации костного мозга в зависимости от группы прогноза, определенной по цитогенетическим маркерам, не позволяет сделать однозначные выводы. Это связано как с противоречивостью данных, так и с малым числом больных. Данные представлены в таблице.
Как видно из таблице, по результатам исследований MRC и US Intergroup безрецидивная выживаемость после выполнения аутологичной трансплантации костного мозга у больных из группы благоприятного прогноза выше. У больных из группы среднего прогноза преимущества аутологичной трансплантации костного мозга выявлены лишь в исследовании US Intergroup. Одинаково малоэффективной трансплантации костного мозга оказалась у больных из группы неблагоприятного прогноза, однако следует отметить, что показатели безрецидивной выживаемости у этих больных значительно отличаются в каждом исследовании. Это позволяет сделать вывод о том, что в американском исследовании программа химиотерапии менее интенсивная.
При отсутствии возможности оценивать цитогенетические маркеры в анализ прогностических факторов могут быть включены такие простые параметры, как число лейкоцитов в дебюте заболевания и вариант острого миелоидного лейкоза (ОМЛ).
Данные французского исследования GOELAM демонстрируют, что различий в 4-летней безрецидивной выживаемости в зависимости от числа лейкоцитов в дебюте заболевания (более или менее 30 • 109/л) и варианта ОМЛ при сравнении эффективности аутологичной трансплантации костного мозга и интенсивной консолидации не получено. Вывод этого исследования — выполнение аутологичной трансплантации костного мозга больным ОМЛ в период первой полной ремиссии не обязательно. Однако число больных в группах крайне невелико, и большинство исследователей указывают, что аутологичная трансплантация костного мозга может быть включена в программу терапии больных в период первой полной ремиссии ОМЛ при условии снижения летальности, связанной с самой трансплантацией.
Безрецидивная 5-летняя выживаемость больных острым миелоидным лейкозом в зависимости от группы прогноза и наличия у них HLA-совместимого донора
Эффективность аллогенной трансплантации костного мозга зависит не только от мощного лучевого и выраженного цитостатического воздействий, но и от реакции иммунной системы донора костного мозга на опухолевые клетки больного (реакция трансплантат против лейкоза). Именно иммунные механизмы обеспечивают основное противоопухолевое воздействие. К сожалению, у большинства пациентов HLA-совместимого донора нет. По данным обсуждаемых исследований, HLA-совместимого донора определяли у 22—26 % больных, у которых была достигнута полная ремиссия.
Причем учитывали только больных в возрасте максимально до 45 лет, при котором возможно было проведение аллогенной трансплантации костного мозга. Число больных, которым выполнили запланированную ранее аллогенную трансплантацию костного мозга, по данным разных исследований, колеблется от 60 до 86 %. Данные по выполняемости аллогенной трансплантации костного мозга представлены в таблице.
Существенные различия между запланированными и реально выполненными трансплантациями могут быть связаны с токсичностью предшествующей химиотерапии, с развитием ранних рецидивов, отказами пациентов.
Анализ ее эффективности следует проводить по так называемому принципу — донор есть/донора нет. В группу «донор есть» включают больных, у которых имеется HLA-совместимый донор, а в группу «донора нет» тех, у кого HLA-совместимый донор отсутствует. В группе «донор есть» анализируют результаты лечения всех больных независимо от того, выполнили им аллогенную трансплантацию костного мозга или нет.
Частота развития рецидивов у больных, которым выполнили аллогенную трансплантацию костного мозга или провели химиотерапию
В таблице приведены показатели 5-летней безрецидивной выживаемости больных в зависимости от наличия или отсутствия у них HLA-совместимого донора и группы прогноза, определенного по цитогенетическим маркерам, в трех исследованиях: MRC, US Intergroup, EORTC+GIMEMA.
Следует напомнить, что в группе «есть донор» представлены показатели больных, большинству из которых (в среднем 70 %) выполнили аллогенную трансплантацию костного мозга. Так же как и при анализе результатов аутологичной трансплантации костного мозга, становится очевидной разнородность результатов аллогенной трансплантации костного мозга. Так, если в английском исследовании MRC аллогенная трансплантация костного мозга имеет преимущество перед химиотерапией лишь у больных из группы среднего прогноза, то в американском исследовании US Intergroup статистически достоверные различия в пользу аллогенной трансплантации костного мозга получены у больных из группы благоприятного и неблагоприятного прогноза.
В европейском исследовании EORTC+GIMEMA, итоги которого подводились в 2001 г., показатели безрецидивной выживаемости во всех группах статистически не отличаются. По данным 2004 г., показатели безрецидивной выживаемости больных из разных прогностических групп были практически такими же, за исключением группы высокого риска: у больных из группы благоприятного прогноза — 61 % (донор есть) и 66 % (донора нет), промежуточного прогноза — 45 % (донор есть) и 49 % (донора нет), плохого прогноза —43 % (донор есть) и 18,4 % (донора нет).
Бесспорным доказательством преимущества аллогенной трансплантации костного мозга может служить анализ терапии 149 больных ОМЛ (15—55 лет), которых наблюдали и лечили в Северном регионе Великобритании. Так, полная ремиссия была достигнута у 74 % больных в возрасте до 40 лет и у 58 % — в возрасте от 40 до 55 лет. После проведения двух курсов индукции и двух курсов консолидации (протокол MRC-10) всем больным терапию прекращали. Тем больным, у которых были HLA-совместимые доноры, выполняли аллогенную ТКМ. У 28 больных моложе 40 лет выявили HLA-совместимых родственных доноров, 22 из них провели аллогенную ТКМ (одну — сингенную). Безрецидивная 4-летняя выживаемость с момента достижения полной ремиссии составила 24 % у больных, которым выполнили программу химиотерапии, и 62 % у больных, которым провели аллогенную ТКМ. Конечно, число анализируемых больных невелико.
Сравнительная оценка эффективности химиотерапии и аллогенной трансплантации костного мозга близнецовым методом
Кроме того, приведены результаты лечения, которое осуществляли в одном исследовательском центре, однако преимуществом этого исследования является то, что в анализ включены все заболевшие ОМЛ в одном географическом регионе и им четко выполнили программу лечения. Вывод однозначный — при наличии донора следует выполнять аллогенную ТКМ.
По данным Международного регистра, за период с 1988 по 1995 г. больным ОНЛЛ было выполнено в общей сложности 3503 аллогенных ТКМ от родственного донора и 208 от неродственного, 1403 аутологичных ТКМ. С учетом значительной селекции пациентов получены хорошие результаты у больных в первой ремиссии, во второй ремиссии и в развернутой фазе болезни. Более 5 лет без рецидива живут 59 % больных ОНЛЛ в первой ремиссии, 35 % во второй полной ремисии и 25 % больных, которым ТКМ была выполнена вне полной ремиссии.
Последние цифры — действительно уникальные результаты, поскольку при лечении больных ОМЛ во второй ремиссии и тех, у кого ремиссию не удается достичь, стандартные и даже агрессивные программы химиотерапии неэффективны. Выполнение аутоло-гичной ТКМ больным в первой полной ремиссии позволяет практически 50 % из них прожить более 5 лет. В том случае если аутологичную ТКМ выполняют больным во второй ремиссии, то безрецидивная выживаемость в течение 5—6 лет составляет 35— 40 %. Из тех больных, у которых не была достигнута полная ремиссия, без рецидива более 4 лет живут лишь 10 %. ТКМ от неродственного донора уступает по долгосрочным результатам как аутологичной, так и аллогенной родственной: более 4 лет без рецидива живут 40 % больных. Аллогенная ТКМ от неродственного донора характеризуется очень высокой летальностью в первые 100 дней и в течение 1-го года.
Приведенные данные свидетельствуют о том, что трансплантация костного мозга, как аллогенного, так и аутологичного костного мозга, можно рассматривать в качестве альтернативы стандартной современной химиотерапии для больных в первой ремиссии и считать единственным подходом, который предоставляет возможность определенному проценту больных во второй ремиссии или вне ремиссии прожить более 5 лет. Однако вновь хотелось бы остановиться на вопросах селекции, поскольку речь идет лишь о той категории больных, которым вообще возможно проведение ТКМ (возраст менее 45 лет, хороший соматический статус).
Выполнение как аутологичной, так и аллогенной трансплантации костного мозга у больных в период первой полной ремиссии ОМЛ не решает основных вопросов терапии этого заболевания, так как половина больных — лица старше 60 лет, полные ремиссии достигаются лишь у 2/3 больных моложе 60 лет, часть больных умирают в период консолидации, некоторые отказываются от предложенного лечения и т. д., однако ТКМ, особенно аллогенная, — это новый способ воздействия на опухолевые клетки. Аллогенная ТКМ, индуцируя такой феномен, как трансплантат против лейкоза, является эффективным противоопухолевым воздействием. Она может служить основой для моделирования и создания новых методов биологического лечения ОМЛ, не сопряженных, как сама ТКМ, с большим числом побочных эффектов.
Таким образом, трансплантация костного мозга — это этап в терапии ОЛ. Эту процедуру необходимо выполнять в специализированных центрах, где осуществляют не менее 10 аллогенных и 10 аутологичных ТКМ в год. Это условие представляется важным, иначе летальность, обусловленная развитием осложнений вследствие самой процедуры, будет очень высока, что естественным образом отразится на общей выживаемости больных.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021