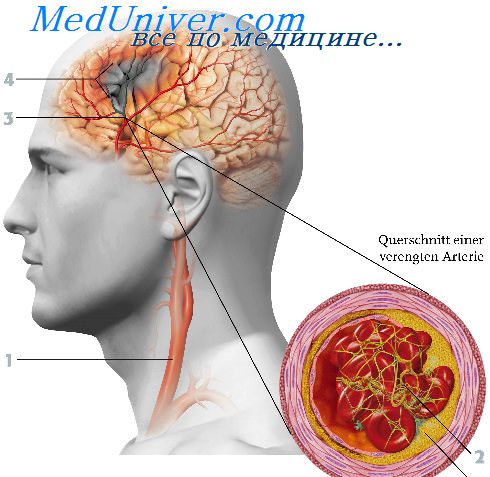
патология сосудов головного мозга у новорожденных
Патология сосудов головного мозга у новорожденных
Врожденные пороки сосудов формируются вследствие нарушения развития сосудистой системы и могут быть в виде аневризм или аномалий строения капилляров между артериальной и венозной системой.
Артериальные и артерио-венозные аневризмы — это дефект стенки сосуда в месте бифуркации артерий или вен. Нарушение строения сосудистой стенки сопровождается ее мешотчатым расширением (аневризма).
У детей раннего возраста наиболее частой аномалией является дефект развития вены Галена. Порок представляет собой прямой анастомоз между задней мозговой или верхней мозжечковой артерией и веной Галена. Аневризматическое расширение сдавливает сильвиев водопровод, III желудочек, пластинку четверохолмия. В результате артерио-венозного шунтирования и переполнения венозной системы у ребенка с рождения развивается сердечная недостаточность. Сдавление III желудочка и сильвиева водопровода приводит к формированию гидроцефалии. На первом году жизни она проявляется быстрым нарастанием окружности черепа без клинических признаков повышения внутричерепного давления. Заподозрить возможность аневризмы помогает наличие других сосудистых аномалий на лице, черепе, туловище, конечностях, а также изменения со стороны сердца. На 2—3-м году жизни ребенка основным в клинике заболевания является синдром повышения внутричерепного давления.
Дети малоактивны, плохо спят, страдают головной болью, рвотой. В области лба, висков — расширение поверхностных вен, их извитость. При больших размерах аневризмы наблюдается односторонний, реже двусторонний, различной степени выраженности «пульсирующий экзофтальм». Артерио-венозное шунтирование сопровождается шумом в голове, который нередко отмечается ребенком и может быть прослушан врачом. Шум бывает локальным или диффузным, интенсивность его изменяется синхронно с пульсом. Очаговая неврологическая симптоматика проявляется птозом, косоглазием, вялой реакцией зрачков на свет, снижением зрения. Эти симптомы возникают в результате сдавления аневризмой черепномозговых нервов, часто бывают «мерцающими». На глазном дне — выраженные застойные явления, отек соска зрительного нерва, возможны аномалии развития сосудов глазного дна.
Наличие артерио-венозного шунта подтверждается повышением парциального давления кислорода в яремной вене. Это простой и демонстративный тест для диагноза аномалии вены Галена. Диагноз уточняется с помощью пневмоэнцефалографии, которая позволяет выявить наличие масс, проецирующихся кпереди от III желудочка. Ангиография устанавливает характер и размер аневризмы.
Артерио-венозные аневризмы, локализующиеся на поверхности гемисфер, в бассейнах передней и средней мозговых артерий, у детей раннего возраста могут быть «немыми». Однако в некоторых случаях отмечаются периодические мигренозные головные боли, очаговые неврологические симптомы. Основные из них — фокальные моторные и сенсорные припадки. Они могут быть единственным симптомом в течение многих лет, не сопровождаются изменениями биоэлектрической активности мозга в межприступный период.
Артериальные аневризмы у детей раннего возраста обычно клинически не проявляются. В редких случаях отмечаются головная боль, нарушения сна. Головная боль усиливается после физического или эмоционального напряжения. В неврологическом статусе возможно изолированное преходящее одностороннее поражение черепномозговых нервов, чаще глазодвигательных. Диагноз артериальной или артерио-венозной аневризмы уточняется с помощью ангиографии.
Разрыв аневризмы наступает внезапно или может быть спровоцирован физическим напряжением, травмой. О возможности разрыва аневризмы всегда следует подумать, когда тяжелое состояние — потеря сознания, судороги — развивается у ребенка после легкой травмы головы. Разрыв артериальной и артерио-венозной аневризмы характеризуется клиникой внутричерепного кровоизлияния. Наиболее часто наблюдаются субарахноидальные кровоизлияния.
У детей раннего возраста наблюдаются и другие типы пороков развития сосудов головного мозга: телеангиэктазии, кавернозные гемангиомы. Они могут быть изолированными, но чаще являются одним из проявлений генетически детерминированпых заболеваний, таких, как энцефалотригеминальный ангиоматоз (болезнь Штурге — Вебера), цереброретинальный ангиоматоз Гиппеля-Линдау, сосудисто-костная дизэмбриоплазия и др.
Сосудистые заболевания головного мозга у детей
Инсульт принято считать заболеванием взрослых. Однако сегодня специалистам все чаще приходится сталкиваться с тем, что от инсульта страдают совсем маленькие пациенты. К каким проблемам могут привести нарушения мозгового кровообращения у детей, когда родителям стоит бить тревогу и как решить эти проблемы, расскажет наша статья.
Функционирование головного мозга требует значительных затрат энергии, источники которой он получает через сеть кровоснабжения. Во время напряженной физической и умственной работы, а также при психоэмоциональном возбуждении энергетические потребности мозга значительно возрастают.
Снабжение мозга кровью обеспечивается тремя крупными артериями: двумя внутренними сонными артериями (a. carotis interna) и основной артерией (a. basilaris). Полная остановка кровотока в головной мозг в течение 5-6 мин. приводит к необратимой гибели клеток мозга. При недостатке кровоснабжения мозга (ишемия) возникает зона инфаркта мозга с необратимыми изменениями в ней.
К нарушению мозгового кровообращения приводят различные патологические состояния мозговых сосудов, возникающие как внутри них, так и при воздействии на сосуды извне. Иногда патология сосудов имеет врожденный характер. Специалисты утверждают, что одной из основных причин острых и хронических нарушений мозгового кровообращения в детском возрасте являются врожденные патологические извитости внутренних сонных артерий, изолированные или в сочетании с другими аномалиями магистральных сосудов головы.
Нормальное кровоснабжение клеток мозга важно в любом возрасте. Но нельзя забывать о том, что ребенок практически каждый день учится чему-то новому, открывает для себя окружающий мир. А это требует от него максимальных затрат энергии, концентрации внимания и памяти. Поэтому нарушение мозгового кровообращения может иметь фатальные последствия для умственного и физического развития ребенка. Понять, что у ребенка есть какие-то проблемы мозгового кровообращения, очень сложно. Однако серьезным поводом для беспокойства родителей может быть один или несколько следующих симптомов:
1.Мигренеподобные головные боли:
2.Головокружения системного и несистемного характера.
3.Астенические состояния и когнитивные нарушения:
Из ноотропных препаратов, применяемых для лечения и профилактики сосудистых заболеваний головного мозга, можно выделить D-гопантеновую кислоту. Это ноотроп смешанного типа действия с широким спектром клинического применения. Он улучшает обменные процессы и кровообращение в головном мозгу, повышает утилизацию глюкозы. D-гопантеновая кислота оптимизирует биоэнергетические процессы в нервной клетке, способствует улучшению работы нейронов в условиях гипоксии, защищает мозг от ее повреждающих воздействий. Препарат оказывает положительное влияние на метаболические процессы и микроциркуляцию в ишемизированных тканях. D-гопантеновая кислота обладает противосудорожным действием, нейровегетотропным эффектом, проявляет нейропротективное и нейротрофическое действие. Препарат улучшает когнитивные функции (память, внимание, восприятие), повышает объем познавательной деятельности. Благодаря седативному эффекту он не вызывает нарушений сна, а мягкий стимулирующий эффект не вызывает гиперактивности. D-гопантеновая кислота обладает высоким профилем безопасности, поэтому ее препараты разрешены к использованию у детей с первых дней жизни.
Мнение специалиста:
Михаил ЛОБОВ, докт. мед. наук, проф., руководитель клиники детской неврологии МОНИКИ, главный детский невролог Минздрава Московской области
Марина БОРИСОВА, канд. мед. наук, старший научный сотрудник клиники детской неврологии МОНИКИ.
Спектр патологических состояний, приводящих к ишемическим поражениям головного мозга в детском возрасте, достаточно широк. К ним относят врожденные пороки сердца, инфекционно-аллергические васкулиты, токсические поражения сосудов головного мозга, заболевания, проявляющиеся симптоматической артериальной гипертензией, гематологические расстройства, генетические нарушения, вазомоторные дистонии, мигрень и др.
В последнее время среди причин формирования ПИ ВСА называется врожденная неполноценность соединительной ткани. В результате экспериментальных исследований предложена одна из наиболее вероятных гипотез патогенеза конфигурационных сосудистых аномалий: появление дефектов в структуре эластина и коллагена вследствие эндогенного (возможно, генетически детерминированного) усиления активности деградативных энзимов (коллагеназы и эластазы). В наших наблюдениях наследственные формы синдромальной патологии (СЭД, недифференцированная дисплазия соединительной ткани) диагностированы у 60% детей с ПИ ВСА.
ПИ ВСА, не сопровождающиеся нарушением церебральной гемодинамики, как правило, асимптомны. Нами показано, что в процессе роста ребенка возможно полное нивелирование ПИ ВСА либо «выпрямление» артерии, что сопровождается восстановлением или улучшением кровотока и регрессом неврологических нарушений.
Лечение и реабилитация перинатальных поражений нервной системы у детей первых месяцев жизни
В последние десятилетия, в связи с достижениями новейших медицинских технологий (экстракорпоральное оплодотворение, пролонгирование патологической беременности, реанимация новорожденных), особую актуальность приобрела проблема повышения качества жизни де
В последние десятилетия, в связи с достижениями новейших медицинских технологий (экстракорпоральное оплодотворение, пролонгирование патологической беременности, реанимация новорожденных), особую актуальность приобрела проблема повышения качества жизни детей с перинатальной патологией нервной системы [1, 2, 3]. Существенные нарушения: вначале постнатальной адаптации, затем снижение возможности усвоения социального опыта и, как следствие, социальная дезадаптация ребенка — возникают у большинства детей с тяжелыми поражениями нервной системы. По данным ведущих неврологов [3], эти поражения обусловливают основную часть причин детской инвалидности. Кроме того, у детей с нетяжелыми формами перинатальной патологии в последующие годы нередко отмечаются проявления минимальных церебральных дисфункций, существенно затрудняющих их обучение и образование [2]. Поэтому проблемы своевременного лечения и адекватной реабилитации детей с перинатальными поражениями привлекают пристальное внимание врачей различных специальностей: педиатров, неврологов, ортопедов, реабилитологов и др., — а также специалистов по коррекционной педагогике.
Основные методологические принципы реабилитации детей при перинатальной патологии ЦНС, разработанные за последние 10–12 лет [4], могут также лежать в основе терапии этих состояний, задачи которой как в остром периоде, так и в ходе реабилитации, вторичной профилактики отсроченных проявлений заболевания по сути одни и те же. Тем не менее некоторые неврологи понимают под реабилитацией в детском возрасте абилитацию, т. е. создание возможностей для поступательного развития ребенка и коррекцию постепенно выявляющихся отклонений в развитии [3]. С учетом этого общая методология лечения и реабилитации при перинатальном поражении мозга базируется на следующих принципах.
На каждом из этапов оказания помощи больному новорожденному и грудному ребенку существуют свои ведущие задачи. Так, на первом этапе — в родильном зале, палате интенсивной терапии и отделении реанимации новорожденных — в соответствии с приказом МЗ РФ № 372 от 1995 г. прежде всего решаются задачи компенсации системных нарушений жизненно важных функций — дыхания, кровообращения, выделительной функции почек, энергетического баланса и общего метаболизма.
Медикаментозно-инструментальная терапия предполагает на этом этапе в первую очередь коррекцию кислотно-основного состояния, гипер- или гипогликемии, гиповолемии, артериальной гипотензии или гипертензии, сердечного выброса. По показаниям, с учетом данных мониторирования и лабораторных анализов, применяются осмотические и петлевые диуретики, антигеморрагические, противосудорожные средства (препарат первого выбора — фенобарбитал в стандартной дозе до 20 мг/кг массы тела в сутки). Применение на этом этапе антиоксидантов и ноотрофов (церебропротекторов — пирацетам, эссенциале, ГОМК) не всегда обосновано. Особая осторожность необходима при назначении вазоактивных препаратов: так, некоторые специалисты рекомендуют с 4-го дня жизни инстенон [3], тогда как другие говорят о возможных побочных действиях сосудистых средств [5]. Адекватное лечение в раннем неонатальном периоде (при создании максимально щадящих условий для ребенка и температурного комфорта) способствует адаптационным процессам саногенетической направленности и является основой последующей реабилитации.
Новорожденные не только с тяжелыми, но и со среднетяжелыми проявлениями перинатальной патологии ЦНС переводятся, как правило, в отделение «второго этапа» (отделение патологии новорожденных, отделение для недоношенных детей). Задачи этого этапа — дальнейшая оптимизация адаптационных процессов, лечение сопутствующих (как правило, инфекционно-воспалительных) заболеваний и начало собственно реабилитации, т. е. коррекции неврологических нарушений. Третий этап реабилитации — это специализированные стационары (отделение неврологии раннего возраста, центр реабилитации маловесных и недоношенных детей, центр коррекции), амбулаторные отделения реабилитации детских поликлиник (стационар-замещающие технологии). На всех этапах реабилитации перинатально пострадавших детей необходимо активное участие семьи больного ребенка; по показаниям, в конце первого — начале второго года жизни возможно привлечение специализированных детских дошкольных учреждений (группы коррекции в яслях и детских садах, центры коррекции). На втором и третьем этапах реабилитации используются практически одинаковые средства и методы, хотя выбор их зависит от индивидуального патокинеза болезни и эффективности коррекции на предыдущем этапе.
В практике большинства врачей фармакотерапия при перинатальных поражениях мозга занимает ведущее место, что далеко не всегда оправдано. В последнее десятилетие в условиях «фармацевтического бума» ежегодно появляются новые препараты, которые из области взрослой неврологии часто без достаточной проверки с позиций доказательной медицины попадают в арсенал средств, используемых неонатологом [5, 6, 7]. Назначая новорожденному лекарство, врач должен учитывать его возможные как ближайшие, так и отдаленные побочные эффекты (в том числе риск сенсибилизации), выбирать наименее травматичные пути введения лекарств: при необходимости проведения инъекций предусматривать обезболивание местными анестетиками типа пластыря ЕМLA или метаболитами [4, 6]. Во избежание ятрогений необходимо учитывать возможный синергизм или антагонизм фармакопрепаратов (не назначать более 3–4 лекарств одновременно), строго индивидуально выбирать дозировки (принцип минимизации, контроль индивидуальной фармакокинетики). Особая осторожность нужна при выборе алгоритма лечения глубоко недоношенных детей с экстремально низкой массой тела. Один из путей профилактики ятрогений в неонатологии — это использование гомеопатических препаратов [8], поскольку они содержат микродозы мягкодействующих растительных и минеральных веществ. Механизм действия этих препаратов не вполне ясен (возможны объяснения с позиций теории доминанты Ухтомского или теории биологического резонанса), тем не менее химическая эффективность некоторых из гомеопатических препаратов в неонатологии вполне доказана [4].
Фармакопрепараты, используемые в реабилитации как доношенных, так и недоношенных новорожденных, условно могут быть разделены на применяющиеся посиндромно (симптоматические) и средства преимущественно патогенетической коррекции, хотя некоторые препараты обладают и тем и другим воздействием. Рассмотрим их подробнее.
Медикаментозная реабилитация детей с перинатальными поражениями ЦНС — поздний неонатальный период, начало восстановительного периода
Преимущественно посиндромные (симптоматические) средства: противосудорожные: фенобарбитал, ГОМК, дроперидол, реланиум, вальпроаты — при некупируемых другими средствами судорогах и тщательном мониторинге функций печени и кроветворения; дегидратационные: диакарб (со 2–3-й недель жизни, у глубоконедоношенных — позднее), триампур, верошпирон, гомеопатические препараты (гелиборус, апис, магнезия фосфорика), сборы трав — отвары и настои; седативные (сульфат магния, сборы трав — отвары и настои, лечебные ванны, реланиум, радедорм, гомеопатические препараты — валерианахель, нервохель, вибуркол), эфирные масла, ароматерапия (анис, ромашка, лаванда); спазмолитики и прокинетики (при вегетативных нарушениях): но-шпа, церукал, риабал, мотилиум, гомеопатические препараты (нуксвомика, гомакорд, вибуркол, хапель).
Средства патогенетической направленности: нейропротекторы (ноотропы, ноотрофы, ингибиторы нейрального апоптоза) — пирацетам (ИСВ), кортексин, семакс, минисем, церебролизин, пантогам, глиатилин, глицин, аминокислотные композиты, стволовые клетки; вазоактивные препараты (нормализаторы общей и мозговой гемодинамики) назначаются при отсутствии угрозы кровотечений под контролем допплерографии: кавинтон, циннаризин, сермион, димефосфон, кверцетин, гомеопатические препараты (эскулюс композитум, траумель); модуляторы синаптической проводимости: мидокалм, дибазол; aнтиоксиданты и антигипоксанты: танакан, мексидол, токоферол, соевое масло, кудесан, димефосфон, биолан, актовегин; метаболиты и поливитаминные комплексы: глицин, биотредин, лимонтар, эссенциале, элькар, кудесан, корилип, кверцетин, бета-каротин, киндер биовиталь, поливит беби, церебрум композитум, мульти-табс, капли Береш Плюс.
Как следует из вышеизложенного, выбор препаратов ограничен и нужна поистине «снайперская» точность при их назначении, кроме того, необходим клинический и лабораторный неинвазивный контроль эффективности. Следует обратить внимание на возможность относительно нетравматичного введения препаратов — накожное (соевое масло), ингаляционные (эфирные масла при ароматерапии), ректальные суппозитории (многие гомеопатические средства). В неонатологии важно использование наиболее «чистых» препаратов, например целесообразен выбор из препаратов пирацетама лекарств, выпускаемых фирмой ИСВ (Бельгия, Швейцария). В перечне средств патогенетической направленности к ингибирующим нейральный апоптоз условно отнесены стволовые клетки (в строгом смысле это не фармакопрепарат), степень терапевтической эффективности которых еще нуждается в дальнейших исследованиях. В то же время от использования фетальных трансплантатов [3] следует решительно отказаться по соображениям общечеловеческой и медицинской этики.
Обеспечить минимизацию лекарственной терапии помогает раннее (начиная с первого этапа) включение в программу комплексной реабилитации немедикаментозных воздействий. На втором и третьем этапах реабилитации детей с перинатальной патологией эти методики должны быть признаны приоритетными [1]. Несомненно, в обеспечении успешной реабилитации важная роль принадлежит адекватному вскармливанию и оптимальной организации окружающей среды (лечебно-охранительный режим), но в настоящей статье эти вопросы не рассматриваются. Тем не менее некоторые аспекты организации выхаживания тяжелобольных детей (ограничение сенсорной нагрузки в остром периоде поражения мозга, температурный комфорт, ограничение электромагнитных воздействий, выхаживание на колышащихся матрасиках или на шерсти ягнят) могут быть отнесены к методам немедикаментозной реабилитации [1, 5, 6].
Перечислим средства немедикаментозного лечения и реабилитации, весьма условно разделив их на физические и психолого-педагогические, поскольку любое физическое воздействие на маленького ребенка предполагает обязательный психоэмоциональный контакт с ним.
Немедикаментозная реабилитация детей первого года жизни с перинатальными поражениями ЦНС
Физическая реабилитация: разнообразный лечебный массаж, лечебная гимнастика, лечение «положением» (укладки, туторы, «воротники» и т. д.), терапия по Войту; упражнения в воде и гидромассаж; сухая иммерсия (имитация невесомости); использование кроватки «Сатурн» (эффект невесомости + вибромассаж); физиотерапия (переменное магнитное поле, синусоидальные модулированные токи, электрофорез, парафинотерапия, лазеротерапия, свето- и цветотерапия).
Психолого-педагогическая коррекция и психоэстетотерапия: коррекционная (кондуктивная) педагогика; психотерапевтическая коррекция в диаде «мать–дитя» (контакт «кожа-к-коже», «кенгуру») и в целом в семье больного ребенка; музыкотерапия, эстетотерапия; тактильно-кинестетическая стимуляция.
Большинство из вышеперечисленных методик не являются новыми. В последние 3–5 лет к новым разработкам следует отнести методику мягкого вибромассажа в условиях невесомости (отечественная кроватка «Сатурн», ООО «Ритм», г. Екатеринбург), светотерапию и цветотерапию с помощью лампы линейного поляризованного видимого света «Биоптрон» («Цептер», Швейцария), тактильно-кинестетическую стимуляцию ладоней и пальцев, применяемую у детей с низкой и экстремально низкой массой тела [4]. В последние годы для недоношенных детей особенно рекомендуется сочетание двух-трех «мягких» методов физического воздействия с психоэмоциональной и психосенсорной коррекцией, что помогает моделировать эффект так называемых «сенсорных комнат», применяемых в реабилитации более старших пациентов [9].
Методика музыкотерапии для доношенных и недоношенных новорожденных детей, разработанная в клинике НЦЗД РАМН, включает как подбираемые индивидуально программы, записанные на магнитофон, так и пение кормящих матерей [4]. Матери обучаются комплексной мягкой психосенсорной стимуляции ребенка, напевают колыбельные и другие рекомендованные песни, учатся проведению мелоритмического воздействия (движение и тактильная стимуляция в сочетании с пением и чтением стихов) — элементам эвритмической терапии по Р. Штайнеру, который доказал благотворное влияние на организм ребенка ритмических движений под музыку [10].
В последние годы установлено, что начинать общение с ребенком необходимо еще в период внутриутробного онтогенеза; сегодня активно развивается перинатальная психология и перинатальная педагогика. Для детей с перинатальной патологией ЦНС раннее начало педагогической коррекции (элементы кондуктивной педагогики) является важнейшей составной частью реабилитации, поскольку мягкие сенсорные и эмоциональные воздействия — это немедикаментозные «ноотрофы» для развивающегося мозга [1, 4, 5, 6]. Ежедневное влияние родителей (прежде всего матери) направляется специалистом — психологом (педагогом), который формирует у родителей активную позицию по преодолению психоневрологических дефектов, обучает их разнообразным формам, приемам и средствам взаимодействия с ребенком и умению оценивать его реакции.
Целью ранней педагогической коррекционной работы является создание условий для поступательного психосоциального развития ребенка, для использования его индивидуального «потенциала компенсаций». На каждом возрастном этапе педагог решает определенные развивающие задачи: вначале это стимуляция интереса ребенка к окружающей среде, формирование исследовательского поведения, затем укрепление межанализаторных связей, расширение спектра сенсомоторных навыков и умений, повышение коммутативной активности, развитие и обогащение игровых и предметных действий, а также социальной активности ребенка [11].
В настоящей статье не затрагиваются некоторые специальные аспекты реабилитации (коррекция зрительных нарушений при ретинопатии недоношенных, нейросенсорной тугоухости, ортопедической патологии).
Использование широкого спектра немедикаментозных воздействий на втором и третьем этапах реабилитации больных детей позволяет (по данным клиники НЦЗД РАМН) уменьшить дозировки и длительность курсов фармакотерапии (по вазоактивным препаратам — на 15–20% и 3–3,5 дня; по мочегонным (диакарб) — на 20–30% и 2–3 дня; по седативным препаратам — на 30–40% и 4–5 дней). Эффективность комплексной реабилитации оценивалась в клинике по достижении детьми 1,5–2 лет. Функциональная компенсация неврологических и нейросенсорных нарушений имела место почти у всех детей со среднетяжелыми и легкими формами перинатальных поражений мозга и у 80% детей с тяжелыми (по оценке в периоде новорожденности) нарушениями. Кроме того, даже у детей, имевших в конце периода наблюдения инвалидность вследствие сенсорного или моторного дефекта, удавалось добиться некоторого смягчения моторных или сенсорных расстройств и соответственно несколько улучшить качество жизни.
Е. П. Бомбардирова, доктор медицинских наук, профессор
Г. В. Яцык, доктор медицинских наук, профессор
А. А. Степанов, кандидат медицинских наук
НЦЗД РАМН, Москва
По вопросам литературы обращайтесь в редакцию.