Гладкие мышцы иннервируются чем
Гладкие мышцы иннервируются чем
а) Нервно-мышечные веретена. Разные мышцы содержат от десятков до нескольких сотен мышечных веретен, длина которых не превышает 1 см. Большое количество мышечных веретен расположено в (а) «антигравитационных» (постуральных) мышцах позвоночника, бедра и голени, а также (б) мышцах шеи и (в) внутренних мышцах руки. Все перечисленные мышцы содержат множество медленных оксидативных волокон. Мышечные веретена представлены в небольшом количестве в мышцах, состоящих преимущественно из быстрых гликолитических и промежуточных волокон.
Мышечные веретена состоят из интрафузальных мышечных волокон, количество которых не превышает 12. (В данном контексте экстрафузалъные мышечные волокна считают обычными). Крупные интрафузальные волокна начинаются от полюсов (концов) мышечных веретен и фиксируются к соединительной ткани — перимизию. Некрупные интрафузальные волокна фиксируются к коллагеновой капсуле веретена. В средней части (экваторе) веретена саркомеры практически полностью замещены ядрами, расположенными в форме сумки—сумчато-ядерные мышечные волокна (характерно для широких волокон) или цепочки — цепочечно-ядерные мышечные волокна (характерно для тонких волокон).
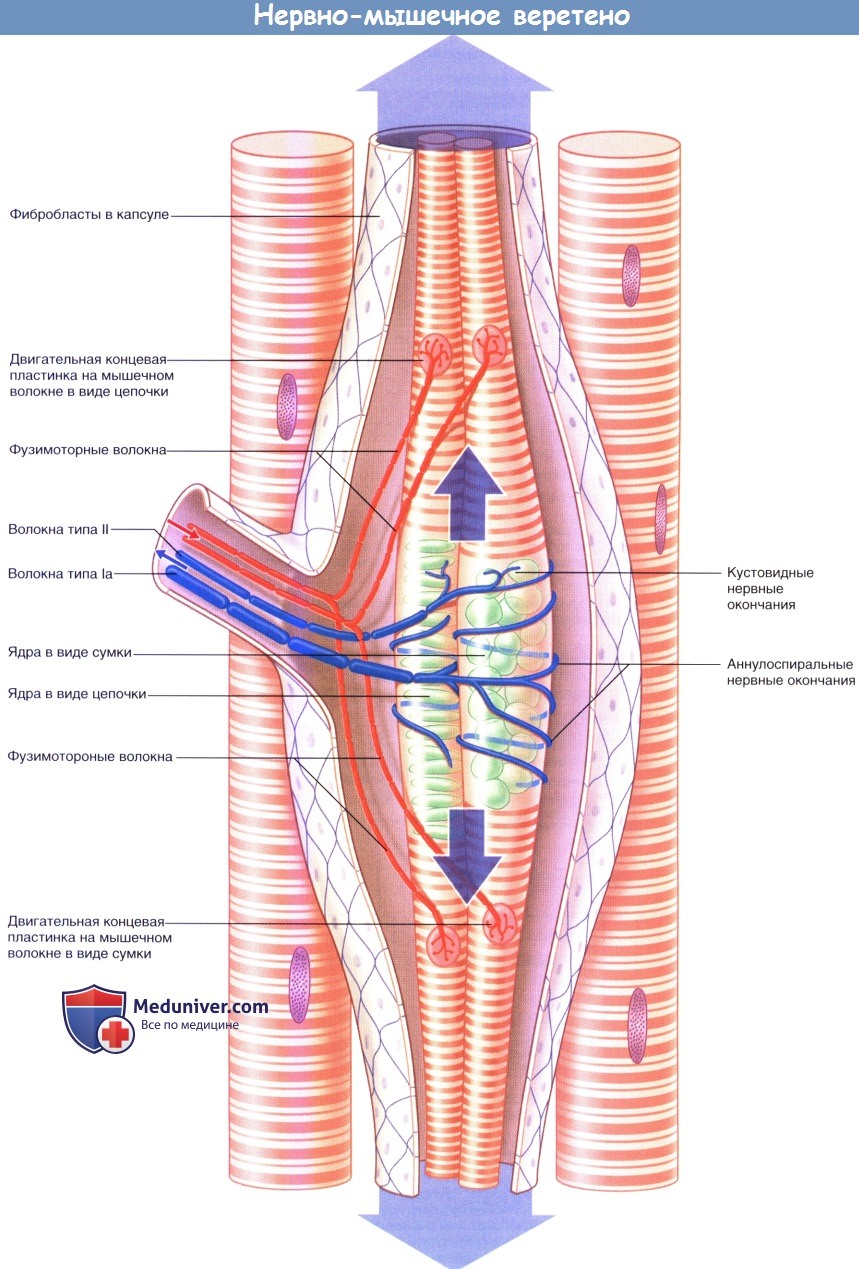
Стрелками среднего размера обозначено активное растяжение аннулоспиральных нервных окончаний фузимоторными нервными волокнами.
Активное растяжение в достаточной степени компенсирует эффект разгрузки одновременного сокращения экстрафузальных мышечных волокон.
Стрелками маленького размера показаны направления проведения импульсов к мышечному веретену и от него при сокращении мышцы.
1. Иннервация. Иннервацию мышечных веретен осуществляют двигательные и чувствительные нервные волокна. Двигательные нервные волокна — фузимоторные—в соответствии с толщиной относят к типу Аγ, а нервные волокна экстрафузальных мышц — к типу Аα. Фузимоторные аксоны разветвляются и иннервируют поперечно-исчерченные сегменты концевых участков интрафузальных мышц. Единичные первичные чувствительные нервные волокна типа 1а оборачиваются спирально-кольцевым образом вокруг сумчато-ядерных или цепочечно-ядерных мышечных волокон. Вторичные кустовидные чувствительные нервные окончания образованы нервными волокнами II типа и располагаются с одной или с двух сторон от первичного волокна.
2. Активация. Мышечные веретена представляют собой рецепторы растяжения. При растяжении мышечного веретена ионные каналы поверхностной мембраны чувствительных нервных окончаний открываются, за счет чего создаются положительные электроволны. В результате их суммирования в области терминального участка аксона чувствительного нервного волокна происходит образование рецепторного потенциала, который при достижении пороговых значений генерирует нервные импульсы.
Растяжение мышечных веретен может происходить пассивным и активным путями.
3. Пассивное растяжение. Пассивное растяжение мышечного веретена происходит при пассивном удлинении всего мышечного брюшка. Например, при воспроизведении сухожильных рефлексов, в частности коленного, во время удара по сухожилию происходит пассивное растяжение мышечных веретен брюшка четырехглавой мышцы бедра. Волокна типов Iа и II направляются к спинному мозгу и образуют синапсы с дендритами α-мотонейронов. (Принадлежность мотонейронов к типу а определяется Аα-диаметром их аксонов.)
По механизму положительной обратной связи происходит резкое сокращение экстрафузальных волокон четырехглавой мышцы бедра, что приводит к пассивному укорочению мышечного веретена, поскольку оно лежит параллельно экстрафузальным волокнам. Вследствие того, что мышечные веретена лежат параллельно экстрафузальным мышцам, их сокращение происходит пассивно. Этот процесс условно описывают как «разгрузка мышечного веретена».
Сухожильные рефлексы относят к моносинаптическим. Для них характерен латентный период (промежуток времени до ответной реакции на стимул), составляющий 15-25 мс.
Помимо возбуждающего действия на гомонимные мотонейроны (т. е. двигательные нейроны, иннервирующие одни и те же мышцы), афферентные волокна мышечных веретен опосредованно через вставочные тормозные мотонейроны оказывают тормозное действие на а-мотонейроны мышц-антагонистов. Этот процесс получил название реципрокного торможения. Задействованные тормозные нейроны называют вставочными нейронами типа Iа.
4. Кодирование информации. Первичные афференты мышечных веретен проявляют наибольшую активность во время растяжения. Они определяют скорость растяжения мышцы: чем быстрее происходит растяжение, тем больше импульсов они генерируют.
Вторичные афференты мышечных веретен по сравнению с первичными активнее задействованы в процессе поддержания определенной позиции и определяют степень растяжения мышцы: чем выше степень статического растяжения, тем больше формируется импульсов.
5. Активное растяжение. Активное растяжение осуществляют фузимоторные нейроны, вызывающие сокращение поперечно-исчерченных сегментов интрафузальных мышечных волокон. Интрафузальные волокна фиксированы к соединительной ткани и растягивают среднюю часть (экватор) по направлению к полюсам. Это явление получило название «эффект новогодней хлопушки».
В процессе произвольных движений за счет кортикоспинального (пирамидного) проводящего пути происходит одновременная активация Аα- и Аγ-мотонейронов. Таким образом, под действием сокращения экстрафузальных мышц не происходит «разгрузка мышечных веретен». Афференты мышечных веретен, расположенные по обеим сторонам соответствующих суставов, направляют в мозг сигналы обо всех происходящих в данный момент времени сокращениях и расслаблениях мышц.
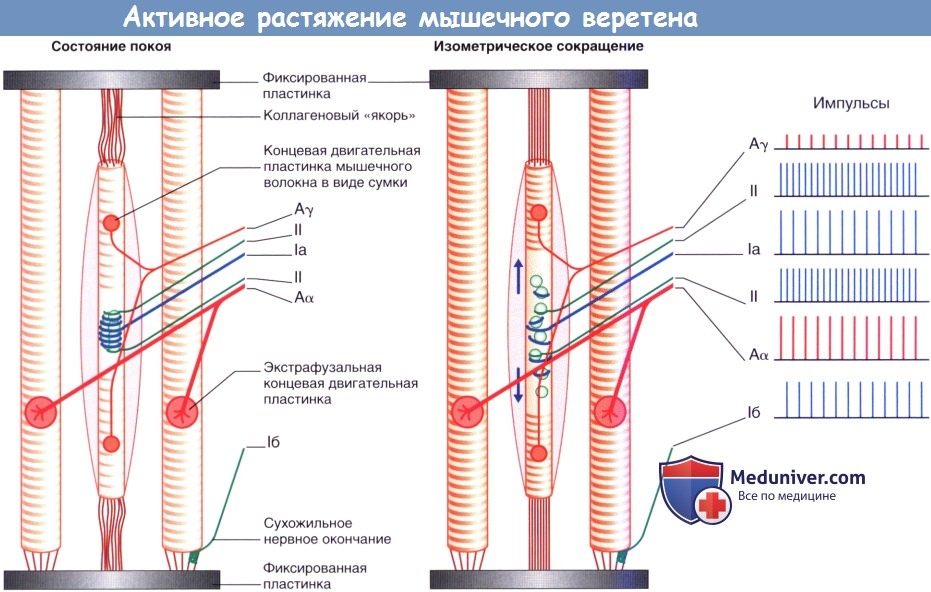
Термин «изометрический» обозначает «имеющий постоянную длину». Экстрафузальные мышечные волокна находятся в изометрическом состоянии, если они растянуты и их концы зафиксированы.
Мышечное веретено также сохраняет постоянную длину за счет того, что оно опосредованно через соединительную ткань прикрепляется к пластинке.
Однако поперечно-исчерченные компоненты интрафузальных волокон не поддерживаются в изометрическом состоянии: они укорачиваются, поскольку их центральная часть эластична и подвержена внешнему воздействию.
Первичные и вторичные афференты мышечного веретена, подходящие к его центральной части, обеспечивают «активное» растяжение за счет фузимоторной активности, осуществляемой путем направления афферентных импульсов в ЦНС и последующего усиления экстрафузальных сокращений с задействованием механизма гамма-петли.
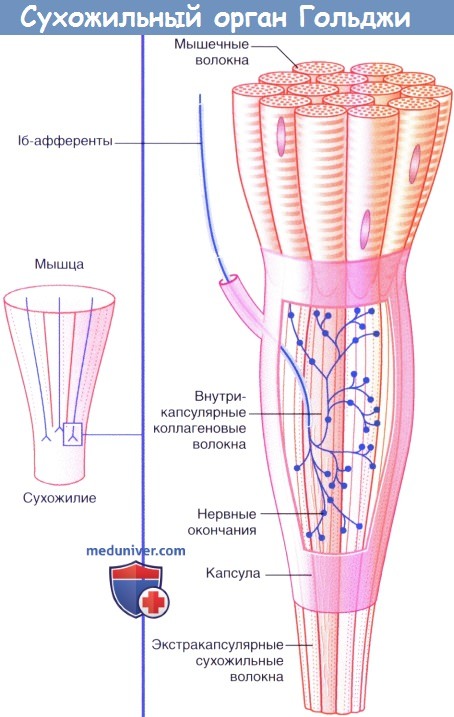
б) Нервные окончания сухожилий. Сухожильные органы Гольджи располагаются в местах соединения сухожилий с мышцами. Единичное нервное волокно типа Ib распадается на сложноорганизованные мельчайшие разветвления, оплетающие пучки сухожильных волокон, связанные с соединительно-тканной капсулой.
Десятки мышечных волокон погружаются в сухожильные интракапсулярные волокна, которые последовательно связываются с другими мышечными волокнами в пределах определенной мышцы. Под действием натяжения, возникающего в процессе сокращения мышцы, происходит активация луковицеобразных нервных окончаний. В связи с тем, что скорость возникновения импульсов в исходном нервном волокне зависит от силы натяжения, сухожильные нервные окончания определяют силу сокращения мышцы.
Афференты типа Iб передают сигнал на гомонимные мотонейроны по механизму отрицательной обратной связи, в отличие от афферентов мышечных веретен, передающих информацию посредством положительной обратной связи. Это явление получило название «аутогенное торможение»; рефлекторная дуга в данном случае — двухсинаптическая, поскольку в ее образовании принимает участие вставочный тормозной нейрон. При необходимости этот процесс сопровождает реципрокное возбуждение мотонейронов, иннервирующих мышцы-антагонисты.
Важная функция сухожильного органа Гольджи — ограничение и «сглаживание» колебательных движений, характерных для совершающих движение сегментов конечности. Такое ограничение известно с точки зрения физиологии как «скованность в суставах». Парадоксально излишняя активность афферентов типа Iб, типичная для болезни Паркинсона, усиливает колебательные движения, что проявляется характерным тремором покоя, который наиболее выражен в области предплечья (движения пронации и супинации) и пальцев (большой палец совершает движения, напоминающие пересчитывание монет или катание пилюль).
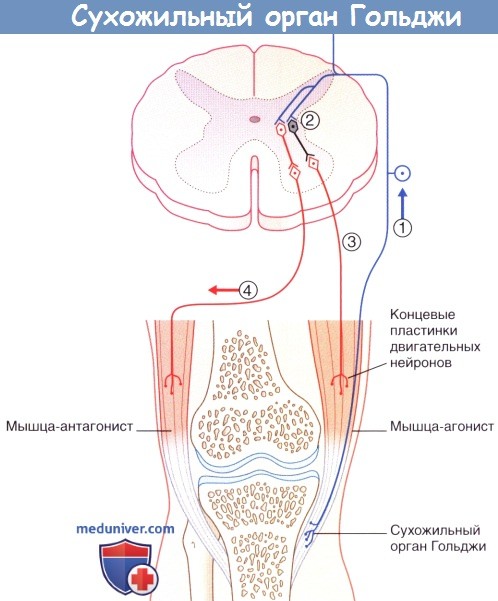
(1) Сокращение мышцы-агониста вызывает возбуждение афферентов сухожильного органа Гольджи,
что приводит к (2) возбуждению тормозных вставочных нейронов, образующих синапсы с гомонимными мотонейронами,
а также (3) возбуждению тормозных вставочных нейронов, образующих синапсы с (4) мотонейронами мышцы-антагониста.
в) Свободные нервные окончания. В мышцах имеется множество свободных нервных окончаний, большинство которых расположено во внутримышечной соединительной ткани и покрывающих мышцы фасциях. Эти нервные окончания отвечают за болевую чувствительность, возникающую при непосредственном повреждающем воздействии или при накоплении продуктов распада, к которым относят молочную кислоту.
г) Иннервация суставов. Немиелинизированные нервные волокна со свободными нервными окончаниями в большом количестве присутствуют в связках и капсулах суставов, а также во внешних частях внутрисуставных менисков. Эти нервные волокна обеспечивают болевую чувствительность при деформациях суставов, а также участвуют в формировании защитного рефлекса для капсулы сустава. Так, например, переднюю капсулу запястья иннервируют срединный и локтевой нервы; внезапное растяжение при насильственном разгибании вызывает рефлекторную активацию двигательных волокон, что приводит к сгибанию верхней конечности в лучезапястном суставе.
В экспериментах на животных показано, что при воспалении сустава в возбужденном состоянии находится большее количество нервных волокон, чем при растяжении капсулы здорового сустава. Вероятно, существуют нервные окончания, единственным стимулом которых служит воспалительный процесс.
Инкапсулированные нервные окончания, расположенные внутри суставных капсул и вокруг них, представлены тельцами Руффини, реагирующими на натяжение, ламеллярными окончаниями, воспринимающими давление, а также тельцами Пачини, ответственными за ощущение вибрации.
д) Миофасциальный болевой синдром. Миофасциальный болевой синдром—распространенное заболевание, проявляющееся региональной мышечной болезненностью, связанной с чрезмерной чувствительностью пучков напряженных мышечных волокон. (Сходные синдромы наблюдают при другом заболевании—фибромиалгии. Однако при фибромиалгии происходит центральное нарушение болевой чувствительности—дисфункция системы модуляции боли.)
Прикосновение к пучкам мышечных волокон с повышенной чувствительностью вызывает боль; клинически эту область называют миофасциальной триггерной точкой. Для боли не характерно распространение в области дерматома какого-то определенного нерва; в некоторых случаях боль может выходить за пределы триггерной точки—иррадиировать. Кроме того, боль могут сопровождать вегетативные проявления, такие как покраснение и пилоэрекция. Возникновение триггерных точек может быть связано с травмой мышц, чрезмерными нагрузками во время профессиональной деятельности или спортивных занятий при нарушении процесса нормального восстановления.
Спонтанно активирующиеся очаги получили название активных миофасциальных триггерных точек (МТТ), а находящиеся в данный момент времени в неактивном состоянии—латентных миофасциальных триггерных точек. Происходящие процессы недостаточно ясны с точки зрения патофизиологии, однако установлено, что тканевая жидкость, окружающая активные МТТ, содержит большее количество ассоциированных с воспалением веществ (например, брадикинины, простагландины, протоны Н + ).
Со временем боль может захватывать новые области или усиливаться в результате раздражения нейронов задних рогов. Высвобождение другими ветвями раздраженных нейронов субстанции Р может привести к возникновению новых МТТ в области той же или прилежащей мышцы.
Стойкое сокращение мышечных волокон, прилежащих к узелковым утолщениям, объясняют инактивацией ацетилхолинэстеразы в базальной мембране их концевых двигательных пластинок. Принципы лечения этого заболевания—длительное пассивное растяжение пораженных мышц, длительное давление в горизонтальном положении больного (например, путем подкладывания теннисного мячика под пораженную область), а также механическое повреждение прокалыванием иглой или введением местных анестетиков и/или стероидов.
е) Резюме. Мышцы. Двигательная единица состоит из двигательного нейрона и иннервируемой им группы мышечных волокон. Каждая двигательная единица содержит определенный гистохимический вид мышечных волокон. Концевое утолщение нервно-мышечного синапса, содержащее пузырьки с АХ, отделено от синаптических складок сарколеммы базальной мембраной, в которой присутствует ацетилхолинэстераза.
В состав мышечных веретен входят интрафузальные мышечные волокна, активация которых происходит с обоих концов за счет γ-фузимоторных нейронов. Чувствительные волокна типа Iа образуют первичные аннулоспиральные нервные окончания в области средней части (экватора), а волокна типа II — вторичные нервные окончания. Оба типа волокон являются рецепторами растяжения. Растяжение может происходить пассивным (например, при сухожильном рефлексе) или активным путем во время фузимоторной активности. Гомонимные мотонейроны—моносинаптические; мышцы-антагонисты реципрокно ингибируются посредством вставочных нейронов Iа. Первичные афференты мышечных веретен определяют скорость мышечного сокращения, а вторичные — степень.
В процессе произвольных движений происходит одновременная активация А α- и Аγ-мотонейронов.
Сухожильные органы Гольджи определяют силу мышечных сокращений. В состав сухожильных органов входит инкапсулированное сухожилие, иннервацию которого осуществляют афференты типа Iб, вызывающие двухсинаптическое торможение гомонимных мотонейронов и реципрокное возбуждение мышц-анта-гонистов.
Свободные внутримышечные нервные окончания обеспечивают болевую чувствительность.
Суставы. Свободные нервные окончания в большом количестве присутствуют в связках и капсулах суставов, а также во внешних частях внутрисуставных менисков. Они обеспечивают болевую чувствительность и формирование суставного защитного рефлекса. Инкапсулированные нервные окончания принимают импульсы от движений суставов.
— Вернуться в оглавление раздела «Неврология.»
Редактор: Искандер Милевски. Дата публикации: 12.11.2018
Гладкие мышцы иннервируются чем
Волокна скелетной мышцы стимулируются исключительно нервными сигналами, но сокращения гладкой мышцы могут вызываться множеством типов сигналов: нервными, гормональными, растяжением мышцы и некоторыми другими. Основная причина различий состоит в том, что гладкомышечная мембрана содержит много типов рецепторных белков, способных запустить сократительный процесс. Кроме того, есть и другие рецепторные белки, тормозящие сокращение гладкой мышцы, что также отличает ее от скелетной мышцы. Обсудим сначала нервную регуляцию гладкомышечного сокращения, а затем гормональный контроль и другие способы управления.
Физиологическая анатомия нервно-мышечных соединений гладких мышц. Сложно организованные нервно-мышечные соединения, обнаруживаемые на волокнах скелетных мышц, в гладких мышцах не встречаются. Вместо этого вегетативные нервные волокна, иннервирующие гладкие мышцы, обычно диффузно разветвляются на наружной поверхности пласта мышечных волокон. В большинстве случаев эти волокна не входят в непосредственный контакт с клеточными мембранами гладкомышечных волокон, а формируют так называемые диффузные соединения, которые секретируют медиаторы в матрикс, покрывающий гладкую мышцу, часто на расстоянии от нескольких нанометров до нескольких микрометров от мышечных клеток; затем медиатор диффундирует к клеткам.
Более того, при наличии многих слоев мышечных клеток нервные волокна часто иннервируют только наружный слой, и возбуждение распространяется от этого наружного слоя к внутренним слоям путем проведения потенциалов действия по мышечной массе или путем дополнительной диффузии медиатора.
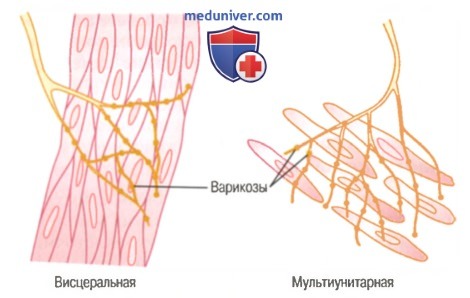
Аксоны, иннервирующие гладкомышечные волокна, не имеют типичных ветвящихся окончаний, характерных для двигательной концевой пластинки волокон скелетной мышцы. Вместо этого большинство тонких концевых частей аксонов имеют множество варикозных расширений (варикозов), распределенных вдоль их осей. В этих местах связь между шванновскими клетками, окутывающими аксоны, прерывается, и медиатор может секретироваться через стенки варикозов. В варикозах находятся везикулы, которые подобно везикулам в концевой пластинке скелетных мышц содержат медиатор. Но в противоположность везикулам в соединениях скелетных мышц, которые всегда содержат ацетилхолин, везикулы окончаний вегетативных нервных волокон содержат ацетилхолин в одних волокнах и норадреналин — в других, а иногда и другие вещества.
В некоторых случаях, особенно в гладких мышцах мультиунитарного типа, варикозы отдалены от мембраны мышечных клеток на 20-30 нм, что равно ширине синаптической щели в соединении скелетной мышцы. Такие соединения называют контактными, и они функционируют во многом так же, как нервно-мышечные соединения скелетных мышц. Скорость сокращения этих гладкомышечных волокон значительно больше, чем у волокон, стимулируемых диффузными соединениями.
Возбуждающие и тормозящие медиаторы, секретируемые в нервно-мышечных соединениях гладких мышц. Самыми важными медиаторами, которые секретируются вегетативными нервами, иннервирующими гладкие мышцы, являются ацетилхолин и норадреналин, однако они никогда не выделяются одними и теми же нервными волокнами. Ацетилхолин для гладких мышц одних органов является возбуждающим медиатором, а на гладкие мышцы других органов действует как тормозящий агент. Если ацетилхолин возбуждает мышечное волокно, норадреналин обычно тормозит его. И наоборот, если ацетилхолин тормозит волокно, норадреналин, как правило, его возбуждает.
Но почему возникают такие разные реакции? Ответ заключается в том, что ацетилхолин и норадреналин возбуждают или тормозят гладкую мышцу, связываясь сначала с рецепторным белком на поверхности мембраны мышечной клетки. Некоторые из этих рецепторных белков являются возбуждающими рецепторами, тогда как другие — тормозящими рецепторами. Следовательно, тип рецептора определяет, как будет реагировать гладкая мышца — торможением или возбуждением, а также какой из двух медиаторов (ацетилхолин или норадреналин) будет проявлять возбуждающее или тормозящее действие.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Гладкие мышцы иннервируются чем
Частыми причинами травм скелетных мышц являются дорожно-транспортные происшествия, травмы, полученные при взрывах, боевые ранения, хирургические и ортопедические манипуляции (например, после синдрома длительного сдавливания или резекции опухоли) или повреждения, случившиеся в ходе занятий спортом, приводящие к острой потере мышечной ткани. Повреждения, превышающие 20% мышечной массы, нуждаются в реконструктивных хирургических вмешательствах. Прогрессирующая мышечная потеря может быть следствием метаболических нарушений или наследственных генетических заболеваний, таких как мышечная дистрофия Дюшена, латеральный амиотрофический склероз и детская болезнь Шарко-Мари-Тута [10]. Атрофия мышц также может быть следствием травм периферических нервов, хронической болезни почек, сахарного диабета и сердечной недостаточности [3]. Потеря мышечной массы до 20% может быть компенсирована высокой адаптивностью и регенеративным потенциалом скелетных мышц. За этим порогом функциональные нарушения неизбежны и могут привести как к тяжелой инвалидности, так и к косметическим деформациям, поэтому терапевтическое вмешательство крайне востребовано для таких пациентов.
Анализ и обсуждение. Мышечная регенерация зависит от гетерогенной популяции сателлитных клеток, интерстициальных клеток и кровеносных сосудов и в основном контролируется с помощью белков межклеточного матрикса и секретируемых факторов [4]. В норме мышечная масса поддерживается балансом между синтезом и катаболизмом белка. В большинстве случаев VML тормозит регенерационную способность скелетных мышц, поскольку физически удаляются необходимые регенеративные элементы, в основном сателлитные клетки, периваскулярные стволовые клетки и базальная мембрана. Через денервацию активируются сигнальные пути распада белков (протеасомальные и аутофагиально-лизосомальные пути). Поэтому скорость разложения белка превышает его синтез, что способствует атрофии мышц, сопровождающейся постепенным снижением мышечной массы и диаметров мышечных волокон. Реваскуляризация обычно нарушается. Вследствие наступают ишемические условия способствующие пролиферации фибробластов, фиброзу и формированию фиброзной рубцовой ткани, что приводит к дальнейшей дистрофии мышцы. Состав и степень белков межклеточного матрикса в рубцовых тканях влияют на многие аспекты миогенеза, функции мышц и реиннервации. При хронической потере мышечной массы, такой как мышечная дистрофия Дюшена, фиброз является серьезной проблемой. Вследствие того, что последовательное разрушение миофибрилл не может быть полностью компенсировано пролиферацией сателлитных клеток, следующие воспалительные процессы приводят к изменению продукции белков внеклеточного матрикса и последующему развитию фиброза, а также формированию рубцовой ткани. Рубцовое образование можно уменьшить либо путем введения, например, 5-фторурацила и блеомицина, которые противодействуют пролиферации фибробластов и неоангиогенезу, либо с помощью лазерной терапии и функциональными улучшениями через 6-12 месяцев лечения [1]. Регенерация с регрессией рубцовой ткани и функциональным восстановлением может быть также оптимизирована с помощью трансплантации жира. Тем не менее, уменьшение фиброзирования недостаточно для восстановления и регенерации мышечного волокна. Клинические и научные исследования способствуют восстановлению большой мышечной потери. Современный стандарт лечения VML, как правило, основан на хирургическом вмешательстве с аутологичным мышечным трансплантатом и физиотерапией. Другими способами, которые применяют в клинике, являются: иглоукалывание и применение скаффолдов.
Хирургическое лечение VML включает в себя в основном санацию рубцовой ткани и / или транспозицию мышц. Аутологичная пересадка мышц обычно выполняется в клинической ситуации, когда после травмы, резекции опухоли или повреждения нерва возникают большие участки мышечной потери, что значительно ухудшает двигательную функцию. Хирурги трансплантируют здоровую мышцу из донорского участка, не затронутого повреждением, для восстановления утраченной или нарушенной функции. При отсутствии прилегающей мышцы из-за высокого уровня повреждений нерва или тяжелой травмы может быть применена аутологичная трансплантация мышцы в виде свободной функциональной пересадки. Часто используемыми аутологичными мышцами являются m. latissimus dorsi и m. gracilis. Было показано, что пересадка m. latissimus dorsi является безопасной и эффективной для восстановления сгибания локтевого сустава [8]. В случае синовиальной саркомы, поражающей m. gluteus medius и m. gluteus minimus, функция пораженного тазобедренного сустава может быть полностью восстановлена с помощью свободной нейроваскулярной трансплантации m. latissimus dorsi. Трансплантация m. gracilis обычно используется для восстановления локтевого сустава после травмы плечевого сплетения. Хотя данные мышечные лоскуты могут приводить к значительным терапевтическим результатам, они вызывают прогрессирующую заболеваемость донорского участка и недостаточность иннервации. Более того, до 10% этих реконструктивных операций приводят к полному отторжению трансплантата из-за таких осложнений, как инфекция и некроз.
Заключение. Повреждение скелетной мышечной ткани или атрофия мышц встречается довольно часто. Хирургические методы достигли значительных результатов и могут гарантировать хорошие результаты для восстановления мышечных функций. Однако, при хирургическом вмешательстве всегда остается риск, обусловленный как человеческим фактором, так особенностями операции. Исследования в области тканевой инженерии и регенеративной клеточной терапии могут решить данную проблему. Тканевая инженерия использует биологические скаффолды, которые направляют развитие мышечной ткани при участии факторов роста. Эти клетки способствуют пролиферации миогенных клеток в поврежденных или атрофических мышцах, что отражается на их дальнейшей регенерации. Подобные творческие подходы опираются на глубокое понимание процесса, необходимого для функционального восстановления мышц (реакция клеток на скаффолды, васкуляризация, миогенез и иннервация), однако все равно нуждаются в дальнейших исследованиях.