Гипертензия без значительной протеинурии что это
Гипертензия без значительной протеинурии что это
Гестоз – это тяжелое осложнение беременности, существенно повышающее материнскую и младенческую заболеваемость и смертность.
Согласно статистическим данным, в России гестоз занимает третье место в структуре материнской смертности, уступая лишь экстрагенитальным заболеваниям и кровотечениям. Однако наши исследования (В.Н. Серов и соавт., 1997, 2002) показали, что при кровотечениях и сепсисе гестоз был основной причиной смерти в 35–40 % случаев. Кроме того, если материнская смертность от кровотечений и сепсиса снижается, то смертность от гестоза остается стабильной. В развитых странах гестоз является основной причиной материнской смертности.
Перинатальная смертность при гестозе превышает средние показатели в 5–7 раз.
Гестоз (преэклампсия и эклампсия) называют болезнью теорий, так природу этого клинического синдрома пытались объяснить самымими разными причинами – поражением почек, эндокринными изменениями, иммунологической несовместимостью, инфекциями, аутоиммунной патологией, сосудистыми и эндотелиальными дисфункциями и др. Каждая отдельно взятая теория не могла охватить все многообразие клиники, но многие из перечисленных факторов реально участвуют в патогенезе происходящих при гестозе нарушений.
Наибольшее значение в клинике гестоза имеют гиповолемия, периферический сосудистый спазм, изменение функции эндотелия, нарушения гемостаза. По мнению В.Н. Серова и Н.М. Пасмана, этиологически это патологическое состояние в первую очередь определяется иммунологическими и аутоиммунными нарушениями. Было показано, что патогенез гестоза укладывается в синдром системного воспалительного ответа и в тяжелых случаях характеризуется полиорганной недостаточностью.
Частота гестоза, согласно данным различных авторов (В.Н. Серов и С.А. Маркин, Р.И. Шалина, Е.М. Шифман), колеблется в пределах от 5 до 20 % по отношению ко всем беременностям. Такие различия обусловлены различными подходами к определению самого понятия «гестоз».
Со времен В. Цангемейстера это заболевание характеризуется триадой симптомов, формирующейся после 20 недель беременности и включающей артериальную гипертензию, протеинурию и отеки.
Оценивая клинические проявления гестоза, основное внимание уделяют артериальной гипертензии, степень которой лежит в основе почти всех современных классификаций преэклампсии (гестоза). В зарубежной литературе гестоз чаще всего обозначается как артериальная гипертензия при беременности или преэклампсия.
Международная статистическая классификация болезней (МКБ-10, 1995) предусматривает следующую классификацию отеков, протеинурии и гипертензивных расстройств во время беременности, родов и в послеродовом периоде.
В настоящее время чаще всего используется классификация преэклампсии Американской ассоциации акушеров и гинекологов, которая легла в основу современной классификации ВОЗ (табл. 1).
В России принята классификация гестоза, представленная в таблице 2.
Основное различие между американской и российской классификациями заключается в терминах – “гестоз” и “преэклампсия”. В американской классификации ставится знак равенства между нефропатией и преэклампсией, повышая настороженность лечащего врача. В то же время, в ней выделяют легкую и тяжелую преэклампсию, как бы стирая между ними грань. Особое внимание уделяется артериальной гипертензии, причем четко выделяется гипертензия, бывшая до беременности, что является несомненным преимуществом этой классификации. В целом, классификация Американской ассоциации акушеров и гинекологов в большей степени отвечает запросам практики, не отличается от рекомендуемой ВОЗ и, видимо, найдет более широкое применение в нашей стране.
Патофизиология преэкламсии заслуживает особого внимания, так как рациональная лечебная практика невозможна без знания изменений, происходящих в организме беременной при этом патологическом состоянии.
Преэклампсия представляет собой синдром, оказывающий негативное воздействие на все органы и системы организма матери. Лежащие в основе преэклампсии патофизиологические механизмы не до конца изучены, однако установлено, что наиболее значимые патологические процессы, происходящие в плаценте, почках и головном мозге, сводятся к сосудистым эндотелиальным нарушениям, причем патологические изменения локализуются в основном в области плацентарной площадки.
При нормальном течении беременности эндотелий, внутренний эластичный слой и мышечные пластинки участка спиральных артерий, питающих плаценту, вытесняются трофобластом и фибриносодержащим аморфным матриксом (F. Lyall и G.A. Greer, 1994). Происходящие при этом изменения обусловливают понижение давления в сосудистом русле и дополнительный приток крови, обеспечивающий потребности плода и плаценты.
Преэклампсия характеризуется отсутствием проникновения или неполным проникновением трофобласта в спиральные артерии, что приводит к сужению их просвета и последующему развитию плацентарной ишемии. Измененная плацента может провоцировать образование одного или нескольких факторов, разрушающих сосудистые клетки, вызывая дисфункцию многих систем организма (J. Roberts и C.W. Redman, 1993).
Эндотелиальная клетка выполняет ряд важнейших функций, включая регуляцию обмена жидкости, профилактику внутрисосудистой коагуляции, изменение сократительной способности стенок гладкой мускулатуры, сохранение иммунного и противовоспалительного статусов (S.A. Freidman и соавт., 1991).
При повреждении эндотелиальные клетки не только утрачивают свою регулирующую функцию, но и продуцируют прокоагулянты, вазоконстрикторы и вещества, вызывающие трансформацию лимфоцитов. У беременной с преэклампсией повышена капиллярная проницаемость и чрезмерно выражена ответная реакция на ангиотензин. Повышение чувствительности к сосудосуживающему эффекту приводит к обширному вазоспазму и снижению перфузии органов. Падает продукция простоциклина, повышаются уровни фактора фон Виллебранда и фибронектина. Активированные нейтрофилы служат источником субстанций, выступающих в роли медиаторов сосудистых колебаний, определяющих изменения артериального давления. Было показано, что в крови больных преэклампсией происходит ускоренное формирование свободных радикалов, что в свою очередь нарушает функции эндотелия (G.A. Dekker и A.A. Kraayenbrink, 1991).
На рисунке представлены изменения, развивающиеся при преэклампсии в различных органах. Они свидетельствуют о том, что преэклампсия может быть охарактеризована как синдром полиорганной недостаточности (В.Н. Серов и соавт., 1997, 2002).
В последние годы было показано, что при преэклампсии, наряду с полиорганной недостаточностью, развивается синдром системного воспалительного ответа с характерным изменением иммунного состояния, цитокиновым каскадом, нарушениями гемостаза и возможной бактериальной транслокацией (В.Н. Серов и соавт., 2002).
Маркером эндотоксикоза у больных преэклампсией может служить содержание эндотоксина, антиэндотоксиновых антител и молекул средней массы (МСМ). В таблице 3 представлены подтверждающие это данные (В.Н. Серов, 2003).
Как следует из приведенных в таблице данных, в зависимости от тяжести преэклампсии уровень эндотоксина повышается параллельно с ростом содержания МСМ и снижением уровня антиэндотоксиновых антител. Увеличение выработки эндотоксина индуцирует выброс фактора некроза опухоли и цитокиновый каскад. Повторная стимуляция цитокинов может значительно усиливать полиорганную недостаточность, нарушения гемостаза, процессов дыхания и ферментативных реакций.
В последние годы получены новые данные о наиболее тяжелых формах преэклампсии. Обнаружено, что на фоне антифосфолипидного синдрома или наличия антифосфолипидных антител преэклампсия протекает особенно тяжело.
При аутоиммунной патологии развиваются особенно формы преэклампсии – HELLP-синдром и острый жировой гепатоз. Создается впечатление, что аутоиммунные нарушения являются фактором, предопределяющим развитие наиболее тяжелых осложнений при гестозе.
Диагностика преэклампсии, на первый взгляд, проста: определение повышенного АД, наличия отеков и протеинурии не представляет трудностей. Однако основным в диагностике являются определение степени тяжести гестоза и прогноз развития патологического процесса. Это обусловлено основной проблемой – можно ли продолжать беременность или необходимо прекратить ее, не считаясь с последствиями для плода. При тяжелой преэклампсии (см. классификацию в табл. 1) или после припадка эклампсии лечебная тактика состоит в относительно кратковременной интенсивной подготовке к родоразрешению: с помощью кесарева сечения при неподготовленных родовых путях или через естественные родовые пути.
В случаях, когда преэклампсию можно оценить как средней тяжести, а состояние плода по срокам гестации требует пролонгации беременности, можно избрать консервативную тактику. Однако в подобной ситуации нельзя исключить прогрессию преэклампсии и развитие полиорганных нарушений в виде множественных кровоизлияний в печень, легкие и головной мозг, отека и ишемии мозга, острой почечной недостаточности, приступа или приступов эклампсии с резким утяжелением общего состояния, церебральной комой, отеком легких и даже смертельным исходом.
Таким образом, врач сталкивается с дилеммой: прекратив развитие беременности, с большой вероятностью можно сохранить здоровье женщины, но может пострадать ребенок, особенно глубоконедоношенный.
В литературе можно найти многочисленные ссылки на различные клинические, биофизические и биохимических исследования, позволяющие прогнозировать развитие преэклампсии (G.A. Dekker и A.A. Kraayenbrink, 1991). Однако в большинстве случаев их результаты достаточно противоречивы. На современном этапе не существует идеального прогностического, отвечающего всем необходимым критериям способа. Как и прежде, прогноз продолжает, в основном, базироваться на отсутствии или наличии родов в анамнезе женщины и семейном анамнезе. Диагноз преэклампсии ставится в 5,8 % случаев первой беременности и только у 0,4 % женщин со второй беременностью (J.M. Roberts и C.W. Redman, 1993).
Ультразвуковое допплеровское исследование глубоко расположенных дугообразных артерий на 16–18 неделе беременности может оказаться полезным при выявлении нарушений, связанных с проникновением трофобласта в спиральные артерии, а также имеет определенное значение при прогнозировании беременностей, подверженных риску развития осложнений на фоне преэклампсии (S.A. Steel и соавт., 1990).
Ввиду отсутствия исчерпывающей информации об этиологии и патофизиологии преэклампсии разработка эффективных профилактических мер затруднена. Предполагалось, что аспирин может оказаться эффективным средством профилактики преэклампсии, однако эту гипотезу не удалось подтвердить в многочисленных исследованих (B.M. Sibai и S.N. Cаritis, 1993). С другой стороны, было показано, что прием кальцийсодержащих пищевых добавок позволяет добиться определенного снижения частоты артериальной гипертензии, преэклампсии и преждевременных родов (G.P. Waisman и L.M. Mayorga, 1988). Обращается внимание на отсутствие преэклампсии у беременных с пересаженной почкой на фоне лечения глюкокортикоидами и цитостатиками (Л.Е. Мурашко и А.И. Волобуев, 2002).
В настоящее время терапия преэклампсией базируется на лечении симптомов и признаков вторичных ее проявлений, при этом преследуется цель снижения частоты осложнений со стороны матери и плода. Следует помнить, что по-прежнему важны акушерская тактика и определение оптимальных сроков родоразрешения.
Тяжелая форма преэклампсии или доношенная беременность являются показаниями к родоразрешению.
В процессе подготовки к прекращению беременности необходимо провести гипотензивную, инфузионную и противосудорожную терапию. Антигипертензивные препараты, используемые при тяжелой преэклампсии, представлены в таблице 4.
Противосудорожная терапия осуществляется преимущественно с помощью магния сульфата, механизмы действия которого полностью не изучены. Предполагается наличие у этого препарата положительных эффектов в условиях спазма сосудов головного мозга.
Внутривенное введение магния сульфата предполагает нагрузочную дозу 4–6 г (16–24 мл 25 % раствора в течение 20 минут). Поддерживающая его доза составляет 2 г/час (80 мл 25 % раствора (20 г) в 500 мл 0,9 % раствора хлористого натрия или 5 % раствора глюкозы. Скорость введения – 50 мл/час (16 капель/мин).
При внутримышечном введении магния сустава нагрузочная доза составляет 10 г (по 5 г – 20 мл 25 % раствора в каждую ягодицу), поддерживающая – 5 г каждые 4 часа.
Инфузионная терапия должна быть малообъемной – 800–1200 мл, ее желательно проводить под контролем венозного давления. При отеке головного мозга инфузионная терапия целесообразна при соблюдении следующих условий: малый объем, сочетание кристаллоидов и коллоидов, применение крупномолекулярных гидроксиэтилированных крахмалов (например, Стабизол) и гипертонических солевых растворов (Е.М. Шифман и А.Д. Тиканадзе).
Преэклампсия средней степени тяжести (нефропатия) позволяет пролонгировать беременность до срока доношенного плода (36 недель). Лечение базируется на проведении гипотензивной, инфузионной и антисудорожной терапии.
В качестве антигипертензивных препаратов используются блокаторы кальциевых каналов (нифедипин, амлодипин), клонидин, метилдопа и лабеталол. Не рекомендуется применять ингибиторы ангиотензин-превращающего фермента и мочегонные средства.
Инфузионную терапию целесообразно проводить с использованием препаратов гидроксиэтилированного крахмала, назначение которых особенно оправданно в условиях генерализованного повреждения эндотелия.
По нашим данным (В.Н. Серов и соавт., 1999), применение 10 % гидроксиэтилированного крахмала (Инфукол) способствовало пролонгированию беременности при преэклампсии и снижало перинатальную смертность в 1,5–2 раза.
При недостаточной эффективности инфузионной терапии нами использовался плазмаферез. Для снижения уровня эндогенной интоксикации, оцениваемой по эндотоксинемии, содержанию МСМ и антиэндотоксиновых антител, были применены энтеро- и гемосорбция. Сорбент Энтеросгель назначался 3 раза в день в течение 2 недель в сочетании с гипотензивной и инфузионной терапией. Наблюдения включали 40 больных с гестозом (преэклампсией) средней тяжести. Из их числа досрочное прерывание беременности потребовалось только в 2 случаях, тогда как в контрольной группе досрочные роды пришлось вызывать у каждой третьей больной.
Динамика концентраций эндотоксина и МСМ после энтеросорбции и гемосорбции представлена в таблице 5.
Таким образом, несмотря на определенные достигнутые успехи, терапия гестоза (преэклампсии) остается достаточно сложной задачей. Необходимо проведение дальнейших исследований для определения точных механизмов этиопатогенеза этого заболевания, что будет способствовать разработке эффективных методов его профилактики и лечения.
Литература
Срок беременности более 20 недель;
Протеинурия (белок в моче более 0,3 г/л в суточной порции мочи**);
Массивные быстро
нарастающие отеки (особенно в области поясницы), анасарка,
скопление жидкости в полостях рассматриваются как один из неблагоприятных прогностических критериев тяжелой преэклампсии.
**Учитывая, что в рутинной практике чаще используется определение белка в разовой порции мочи, до исследования суточного объема мочи патологической следует считать любую протеинурию, зафиксированную в разовой порции мочи.
1.2. Критерии артериальной гипертензии во время беременности
– Регистрация величины систолического давления крови выше 140 мм рт. ст., диастолического давления крови выше 90 мм рт. ст. является
достаточной для соответствия критериям артериальной
гипертензии*
– Повышение систолического давления крови на 30 мм рт. ст. по сравнению с его средней величиной, зарегистрированной до 20 недели беременности;
– Повышение диастолического давления крови на 15 мм рт.ст. по сравнению с его средней величиной, зарегистрированной до 20 недели беременности;
*Систолическое давление крови 140 мм рт. ст., диастолическое давление крови 90
мм рт. ст. является пограничным с нормой, указывающим
на необходимость тщательного наблюдения за беременной.
1.3. Правила измерения артериального давления
Измерение артериального давления производят на ртутном или анероидном тонометре (использование автоматического прибора должно быть ограничено только самоконтролем пациентки в домашних условиях)
Пациентка должна быть расслаблена, после отдыха (не менее 5 минут)
Положение пациентки – сидя,
с упором спины и поддержкой руки, на которой проводится
измерение, манжета должна располагаться на уровне сердца*
Манжета аппарата должна соответствовать окружности плеча пациентки (не менее чем в 1,5 раза длиннее окружности плеча)
Манжета не должна располагаться на одежде пациентки
Уровень артериального давления фиксируется при помощи исключительно метода аускультации по Короткову (систолическое АД – начало I тона, диастолическое АД – прекращение V тона)
Показатели должны быть зафиксированы с точностью ± 2 мм рт.
ст.
*Положение на спине может вызвать гипотензию, в положении на левом боку фиксируется наиболее низкое АД, так как правая рука, на которой проводится измерение, чаще всего расположена выше уровня сердца.
1.4. Формы артериальной гипертензии при беременности
Хроническая артериальная гипертензия – повышение систолического давления крови выше 140 мм рт. ст., диастолического давления крови выше 90 мм рт. ст. АД, выявленное до беременности или
зарегистрированное до 20 недель беременности и сохраняющееся в
течение 42 дней после родов и более;
Преэклампсия и эклампсия (см. 1.1. Критерии постановки диагноза преэклампсии);
Хроническая артериальная гипертензия, осложненная преэклампсией;
Обусловленная беременностью артериальная гипертензия – артериальная гипертензия, впервые зарегистрированная во время беременности без протеинурии и других признаков преэклампсии;*
*У 15-45% беременных в дальнейшем переходит в
преэклампсию.
1.5. Степень тяжести артериальной гипертензии
– Норма (для нормотоников):
систолическое давление менее или равно 140 мм рт.ст.,
диастолическое давление менее или равно 90 мм рт.ст.
систолическое давление 140-159 мм рт.ст.,
диастолическое давление 90-109 мм рт.ст.
систолическое давление более и равно160 мм рт.ст.,
диастолическое давление более и равно 110 мм рт.ст.
*Данная классификация
может использоваться для характеристики степени повышения уровня артериального давления при любой форме артериальной гипертензии.
1.6. Классификация*
O13 Вызванная беременностью гипертензия без значительной протеинурии
O14 Вызванная беременностью гипертензия со значительной протеинурией
O14.0 Преэклампсия [нефропатия] средней тяжести
O14.1 Тяжелая
преэклампсия
O14.9 Преэклампсия [нефропатия] неуточненная
O15 Эклампсия
O15.0 Эклампсия во время беременности
O15.1 Эклампсия в родах
O15.2 Эклампсия в послеродовом периоде
O15.9 Эклампсия неуточненная по срокам
O16
Гипертензия у матери неуточненная
*Для постановки диагноза и оценки тяжести должна использоваться терминология МКБ Х пересмотра — Приказ МЗ РФ № 170 от 27.05.97 г «О переходе органов и учреждений здравоохранения Российской Федерации на Международную статистическую классификацию болезней и проблем, связанных со здоровьем Х пересмотра (с изменениями от 12 января 1998 г».
1.7. Профилактика*
При высоком риске преэклампсии допустимо применение аспирина в дозе 75 мг с 12 недели беременности при следующих условиях:
Артериальная
гипертензии при предыдущей беременности
Хроническая почечная недостаточность
Аутоиммунные заболевания (системная красная волчанка, антифосфолипидный синдром, гломерулонефрит и др.)
Сахарный диабет 1 и 2 типа
Хроническая артериальная гипертензия.
Допустимо
применение аспирина** в дозе 75 мг с 12 недели беременности при
более чем одном умеренном факторе риска преэклампсии:
Возраст 40 лет или старше
Интервал между беременностями более чем 10 лет
Индекс массы тела (BMI) 35 кг/м² и более при первом посещении
Семейная история
преэклампсии
*Этиология и патогенез преэклампсии и эклампсии до конца не изучены и эффективных мер профилактики и лечения в настоящее время не существует.
**При назначении ацетилсалициловой кислоты (аспирина) необходимо информированное согласие женщины на прием препарата, противопоказанного во время беременности.
***Другие препараты, в том числе: донаторы NO, прогестерон, гепарин и низкомолекулярный
гепарин, мочегонные средства, магний, фолиевая кислота, витамины С и Е, чеснок,
рыбий жир, ограничение соли не эффективны в отношении профилактики преэклампсии и могут применяться с какой-либо другой целью.
1.8. Критерии тяжести преэклампсии*
Средняя
Тяжелая
140/90 – 160/110 мм рт.ст.
АДсист более 160 мм рт.ст.
АДдиаст более 110 мм рт.ст.
Протеинурия более 2,0 г за 24 часа
При наличии симптомов преэклампсии следующие критерии:
повышение креатинина более 90 мкмоль/л
тромбоцитопения 9 /л
повышение АЛТ или АСТ
устойчивые головные боли или другие церебральные или зрительные расстройства.
устойчивая эпигастральная боль.
Острое повреждение легких/острый респираторный дистресс-синдром, отек легких
задержка развития плода или антенатальная гибель плода
*Четкое представление о степени тяжести необходимо для определения адекватной тактики ведения, т.к. пролонгирование беременности возможно только при отсутствии критериев тяжелой преэклампсии.
1.9.
Клинические проявления преэклампсии
1.9.1. Симптомы и симптомокомплексы
Со стороны центральной нервной системы:
— головная боль, фотопсии, парестезии, фибрилляции, судороги
Со стороны сердечно-сосудистой системы:
— артериальная гипертензия, сердечная недостаточность, гиповолемия.
Со стороны мочевыделительной системы:
— олигурия, анурия, протеинурия
Со стороны желудочно-кишечного тракта:
— боли в эпигастральной области, изжога, тошнота, рвота
Со стороны системы крови:
— тромбоцитопения, нарушения гемостаза, гемолитическая анемия
— задержка развития, внутриутробная гипоксия, антенатальная гибель.
1.9.2. Клинические варианты реализации тяжелой преэклампсии,
определяющие максимальный неблагоприятный исход
Нарушение функции ЦНС в результате кровоизлияния в мозг
Нарушение дыхательной функции в результате КРДС, отека легких, пневмония
Нарушение функции печени: HELLP-синдром, некроз, подкапсульная гематома
Все формы синдрома ДВС (явный или неявный)
Острая почечная недостаточность
Отслойка плаценты, геморрагический шок
1.9.3. Симптомы и симптомокомплексы, появление которых указывает
на развитие критической ситуации
Повышение уровня печеночных трансаминаз
Уровень креатинина более 90 мкмоль/л
Диастолическое АД более 110 мм рт.ст.
Влагалищное кровотечение (любой объем)
1.10. Объем лабораторного и функционального обследования, необходимый для дифференциальной диагностики преэкламсии тяжелой степени
1.10.1. В учреждении I уровня (минимум)
— уровень гемоглобина, количество эритроцитов, гематокрит, количество тромбоцитов, исключение внутрисосудистого гемолиза эритроцитов.
— общий белок, мочевина, креатинин, билирубин, глюкоза крови, активность АЛТ, АСТ.
— УЗИ (исключение критического состояния плода, плацентарной апоплексии)
— КТГ (постоянный мониторинг)
— неинвазивный мониторинг у женщины (АД, ЧСС, ЧДД, диурез)
1.10.2. В учреждении II и III уровня (дополнительно)
—
коагулограмма (количество тромбоцитов, АПТВ, МНО, фибриноген, продукты деградации фибриногена)
— тромбоэластограмма (при технической возможности на III уровне)
— уровень альбумина плазмы
— активность АСТ, АЛТ, щелочной фосфатазы крови, гаммаглутаматтрансферазы (ГГТП)
— кислотно-основное состояние и газы крови
— морфология эритроцитов (шизоциты), уровень свободного гемоглобина
— УЗИ плода, допплерометрия плодово-плацентарного и маточно-плацентарного
кровотоков
— транскраниальная допплерометрия сосудов головного мозга (при технической возможности на III уровне)
1.10.3. Дополнительные лучевые методы диагностики
Показания для проведения компьютерной томографии или магнитно-резонансной томографии головного мозга:
— судорожный приступ, зафиксированный ранее 20-й недели беременности или в первые двое суток после родов
— эклампсия, резистентная к
терапии магния сульфатом при наличии грубой очаговой неврологической симптоматики
— кома, сохраняющаяся после отмены седативной терапии в течение 24 часов.
1.11. Рекомендации по лечению
1.11.1. Противосудорожная терапия
Магния сульфат (группа А по FDA) – основной препарат для лечения тяжелой преэклампсии и профилактики развития эклампсии: риск
развития эклампсии на фоне приема магния сульфата снижается на 58%.
Магния сульфат – противосудорожный препарат и его введение нельзя прерывать только на основании снижения артериального давления. Магния сульфат – препарат неотложной помощи и его плановое применение во время беременности не предотвращает развития и прогрессирования преэклампсии.
Схема применения: 5 г в/в за 10-15 мин, затем — 2 г/ч микроструйно. Терапия магния сульфатом у женщин с тяжелой преэклампсией и эклампсией должна продолжаться и не менее 48 ч после родоразрешения.
Препараты, имеющие второстепенное значение для достижения
противосудорожного эффекта при эклампсии и должны использоваться только как вспомогательные
средства и в течение короткого промежутка времени:
Бензодиазепины: диазепам 10 мг в/м или в/в (группа D по FDA). Эффекты диазепама: седативный, противосудорожный (уровень В).
Барбитураты: фенобарбитал 0,2 г/сутки энтерально (группа С по FDA). Эффекты фенобарбитала: противосудорожный, седативный (уровень В). Применение тиопентала натрия должно рассматриваться только как седация и противосудорожная терапия в условиях ИВЛ.
1.11.2. Гипотензивная терапия
Активная
гипотензивная терапия с применением внутривенных гипотензивных препаратов проводится только при уровне АД более 160/110 мм рт.ст. В прочих случаях используются только таблетированные гипотензивные препараты (метилдопа и антагонисты кальция):
Метилдопа (допегит): 500-2000 мг/сутки энтерально (группа В по FDA). Основной гипотензивный препарат при любой форме артериальной гипертензии во время беременности. Противопоказан при гепатите, печеночной недостаточности, феохромоцитоме.
Клофелин (клонидин): до 300 мкг/сутки в/м или энтерально (группа С по FDA). Используется только при устойчивой
артериальной гипертензии и для купирования гипертонического криза. Применение клонидина не имеет никаких
преимуществ перед использованием метилдопы или β-адреноблокаторов. На ранних сроках беременности применение клонидина недопустимо, так как считается, что он способен вызывать эмбриопатию. Противопоказан при синдроме слабости синусового узла, AV-блокаде, брадикардии у плода.
Нифедипин 30-60 мг/сут энтерально (группа С по FDA). В настоящее время доказана безопасность применения данного блокатора кальциевых каналов во время беременности.
Нимодипин 240 мг/сутки (группа С по FDA). Используется только для купирования спазма сосудов головного мозга при ишемическом поражении и эклампсии.
Противопоказан при отеке головного мозга, внутричерепной гипертензии, нарушении функции печени. Для его использования
необходима верификация спазма сосудов головного мозга (допплерометрия), особенно при внутривенном введении.
В некоторых ситуациях может применяться β-адреноблокатор:
Атенолол 25-100 мг/сут энтерально (группа С по FDA). Во время беременности используется только коротким курсом при артериальной гипертензии в сочетании с тахикардией – ЧСС более 100 в мин. Противопоказан при синусовой брадикардии, брадикардии у плода, AV блокаде, сердечной недостаточности, обструктивных заболеваниях легких, сахарном диабете.
При развитии тяжелой
гипертензии (систолическое давление более и равно160 мм рт.ст., диастолическое давление более и равно 110 мм рт.ст.) в настоящее время рекомендуется применение следующих препаратов:
– Урапидил (эбрантил): α-адреноблокатор. Препарат противопоказан во время беременности и эффективно используется непосредственно после родоразрешения. Способ применения: 25 мг урапидила разводится до 20 мл 0,9% физиологическим раствором и вводится со скоростью 2 мг/мин. по эффекту снижения артериального давления. После введения 25 мг урапидила необходимо оценить эффект препарата и его продолжительность. Поддерживающая доза 100 мг урапидила разводится 0,9% физиологическим раствором до 50,0 мл и вводили со скоростью от 4,5 мл/час по эффекту поддержания АД на
безопасном уровне.
При любом исходом уровне артериального давления его снижение должно быть плавным в течение 2-4 ч. Если на фоне проводимой гипотензивной терапии вновь отмечается повышение артериального давления, то это может служить поводом для пересмотра тяжести преэклампсии и даже решения вопроса о родоразрешении.
1.11.3. Инфузионная терапия
При проведении инфузионной терапии до родов следует ограничить объем вводимой внутривенно жидкости до 40-45 мл/ч (максимально 80 мл/ч) и предпочтение отдавать сбалансированным кристаллоидам (Рингер, Стерофундин). Применение синтетических (ГЭК, желатин) и природных (альбумин)
коллоидов не имеет преимуществ перед кристаллоидами в отношении материнских и перинатальных результатов при преэклампсии/
эклампсии и должно быть обусловлено только абсолютными показаниями (гиповолемия, шок, кровопотеря). Для всех синтетических коллоидов в инструкции по применению есть указание: во время беременности препарат можно использовать только тогда, когда риск применения ниже ожидаемой пользы.
Характеристика кристаллоидных растворов для инфузионной терапии у женщин с преэклампсией/эклампсией
Содержание в 1000 мл, ммоль/л
Плазма крови
136-143
2,38-2,63
0,75-1,1
96-105
280-290
Интерстициальная жидкость
Ограничительный режим инфузионной терапии применяется и после родоразрешения (исключение HELLP-синдром: см. ниже). При любом варианте развития критического состояния при преэклампсии/эклампсии
необходимо как можно раньше перейти к энтеральному питанию.
1.11.4. Трансфузионная терапия
Применение компонентов крови регулируется приказом МЗ РФ № 363 от 2002 г. Необходимо учитывать, что преэклампсия и её осложненные формы относятся к самому высокому риску массивных кровотечений в акушерстве. При оказании неотложной помощи пациенткам этой категории необходима готовность обеспечить хирургический, местный и консервативный гемостаз, интенсивную терапию массивной кровопотери (компоненты крови, факторы свертывания крови, возможность аппаратной реинфузии крови).
Некоторые особенности применения компонентов крови представлены ниже:
Компонент крови
Особенности применения
Кровопотеря > 30% ОЦК (более 1500 мл)
Сатурация смешанной венозной крови менее 65%
При решении о переливании тромбоцитов
необходимо исключить иммунный характер тромбоцитопении.
Доза: 1 доза тромбомассы на 10 кг м.т.
Только при сочетании коагулопатии (МНО и АПТВ увеличено более чем в 1,5 раза от нормы) и геморрагического синдрома или массивной кровопотери.
Доза 15-20 мл/кг
Применяется как вспомогательное средство при снижении концентрации фибриногена менее 1,0 г/л.
Доза: 1 доза криопреципитата на 10 кг м.т.
Факторы свертывания крови II, VII, IX, X в
комбинации (Протромбиновый комплекс)
1. Острые кровотечения и хирургическая профилактика при врожденном дефиците одного или нескольких факторов протромбинового комплекса (II, VII, IX, X)
2. Приобретенный дефицит факторов протромбинового комплекса: кровотечения при приеме оральных антикоагулянтов, тяжелой патологии печени, дефиците витамина К
Доза: при остром
кровотечении 50 МЕ/кг
содержит факторы II, IX и X преимущественно в неактивированной форме, а также активированный фактор VII; коагулянтный антиген фактора VIII (FVIII C:Ag) присутствует в концентрации до 0.1 ЕД на 1 ЕД активности препарата.
— лечение и профилактика кровотечений у пациентов с ингибиторной формой гемофилии А;
— лечение и профилактика кровотечений у пациентов с ингибиторной формой гемофилии В;
— лечение и профилактика кровотечений у пациентов с приобретенными коагулопатиями вследствие ингибиторов к факторам VIII, IX и XI;
— для длительной терапии при ИИТ (программы индукции иммунной толерантности) с концентратом фактора VIII во избежание развития кровоточивости.
В нижеследующих ситуациях препарат Фейба ® может
быть использован исключительно тогда, когда применение соответствующих концентратов факторов свертывания является заведомо неэффективным, например, при высоком титре ингибиторов:
— диссеминированное внутрисосудистое свертывание: при лабораторных и/или клинических признаках, четко указывающих на поражение печени, поскольку вследствие замедления клиренса активированных факторов свертывания такие пациенты подвержены повышенному риску развития ДВС-синдрома;
— инфаркт миокарда, острый тромбоз и/или эмболия: у пациентов с предполагаемым или установленным диагнозом ИБС, а также с острым тромбозом и/или эмболией применение препарата Фейба ® показано только при угрожающих жизни кровотечениях.
Доза: 50-100 ЕД/кг массы тела каждые 6 ч, не превышая максимальную суточную дозу 200 ЕД/кг массы тела.
Рекомбинантный активированный фактор VII
У больных с приобретенной гемофилией.
У больных с врожденным дефицитом фактора VII.
У больных с тромбастенией Гланцмана при наличии антител к гликопротеинам IIb-IIIa и рефрактерностью (в настоящем или прошлом) к трансфузиям тромбоцитарной массы.
Дополнительные показания к применению препарата rfVIIa
Профилактика хирургического кровотечения у больных со сниженной активностью или дефицитом факторов свертывания крови, особенно со специфичными ингибиторами к плазменным факторам и приобретенной болезнью Виллебранда
Лечение кровотечений при неэффективности других мер:
— Хронические заболевания печени
— Тромбоцитопатии
— Тромбоцитопения, рефрактерная к тромбоцитарной массе
Геморрагические осложнения при травме или хирургии у больных без исходного системного ухудшения гемостаза
Геморрагические осложнения при применении hirudine, danaparoid, fondaparinux, и ингибиторов гликопротеидов IIb/IIIa
Геморрагический инсульт
Кровотечения в акушерстве.
Антитромбин III человеческий
Врожденный дефицит АТ III
Приобретенный дефицит АТ III:
Повышенное потребление: ДВС-синдром, осложнения беременности (преэклампсия), экстракорпоральное кровообращение
Снижение синтеза: на фоне приема лекарственных препаратов, заболевания печени
Повышенное выведение: нефротический синдром, тяжелая потеря крови
Доза:
ДВС-синдром:
1. Гематологическая реанимация: 6000 МЕ болюсно, затем 6000 МЕ ежедневно в течение 4 дней
2. Обычная реанимация: 3000 МЕ болюсно,
затем 1500 МЕ каждые 12 часов в течение 5 суток
Другие заболевания:
Начальная доза 1500 МЕ, поддерживающая – 750 МЕ через 8-24 часа до нормализации лабораторных показателей или до клинического выздоровления
Контроль уровня АТ III! Необходимо достигнуть 80- 120% в начале курса лечения, затем не ниже 70%
1.11.5. Ограничения лекарственной терапии
До родоразрешения у женщин с тяжелой преэклампсией/эклампсией нежелательно или даже противопоказано (см. инструкции) применение следующих препаратов:
нейролептики (дроперидол), ГОМК
свежезамороженная плазма, альбумин
синтетические коллиды (ГЭК, желатин)
экстракорпоральные методы (плазмаферез, гемосорбция, ультрафильтрация)
дезагреганты
глюкозо-новокаиновая смесь
диуретики (фуросемид, маннитол)
наркотические аналгетики (морфин, промедол)
На этапе интенсивной терапии и подготовке к родоразрешению противопоказаны в связи с высоким риском развития геморрагических осложнений:
дезагреганты (аспирин) и антикоагулянты (гепарин, НМГ)
после родоразрешения противопоказан метилэргометрин
1.12. ПОКАЗАНИЯ К РОДОРАЗРЕШЕНИЮ
1.12.1. Экстренные (минуты) показания к родоразрешению:
— кровотечение из родовых путей, подозрение на отслойку плаценты
— острая гипоксия плода, в сроке беременности более 28 недель
1.12.2. Срочное (часы*) родоразрешение**:
— синдром задержки
развития плода II-III степени
— нарушение состояния плода, зафиксированное по данным КТГ, УЗИ
— количество тромбоцитов менее 100*10 9 /л и прогрессирующее его снижение
— прогрессирующее ухудшение функции печени и/или почек
— постоянная головная боль и зрительные проявления
— постоянная эпигастральная боль, тошнота или рвота
— артериальная гипертензия не поддающаяся коррекции
__________________________________________________________________*Пролонгирование беременности более суток: возможно только при отсутствии диагноза тяжелая преэклампсия или эклампсия.
**При сроке беременности 37 недель и более пролонгирование беременности является нецелесообразным и служит самостоятельным фактором риска.
1.13. Анестезиологическое пособие на этапе родоразрешения
Основная задача интенсивной терапии и анестезии на этапе родоразрешения (консервативного или оперативного) – стабилизация состояния и профилактика прогрессирования осложнений, в том числе полиорганной недостаточности. Для решения этой задачи необходимо соблюдать следующие принципы:
Рекомендация 1:
Во всех случаях требуется предродовая (предоперационная) подготовка в течение 2-6-24 часов на основе базовой терапии преэклампсии (см. 1.10.
Принципы лечения).
Рекомендация 2:
При консервативном родоразрешении обязательно обезболивание методом эпидуральной аналгезии (см. 1.13.1. Анестезиологическое пособие при консервативном родоразрешении).
Рекомендация 3:
При операции кесарева сечения у женщин с преэклампсией методом выбора является регионарная (спинальная, эпидуральная) анестезия (см. 1.13.2. Регионарная анестезия при операции кесарева сечения).
Рекомендация 4:
При операции кесарева сечения у женщин с тяжелой преэклампсией и противопоказаниями к проведению регионраной анестезии и эклампсией метод выбора – общая анестезия (см. 1.13.3. Общая
анестезия при операции кесарева сечения).
Организация работы анестезиолога-реаниматолога и оснащение операционных и палат интенсивной терапии проводится в соответствии с Порядком оказания медицинской помощи взрослому населению по профилю «анестезиология и реаниматология», утвержденному приказом Министерства здравоохранения Российской Федерации от 15 ноября 2012 г. N 919н и Порядком оказания медицинской помощи по профилю «акушерство и гинекология (за исключением использования вспомогательных репродуктивных технологий)», утвержденному приказом
Министерства здравоохранения Российской Федерации от «01» ноября 2012 г. № 572н (подробно смотри в базовом протоколе анестезии в акушерстве)
1.13.1. Анестезиологическое пособие при консервативном родоразрешении
Эпидуральная анальгезия является обязательным компонентом оказания медицинской помощи при родоразрешении через естественные родовые пути пациенток с тяжелой преэклампсией. Для этого используются маркаин или ропивакаин в концентрации 0,125-0,25% с фентанилом 50-100 мкг.
1.13.2. Регионарная анестезия при операции кесарева сечения
При проведении операции кесарева сечения предпочтение должно быть отдано региональным методам обезболивания. Общая анестезия применяется только при наличии противопоказаний к проведению регионарной.
Техника выполнения спинальной и эпидуральной анестезии
Спинальная анестезия проводится по следующей схеме:
Перед операцией: устанавливается катетер в периферической вене и начинается инфузионная поддержка, которая проводится либо в виде прединфузии кристаллоидами в объеме 1000 мл или синтетическими коллоидами (ГЭК, желатин) в объеме 500 мл, либо инфузия проводится после выполнения регионарной анестезии в том же составе. В
любом случае проведение инфузии не должно задерживать выполнение операции (рекомендации ASA, 2007). Проведение инфузии не полностью предупреждает развитие артериальной гипотонии (аорто-кавальная компрессия).
Выполняется катетеризация мочевого пузыря.
Неинвазивный мониторинг (АД, ЧСС SpO2, ЭКГ)
Премедикация включает холиноблокатор (атропин 0,5 мг), антигистаминный препарат (димедрол 10 мг)
Техника спинальной анестезии: положение пациентки – сидя со спущенными ногами
или лежа на боку и выгнутой спиной. Проводится обработка места пункции (от копчика до нижнего угла лопаток) и через введенный предварительно интродюсер на уровне LII-LIII выполняется пункция
субарахноидального пространства. Должны использоваться только иглы размера 25-29 G и желательно «карандашной» заточки – Рencil-point. Попадание иглы в субарахноидальное пространство определяется по появлению спинномозговой жидкости в прозрачной канюле иглы. После введения местного анестетика игла немедленно извлекается и на место пункции накладывается стерильная салфетка.
Техника выполнения эпидуральной анестезии: Начальные мероприятия аналогичны таковым при спинальной анестезии.
После обработки антисептиком проводится анестезия
места пункции: обычно используется 1% р-р лидокаина 3-5 мл.
Игла Tuohy вводится
между остистыми отростками L2-L3 или L3-L4 в горизонтальном положении на боку или в положении сидя. Могут использоваться любые варианты доступа – медиальный, парамедиальный или боковой. Игла с мандреном продвигается вперед медленно и осторожно для исключения случайного прокола твердой мозговой оболочки. Попадание просвета иглы в эпидуральное пространство идентифицируется с помощью следующих признаков:
— ощущение «провала» иглы
— утрата сопротивления (Сикара и Форестье) – отсутствие ощущения сопротивления при
введении жидкости шприцом через иглу, пузырек воздуха в шприце не деформируется
—
отсутствие вытекания спинномозговой жидкости или крови
— свободное прохождение катетера за пределы иглы
После установки катетера обязательно проводится аспирационная проба.
После введения «тест-дозы» местного анестетика нет признаков спинномозговой анестезии Проведение «тест-дозы» обязательно!
После идентификации эпидурального пространства катетер проводится вверх на 3 см и крепится к коже на всем протяжении лейкопластырем или другим фиксатором. Во время проведения эпидуральной
анестезии в родах пациентка должна избегать положения на спине для профилактики аорто-кавальной компрессии.
Для седации пациентки во время операции могут использоваться такие внутривенные анестетики, как типопентал натрия 1-3 мг/кг и пропофол – 1-3 мг/кг. Последний также обладает противорвотным эффектом, что особенно
важно при развитии тошноты и рвоты во время спинальной анестезии.
Таким образом, можно предложить следующие схемы спинальной анестезии при операции кесарева сечения:
Маркаин Спинал 10,0- 12,5 мг интратекально.
Маркаин Спинал 10,0-12,5 мг интратекально + седация внутривенно тиопентал натрия 50-100 мг, пропофол 50-100 мг.
Схемы эпидуральной анестезии при операции кесарева сечения (оптимально вводить местный анестетик в
эпидуральное пространство дробно):
Ропивакаин 0,75% – 15-20 мл
Бупивакаин 0,5% – 15-20 мл
Общая анестезия при операции кесарева сечения
Общая анестезия проводится по следующей схеме:
Премедикация: атропин 0,5 мг, димедрол 10 мг.
Вводный наркоз с учетом риска развития высокой артериальной гипертензии: тиопентал
натрия 6-7 мг/кг и фентанил 50-100 мкг. Для предотвращения прогрессирования артериальной гипертензии на этапе операции до извлечения плода может использоваться ингаляционный анестетик: севофлюран до 1,5 об%. На качество водного наркоза следует обратить особое внимание – он не должен быть поверхностным, якобы для того, чтобы избежать медикаментозной депрессии плода, а как раз напротив, как можно более глубоким.
Миоплегия при интубации трахеи – сукцинилхолин (дитилин, листенон) 2 мг/ кг (возможна прекураризация).
Поддержание анестезии после извлечения
плода – тиопентал натрия, пропофол, аналгезия – фентанил 100-200 мкг. Миоплегия – антидеполяризующие миорелаксанты: тракриум, нимбекс, эсмерон. Из ингаляционных анестетиков предпочтительнее применение севофлюрана до 1,5 об%. Дозы и
кратность введения отдельных препаратов определяются продолжительностью операции после извлечения плода.
Для профилактики послеродового кровотечения у женщин с тяжелой преэклампсией и эклампсией интраоперационно может использоваться только окситоцин, а метилэргометрин абсолютно противопоказан.
При отсутствии других показаний для продленной ИВЛ (кровопотеря, шок, кома и др.) перевод на спонтанное дыхание и экстубация осуществляются только после оценки неврологического статуса (обязательно наличие сознания)
. Непосредственно после операции начинается/продолжается введение магния сульфата в дозе 2 г/ч для обеспечения противосудорожного эффекта.
2. ЭКЛАМПСИЯ. Основные рекомендации:
2.1. Критерии постановки диагноза эклампсии
Эклампсия – развитие судорожного приступа, серии судорожных приступов у женщин на фоне преэклампсии при отсутствии других причин, способных вызвать судорожный припадок.
В трети случаев эклампсия развивается внезапно на фоне любой по
степени тяжести преэклампсии и далеко не всегда является показателем серьезности поражения. Основным благоприятным фактором после развития судорожного приступа следует считать наличие сознания и искусственно, медикаментозно устранять
сознание возможно только при проведении общей анестезии при родоразрешении.
Лабораторные и инструментальные методы диагностики имеют низкую прогностическую ценность в отношении развития эклампсии.
Основные симптомы, предшествующие эклампсии
Артериальная гипертензия (>140/90 мм рт ст, или > +30/+15 от уровня нормы)
Протеинурия (более 0,3 г/сутки)
Отеки (умеренные отеки голеней)
При развитии судорожного приступа во время беременности необходимо провести дифференциальный диагноз со следующими заболеваниями:
— Сосудистые заболевания ЦНС
— Тромбоз вен сосудов головного мозга
— Опухоли головного мозга
— Абсцессы головного мозга
— Артерио-
венозные мальформации
— Инфекции (энцефалит, менингит)
— Тромботическая тромбоцитопеническая пурпура
2.2. Классификация эклампсии
Эклампсия во время беременности и в
родах*
Эклампсия в послеродовом периоде:
ранняя послеродовая (первые 48 ч)
поздняя послеродовая (в течение 28 суток после родов)
*Частота эклампсии: между 21 и 27 неделями — 7,5%, после 28недели – 91%, во время родов в 18-36%.
Для оценки
степени угнетения сознания при эклампсии может использоваться шкала комы Глазго.
Оценка степени угнетения сознания по шкале Глазго
Признак
Баллы
На обращенную речь
На болевой раздражитель
Целенаправленная на боль
Нецеленаправленная на боль
Тоническое сгибание на боль
Тоническое
разгибание на боль
Сумма баллов
Традиционные термины
Оценка глубины медикаментозной седации
проводится по шкале Ramsay или Richmond
Шкала оценки степени седации Ramsay
1 — Пациент бодрствует, беспокоен, взволнован, нетерпелив.
2 —
Пациент бодрствует, сотрудничает с врачом, ориентирован, спокоен.
3 — Пациент в
сознании, но реагирует только на команды.
4 — Пациент дремлет, но реагирует на прикосновение или громкий звук.
5 — Пациент спит, вяло отвечает на прикосновение или громкий звук, но активно реагирует на болезненный стимул
6 —
Пациент спит и не реагирует на раздражители.
Шкала оценки возбуждения-седации Richmond
Баллы
Состояние
Описание
Явное агрессивное поведение; непосредственная опасность для персонала
Тянет или удаляет
трубки (и) или катетеры (и) или агрессивное поведение
Частые нецелеустремленные движения или десинхронизация с респиратором
Беспокоен или тревожен, не агрессивен
Не полностью бдителен, но
пробуждается (более 10 секунд), открывает глаза на голос
Короткое (менее 10 секунд) пробуждение с открыванием глаз на голос
Никакой реакции (не открывает глаза) на голос
Реакция (любое движение) на физический стимул
Невозможность разбудить больного
Никакого ответа на голосовой или физический стимул
За исключением случаев проведения продленной ИВЛ у пациенток с преэклампсией/эклампсией следует избегать состояния глубокой медикаментозной седации.
2.3. Принципы лечения
ПРИНЦИП № 1:
Главным препаратом для лечения и
профилактики последующих судорожных приступов является магния сульфат, другие препараты (бензодиазепины и барбитураты) играют вспомогательную роль.
При развитии эклампсии необходимо быть готовым к профилактике и лечению таких осложнений эклампсии как отслойка плаценты (7-11%), ДВС-синдром (8%), отек легких (3-5%), острая почечная недостаточность (5-9%), HELLP-синдром (10-15%), гематома печени (1%), аспирационная пневмония (2-3%), легочно-сердечная недостаточность (2-5%), острая гипоксия плода (48%).
2.4. Интенсивная терапия эклампсии
Цель интенсивной терапии эклампсии в дородовом
периоде — только стабилизация состояния, что включает следующие мероприятия:
Обеспечение проходимости дыхательных путей
Поворот на левый бок
Катетеризация периферической вены и введение магния сульфата 25%-20 мл медленно с последующей инфузией 2,0 г/ч
Неинвазивный мониторинг: АД, ЧСС, SpО2
Почасовой контроль диуреза
Ингаляция увлажненного кислорода/ИВЛ
Дальнейшая базовая терапия не отличается от терапии тяжелой преэклампсии (см. 1. преэклампсия. Основные рекомендациИ).
АЛГОРИТМ неотложной помощи и интенсивной терапии пРИ преэклампсии, эклампсиии
3.1. Догоспитальный этап (женская консультация, скорая медицинская помощь, амбулаторный прием смежных специалистов)
Оценка тяжести преэклампсии: АД, сознание, головная боль, судороги, одышка, боли в животе, кровотечение из родовых путей, сердцебиение плода
Венозный доступ: периферическая вена
Магния сульфат 25% 20 мл в/в медленно (за 10 мин) и 100 мл через инфузомат со скоростью 2 г/ч. Инфузия: только магния сульфат на р-ре NaCl 0,9% (или другого кристаллоида)
При АД выше 160/110 мм рт.ст. – гипотензивная терапия метилдопа, нифедипин
При судорогах: обеспечение проходимости дыхательных путей
При судорогах или судорожной готовности – бензодиазепины (диазепам 10 мг) в/в однократно
При отсутствии сознания и/или серии судорожных приступов – перевод
на ИВЛ с тотальной миоплегией
Госпитализация в роддом/перинатальный центр исключительно на транспортировочных насилках
3.2. Госпитальный этап
3.2.1. Приемный покой
Оценка тяжести преэклампсии: АД, сознание, головная боль, судороги, одышка, боли в животе, кровотечение из родовых путей, сердцебиение плода
Анестезиолог-реаниматолог вызывается в приемный покой при поступлении женщины в следующих ситуациях:
— развитии судорог (судороги в анамнезе)
— высоком АД – выше 160/110 мм рт.ст.
— при симптомах
отслойки плаценты, кровотечении из родовых путей и геморрагическом шоке
3.2.2. Госпитальный этап (палата интенсивной терапии)
При АД выше 140/90 м рт.ст. – госпитализация в ПИТ роддома
Оценка тяжести преэклампсии: АД, сознание, головная боль, судороги, одышка, боли в животе, темп диуреза,
кровотечение из родовых путей, сердцебиение плода + УЗИ плода + КТГ + лабораторный контроль (протеинурия, тромбоциты, МНО, АПТВ, ПДФ, общий белок, альбумин, билирубин, АСТ, АЛТ, эритроциты, гемоглобин, лейкоцитоз, креатинин, калий, натрий)
Венозный доступ: периферическая вена. Не рекомендуется катетеризация подключичной вены без абсолютных показаний (шок, гиповолемия)! При тяжелой преэклампсии нет показаний для контроля ЦВД.
Катетеризация мочевого пузыря и почасовой контроль диуреза. Нельзя использовать диуретики и допамин для коррекции олигурии!
Магния сульфат 25% 20
мл в/в медленно (за 10 мин) и 100 мл дозатором со скоростью 2 г/ч
Другие противосудорожные препараты (бензодиазепины, барбитураты) должны использоваться осторожно и только
при неэффективности магния сульфата
Общий объем инфузии: только кристаллоиды (Рингер, Стерофундин) 40-80 мл/ч при диурезе более 0,5 мл/кг/ч
Гипотензивная терапия: метилдопа, нифедипин
Оценка состояния родовых путей
3.2.3. Госпитальный этап (после родоразрешения)
Ранняя нутритивная поддержка – с первых часов после операции
Магния сульфат 1-2 г/ч в/в не менее 48 ч
Гипотензивная терапия при АДдиаст >90 мм рт.ст. (урапидил см. выше)
Тромбопрофилактика до 7 дней после родоразрешения (фармакологическая и механическая)
Инфузионная терапия до 20-25 мл/кг (до 1500 мл/сутки)* в зависимости от потерь ОЦК во время родоразрешения. Используются кристаллоиды (Рингер, Стерофундин) и по строгим показаниям (шок, гиповолемия) синтетические коллоиды – ГЭК (венофундин, тетераспан) или гелофузин.
*В
любом случае придерживаться ограничительной стратегии инфузионной терапии!
3.2.4. Госпитальный этап (продленная ИВЛ)
Показания к продленной ИВЛ при тяжелой преэклампсии и эклампсии:
Нарушение сознания любой этиологии (лекарственные препараты, отек головного мозга, нарушение кровообращения, объемный процесс, гипоксия).
Кровоизлияние в мозг.
Проявления коагулопатического кровотечения.
Сочетание с шоком (геморрагическим, септическим, анафилактическим и т.д.).
Картина острого повреждения легких (ОПЛ) или острого респираторного дистресс-синдрома (ОРДС), альвеолярный отёк легких.
Нестабильная гемодинамика (некорригируемая артериальная гипертензия более 160/110 мм рт.ст., либо наоборот, артериальная гипотония, требующая применения вазопрессоров).
Прогрессирующая
полиорганная недостаточность (церебральная, ОРДС, ДВС-синдром, почечная, печеночная недостаточность).
При проведении продленной ИВЛ необходимо обеспечить режим нормовентиляции и уже в
первые часы после родоразрешения определить степень неврологических нарушений. Для это цели первым этапом отменяются миорелаксанты и оценивается судорожная готовность. При её отсутствии, следующим этапом, отменяются все седативные препараты за исключением магния сульфата, обеспечивающего в этих условиях противосудорожный эффект. После окончания эффекта седативных препаратов определяется уровень сознания, при неосложненном течении эклампсии элементы сознания должны появляться в течение 24 ч. Если этого не происходит при полной отмене седативных препаратов в течение суток, то необходимо проведение компьютерной и магнитно-резонансной томографии головного мозга. В этой ситуации ИВЛ
продолжается до уточнения диагноза.
HELLP-СИНДРОМ. ОСНОВНЫЕ РЕКОМЕНДАЦИИ:
4.1. Определение и критерии постановки диагноза
Одним из таких серьезных поражений печени, связанных с беременностью, является HELLP-синдром (термин впервые предложен в 1982 году L. Weinstein). Данный акроним включает:
Hemolysis — свободный гемоглобин в сыворотке и моче
Elevated Liver enzimes — повышение уровня АСТ, АЛТ
Low Platelets – тромбоцитопения.
В зависимости от набора признаков выделяют полный HELLP-синдром и парциальные его формы: при отсутствии гемолитической анемии развившийся симптомокомплекс обозначают как ELLP-синдром, а при отсутствии или незначительной выраженности тромбоцитопении – HEL-синдром. Парциальный HELLP-синдром, в отличие от полного, характеризуется более благоприятным прогнозом. Поскольку в подавляющем большинстве случаев (до 80-90%) тяжелая преэклампсия и HELLP-синдром
сочетаются друг с другом и рассматриваются как единое целое, то мы объединили их в один раздел.
4.2. Особенности клинического течения
Частота HELLP-синдрома в общей популяции беременных женщин составляет 0,5-0,9%, а при тяжелой преэклампсии и эклампсии он встречается в 10-20% случаев. В 70% случаев развивается во время беременности (в — 10% — до 27 недели, в 50% — 27-37 недель, и в 20% — после 37 недели). В 30% случаев HELLP-синдром проявляет себя в течение 48 ч после родов и это еще раз, как и в случае с послеродовой эклампсией, свидетельствует о том, что женщины с тяжелой преэклампсией должны активно наблюдаться и получать весь комплекс интенсивной терапии не менее 48 ч после родоразрешения. Интересный факт: в 10-20% его развитие не сопровождается
артериальной гипертензией и протеинурией, что еще раз свидетельствует о более сложных механизмах формирования HELLP-синдрома, чем только преэклампсия. Избыточная прибавка массы тела и отеки предшествуют развитию HELLP-синдрома в 50% случаев. HELLP-синдром относится к одному из самых тяжелых вариантов поражения печени и острой печеночной
недостаточности, связанной с беременностью: перинатальная смертность достигает 34%, а летальность у женщин до 25%.
Материнские осложнения HELLP-синдрома весьма серьезны и их частота изменяется в зависимости от степени тяжести и формы (полный или парциальный). К ним относятся ДВС-синдром 5-56%, отслойка плаценты 9-20%, острая почечная недостаточность 7-36% как следствие внутрисосудистого гемолиза, ДВС-синдрома и гипоксии. Массивный асцит встречается в 4-11%, отек легких в 3-10%. Частота внутримозговых кровоизлияний
колеблется от 1,5 до 40% случаев и прямо зависит от степени тяжести коагулопатии (тромбоцитопения, дефицит факторов протромбинового комплекса). Реже встречаются эклампсия 4-9%, отек головного мозга 1-8%, подкапсульная гематома печени 0,9-2,0% и разрыв печени 1,8. Последние варианты поражения печени и обусловливают такой метод лечения этой
патологии, как трансплантация печени.
К перинатальным осложнениям HELLP-синдрома относятся задержка развития плода 38-61%, преждевременные роды 70%, тромбоцитопения новорожденных 15-50%, респираторный дистресс-синдром 5,7-40%, а перинатальная смертность варьирует от 7,4 до 34%.
Перечисленные выше осложнения убедительно показывают, что особое значение в успешном исходе при HELLP-синдроме, также как и при преэклампсии,
имеет ранняя диагностика и своевременное родоразрешение.
4.3. Лабораторная диагностика и классификация
Оценка степени тяжести HELLP-синдрома основана на критериях Tennessee, которые включают только одну степень тяжести – максимальную: тромбоциты 9 /л, АСТ > 70 ЕД/л, ЛДГ > 600 ЕД/л. По критериям Mississippi выделяют три класса тяжести HELLP-синдрома: 1 класс — тромбоциты 9 /л, АСТ, АЛТ > 70 ЕД/л, ЛДГ > 600 ЕД/л, 2 класс — тромбоциты 50-100 9 /л, АСТ, АЛТ > 70 ЕД/л, ЛДГ > 600 ЕД/л, 3 класс — тромбоциты 100-150 9 /л, АСТ, АЛТ 40-70 ЕД/л, ЛДГ > 600 ЕД/л.
Рис.1 Внешний вид гемолизированной сыворотки крови (
справа)
К прочим признакам HELLP-синдрома относятся: боли в животе как проявление растяжения капсулы печени и тканевой ишемии, увеличение продуктов деградации фибрина/фибриногена (ПДФФ), как отражение ДВС-синдрома, снижение уровня гемоглобина, метаболический ацидоз, увеличение уровня непрямого билирубина, ЛДГ и обнаружение обломков эритроцитов (шизоциты) в мазке крови как отражение гемолиза. Гемоглобинемия и гемоглобинурия макроскопически выявляются лишь у 10% пациенток с HELLP-синдромом. Ранним и специфическим лабораторным признаком
внутрисосудистого гемолиза является низкое содержание гаптоглобина (менее 1,0 г/л).
Помимо определения АСТ и АЛТ к ранним признакам поражения печени относится определение глутатион S-трансферазы (GST-a1 или α-GST).
К важнейшим предикторам и критериям тяжести HELLP-синдрома, безусловно, относится и тромбоцитопения, прогрессирование и степень выраженности которой прямо коррелирует с геморрагическими осложнениями и тяжестью ДВС-синдрома.
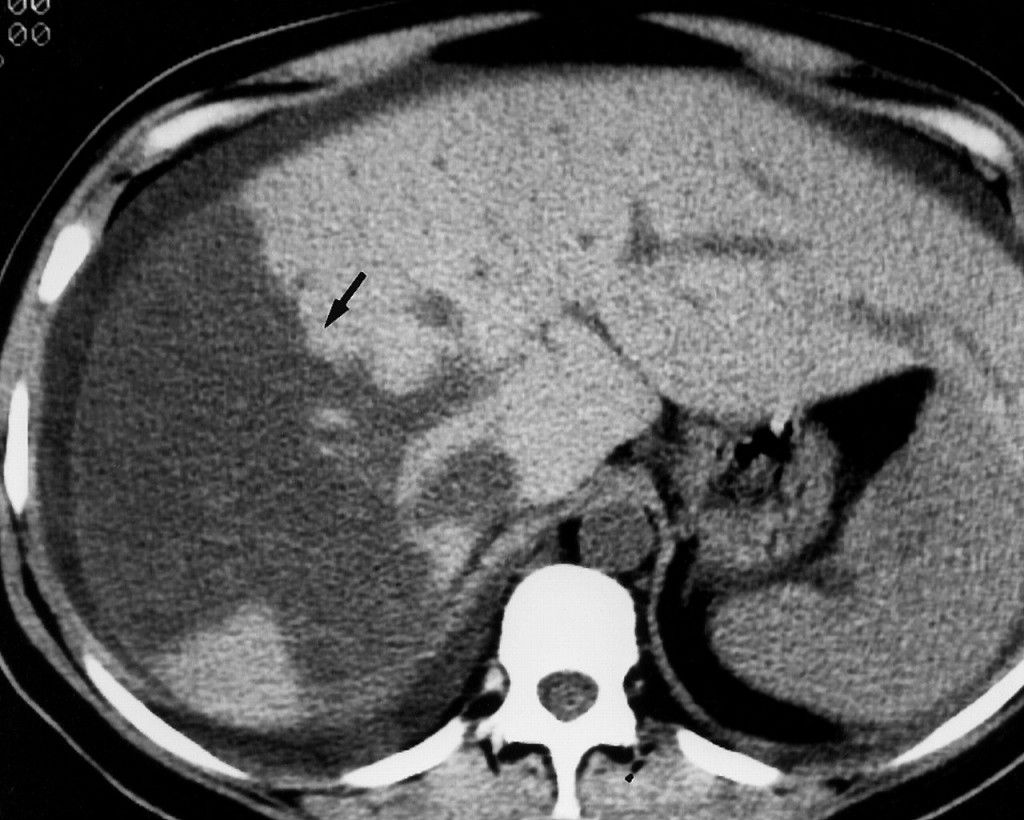
Рис. 2. Массивный очаг некроза в печени по данным МРТ
4.4. Дифференциальная диагностика
Дифференциальный диагноз HELLP синдрома весьма непрост. К заболеваниям, с которыми необходимо дифференцировать HELLP-синдром относятся гестационная тромбоцитопения, острая жировая дистрофия печени, вирусный гепатит, холангит, холецистит, инфекция мочевых путей, гастрит, язва желудка, острый панкреатит, иммунная тромбоцитопения, дефицит фолиевой кислоты, системная красная волчанка, антифосфолипидный синдром, тромботическая тромбоцитопеническая пурпура, гемолитико-уремический синдром.
Дифференциальная диагностика связанных с беременностью микроангиопатий представлена ниже:
Дифференциальная диагностика микроангиопатий,
связанных с беременностью