Гигантоклеточный артериит что это такое
Ревматическая полимиалгия и гигантоклеточный артериит
Ревматическая полимиалгия (РП) — системное воспалительное заболевание неясной этиологии, встречающееся у людей пожилого возраста, характеризующееся болями и скованностью мышц плечевого и/или тазового пояса. Нередко (в 15%) РП сочетается с гигантоклеточным
Ревматическая полимиалгия (РП) — системное воспалительное заболевание неясной этиологии, встречающееся у людей пожилого возраста, характеризующееся болями и скованностью мышц плечевого и/или тазового пояса. Нередко (в 15%) РП сочетается с гигантоклеточным (височным) артериитом (ГА), ранее именовавшимся как болезнь Хортона.
Первое описание РП представил William Bruce в 1888 г., когда было опубликовано наблюдение над пятью пожилыми пациентами с болями в проксимальных отделах конечностей и выраженной утренней скованностью и дано обозначение этому симптомокомплексу как «сенильная ревматическая подагра». В дальнейшем заболевание рассматривалось в рамках плечелопаточного периартроза. В 1945 г. L. Bagratuni предложил термин «несуставной ревматоидный артрит», наблюдая за восемью пациентами с первоначальным диагнозом ревматоидного артрита (РА), у которых заболевание протекало нетипично с поражением проксимальных отделов конечностей и отсутствием суставных деформаций. Но и этот термин не полностью отражал суть болезни и был принят не всеми. В разных странах заболевание определялось по-разному: «гемискапулярный периартроз» (Einar Meulengracht), «ризомелический псевдополиартрит» (Jacques Forestier и E. Certonncini), «ревматоидный синдром у лиц пожилого возрастав» (G. D. Kersley).
Термин «ревматическая полимиалгия» (РП) впервые был предложен в 1957 г. H. S. Barber и вскоре стал общепринятым. Работы L. A. Healey, определившего РП как системное заболевание суставов, основным проявлением которого является доброкачественный синовит, показали патогенетическую необоснованность термина «полимиалгия», который все же исторически продолжает использоваться для обозначения данного страдания. В нашей стране заболевание изучается с начала 70-х годов благодаря работам М. Г. Астапенко, С. Д. Сидельниковой, Э. Р. Агабабовой, которые в 1976 г. представили описание клинического случая РП. Позже уже Н. В. Бунчук опубликовал монографию (1992 г.) «Гигантоклеточный артериит и ревматическая полимиалгия».
В настоящее время общепризнано, что РП нельзя относить к редкой патологии. По данным мировой статистики частота заболевания колеблется от 28,6 до 133 на 100 тыс. населения старше 50 лет с возрастным пиком в 65–75 лет. Начинается РП исключительно в пожилом возрасте. Крайне редко болезнь поражает более молодых лиц (45–49 лет). В отличие от этого, ГА встречается и у молодых лиц. Примечательно, что РП развивается почти исключительно у физически крепких людей без серьезных соматических расстройств и в 2–3 раза чаще у женщин, чем у мужчин [1]. В США заболевают представители только белой расы в возрасте 50 лет и старше с частотой 53,7 на 100 тыс., в Швеции — 28,6 на 100 тыс., в Норвегии — 32,8 на 100 тысяч. РП болеют и жители южных стран, например, Италии и Испании [2]. Распространенность ГА в настоящее время составляет 200 на 100 тыс. лиц старше 50 лет, причем в скандинавских странах он встречается чаще, чем в других европейских государствах и США [3]. За последние годы, по мере роста осведомленности врачей, число диагностированных случаев ГА постоянно увеличивается.
Несмотря на то, что изучением этих заболеваний занимаются более 50 лет, их этиология остается неизвестной. Доказана наследственная предрасположенность к этому заболеванию. При HLA-типировании с повышенной частотой выявляются аллели HLA-DRB1*04 и DRB1*01, обнаружение которых служит фактором риска развития РП и ГА [4]. Что касается РП, то не исключена роль вирусной или бактериальной инфекции в ее возникновении. Поиски инфекционного начала оказались безуспешными: изучали уровень антител к различным вирусам, но поиски антител не привели пока к положительным результатам [5]. Тем не менее, в круг возбудителей, которые могут вызывать данное заболевание, в настоящее время включают парвовирус, аденовирус, вирус гриппа, а также Chlamydia pneumoniae, стимулирующие иммунную систему у генетически предрасположенных индивидуумов [4]. В Швеции в 1994 г. после эпидемической вспышки парвовирусной инфекции наблюдался высокий подъем заболеваемости РП на протяжении 12 месяцев после эпидемии. Описаны случаи возникновения РП вслед за вакцинацией от гриппа [6]. В последние годы в развитии РП большое значение стали придавать экологическому фактору. Обсуждается роль стрессовых ситуаций, переохлаждения.
Патогенез РП остается загадкой. Несомненно участие иммунной системы, хотя ни стойких дефектов иммунного ответа, ни специфических антител не выявлено. Отмечается повышенная продукция интерферона гамма, интерлейкина-1 и интерлейкина-6 [4]. Патоморфология РП характеризуется отсутствием полиорганности, в отличие от других диффузных заболеваний соединительной ткани.
Несмотря на название РП — это системное заболевание суставов, без каких-либо признаков поражения мышечной ткани. Многочисленные исследования биоптатов болезненных мышц не выявили морфологических изменений. При этом системном воспалительном заболевании соединительной ткани поражаются соединительнотканные структуры только периартикулярных тканей и синовиальной оболочки: сухожилия мышц в местах прикрепления к костям, капсула суставов, соединительнотканные прослойки мышц, фасции и т. д. Обязательным является развитие бурситов [6]. В последнее время доказано наличие синовита крупных проксимальных суставов у всех больных РП. Реже встречается синовит более дистальных суставов. Синовиальная природа заболевания подтверждается такими методами обследования, как артроскопия, МРТ и сцинтиграфия суставов. Характерной особенностью синовита при РП в отличие от РА является более доброкачественное течение, отсутствие эрозивных изменений суставной кости, отсутствие деформаций суставов и склонность к самопроизвольному излечению.
Заболевание, как правило, начинается остро, среди полного здоровья. Больной ложится спать в хорошем самочувствии, а утром не может встать с постели из-за выраженной боли и скованности суставов. Чаще наблюдается нарастание симптомов в течение 1–2 дней, иногда развитие их происходит постепенно. Нередко начало заболевания связывают с перенесенным ОРВИ. Иногда развернутой клинической картине предшествует бессимптомное ускорение СОЭ или длительный лихорадочный синдром, что заставляет включать РП при проведении дифференциальной диагностики в рамках «лихорадка неясного генеза» у пожилых [7, 8].
Наиболее характерным проявлением РП является синдром поражения опорно-двигательного аппарата: боль и скованность в проксимальных отделах конечностей. В 100% случаев поражения симметричны, хотя в самом начале возможна односторонность поражения. Одновременно боли отмечаются не менее чем в двух из указанных трех областей. Постоянные боли режущего, тянущего, рвущего характера резко усиливаются при движении. Характерна утренняя скованность. Кроме того, ощущение скованности появляется после любого периода неподвижности. Интенсивность болей четко связана с активностью болезни. Из-за болей ограничиваются движения: больным трудно встать, сесть, поднять руки, завести их за спину, невозможно без помощи войти в транспорт и т. д. Важно пронаблюдать, как больной поднимается с постели: сначала медленно, морщась от боли, поворачивается на бок, подтягивает ноги к животу, спускает их с постели, опираясь руками, с трудом садится и лишь затем, также с помощью рук, встает. Боли могут возникать и в других областях опорно-двигательного аппарата (бедрах, голенях, ягодицах, спине, даже в предплечьях), но не столь закономерно. В покое боли обычно стихают, хотя в 25–30% случаев сохраняются. Часто беспокоят ночные боли, которые усиливаются под влиянием тяжести тела, давления. Сон из-за этого становится прерывистым, отдых нарушается [3].
Симптоматика болезни постепенно нарастает и через 2–6 недель достигает пика, при этом объективные изменения невелики. При пальпации мышц болезненность небольшая или отсутствует вообще. Нет ни атрофий, ни инфильтраций в мышцах плечевого и тазового пояса, мышечная сила сохранена.
Артриты при РП обычно появляются через несколько месяцев после возникновения мышечных болей: это ремиттирующий серонегативный симметричный синовит с небольшим отеком — признак обострения РП. Очень редко боли в кистях, синовииты, воспаление связочного аппарата кистей, тендовагиниты и т. д. манифестируют заболевание (так называемая дистальная мышечно-скелетная манифестация РП).
Особенностями суставного синдрома при РП являются [9]:
Артриты лучезапястных суставов могут сопровождаться односторонним или двусторонним синдромом запястного канала, проявлением которого могут быть парестезии, зябкость и онемение I–IV пальцев, усиливающееся ночью, при нагрузках и провокационных тестах. Так, при сдавлении области запястного канала возможен диффузный безболезненный отек кистей. Кроме того, при РП нередко развивается одно- или двусторонний ладонный апоневрозит, тендовагинит сухожилий сгибателей пальцев и наблюдаются небольшие сгибательные контрактуры пальцев кистей.
Лихорадка у больных РП бывает фебрильной или субфебрильной, но заболевание может протекать без лихорадки. Вместе с тем у некоторых больных длительная лихорадка (недели и даже месяцы) может быть основным или единственным проявлением заболевания, особенно когда оно начинается с ГА. Из общих симптомов встречаются похудание, анорексия, общая слабость. Также нередко возникает депрессия, особенно если больной не находит понимания в лице врача, а назначенная терапия не приносит облегчения.
Выделяют следующие варианты течения РП [2]:
Клинические признаки РП (особенно — характеристика болевого синдрома) очень важны для диагностики, однако ориентироваться только на их проявления нельзя: возможны грубые диагностические ошибки! Осложняет диагностику заболевания при сочетании РП с ГА несвоевременная диагностика последнего, т. к. течение васкулита нередко бывает малосимптомным, скрытым и выявляется лишь при целенаправленном расспросе и осмотре [10].
Среди результатов лабораторных исследований наиболее характерным является резкое стойкое ускорение СОЭ до 50–70 мм/час. Определяются также и другие лабораторные признаки воспаления: отмечается рост С-реактивного белка (СРБ), фибриногена, повышаются белки острой фазы (альфа2- и гамма-глобулины). СРБ является более чувствительным показателем активности заболевания, чем СОЭ. Также маркером активности заболевания служит повышение уровня интерлейкина-6 [4].
Также характерным признаком заболевания является нормохромная анемия, так называемая анемия хронических заболеваний [11].
Подъем трансаминаз, щелочной фосфатазы у части больных РП отражают поражение печени при данном заболевании, что подтверждается результатами биопсии. Изменения в печени не специфичны — выявляют признаки перипортального воспаления, эпителиально-клеточные гранулемы.
В настоящее время диагностические критерии РП выглядят следующим образом.
Еще в 1972 г. В. Hamrin предложил следующие диагностические критерии РП, которые не потеряли актуальность и в наши дни [12]:
Первые 5 критериев считаются обязательными, остальные — дополнительными.
В последнее время критерии представляются в виде аббревиатуры SECRET:
S — Stiffness and pain — скованность и боли;
E — Elderly individuals — пожилой возраст больных;
C — Constitutional symptoms — общие конституциональные симптомы;
R — Arthritis (rheumatism) — артрит;
E — Elevated erythrocyte sedimentation rate (ESR) — повышенная COЭ;
T — Temporal arteritis — височный артериит.
Дифференциальный диагноз РП проводится с рядом заболеваний, протекающих со сходной симптоматикой. В первую очередь с паранеопластическим синдромом: наличие похудания, анорексии, повышения СОЭ у пожилых больных прежде всего заставляет искать неопластический процесс. Мышечная слабость, утренняя скованность, нередко встречающаяся при РП, вполне укладываются в рамки паранеопластического синдрома, поэтому всем больным с такой симптоматикой должен проводиться тщательный онкологический поиск (необходимо исключить опухоль желудка, поджелудочной железы и легких, как наиболее часто проявляющихся схожими паранеопластическими реакциями).
В круг диагностического поиска в ходе обследования следует включить [8]:
Сложности постановки диагноза РП как нозологии возникают еще и в связи с тем, что похожая симптоматика может развиваться при любых хронических бактериальных и вирусных инфекциях, при ряде эндокринопатий, в т. ч. гипотиреозе, при многих аутоиммунных заболеваниях, что даже заставляет некоторых исследователей поднимать вопрос о наличии синдрома РП при других нозологиях [13, 14].
Приведенные выше литературные данные нашли подтверждение в нашей клинической практике и опубликованы в периодической печати. Вместе с тем, несмотря на то, что по данным мировой статистики, в популяции женщины болеют чаще, чем мужчины (соотношение 3:1), оба наших пациента были мужчинами пожилого возраста [15, 16]. И в том, и в другом случае, прежде чем поставить диагноз РП, был проведен большой диагностический поиск, включающий выполнение многих лабораторно-инструментальных методов исследования для исключения заболеваний, сопровождающихся лихорадкой и суставным синдромом.
В связи с частым сочетанием РП и ГА, существует мнение, что они являются синдромами одного и того же заболевания — ГА, однако это лишь гипотеза одиночек. Убедительных данных, подтверждающих эту гипотезу, нет. Вместе с тем, интерес к этому вопросу имеет практическое значение, так как развитие ГА у больных РП значительно ухудшает прогноз и требует назначения более высоких доз кортикостероидов. Поэтому используется тактика динамического наблюдения за больными РП и активного выявления у них симптомов, характерных для ГА, что потребует проведения биопсии височной артерии для подтверждения диагноза ГА с последующей коррекцией терапии.
В 16–21% случаев у пациентов с РП развивается ГА. ГА — гранулематозное воспаление аорты и ее крупных ветвей с поражением экстракраниальных отделов сонной артерии (преимущественно височной). Вместе с тем у 40–60% больных ГА встречается РП [14]. ГА может возникать одновременно с РП, но может предшествовать ей или (чаще!) присоединиться гораздо позднее [4]. Обычно ГА развивается у больных старше 50 лет. Женщины болеют несколько чаще, чем мужчины (соотношение 3:1). ГА страдают почти исключительно люди белой расы. Болезнь чаще встречается в Северной Европе и Америке (особенно среди скандинавских эмигрантов), чем в южных регионах земного шара [17, 18].
В большинстве случаев симптомы заболевания появляются постепенно; реже заболевание начинается остро, когда больные могут четко отметить день и час возникновения болезни.
Клиническая картина ГА складывается из следующих проявлений, включающих лихорадку (субфебрильную и фебрильную), которая нередко, в течение длительного времени, является единственным проявлением болезни, проливные поты, общую слабость, потерю аппетита, снижение массы тела. Поражение суставов при ГА описывается как симметричный серонегативный полиартрит, напоминающий РА у пожилых (вовлекаются преимущественно коленные, лучезапястные, голеностопные суставы), может быть моно- или олигоартрит. Нередко заболевание сопровождается депрессией. Но главным клиническим симптомом ГА являются сосудистые расстройства. Артерии извиты, их стенки уплотнены, при пальпации возможна болезненность по ходу сосуда. Могут наблюдаться синкопальные состояния, которые, как правило, ошибочно трактуют как эпилептиформный синдром вследствие цереброваскулярной болезни у пожилых. Появляется болезненность кожи волосистой части головы, гиперестезии, может быть выпадение волос, боли в языке, затруднения и боли при разговоре, жевании и глотании. Больные могут жаловаться на снижение зрения. Иногда внезапно развивается слепота [19].
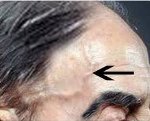
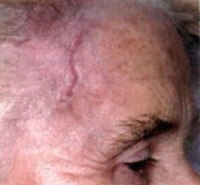
Проявления сосудистых расстройств во многом зависят от локализации процесса в артериальном русле. При поражении височной артерии развивается постоянная острая интенсивная двусторонняя головная боль с преимущественной локализацией в лобной и теменной области. Отмечается набухание, отечность височных артерий, резкая болезненность при касании кожи. При вовлечении в процесс затылочной артерии головная боль локализуется в затылочной области. Если поражены артерии, от которых зависит кровоснабжение глаза и глазных мышц, то развивается нарушение зрения, часто необратимое, которое может быть первым проявлением заболевания. Развитие слепоты — это самое грозное раннее осложнение ГА. Вместе с тем поражение этих артерий может протекать более доброкачественно и сопровождаться конъюнктивитом, эписклеритом, отеком роговицы, снижением зрения и т. д. Если поражена наружная сонная артерия, то развивается отек лица, нарушается глотание и слух. Васкулит верхнечелюстной артерии проявляется нарушением жевания, беспричинной зубной болью, перемежающей «хромотой» языка. Аорта поражается преимущественно в грудном отделе и может сопровождаться развитием аневризмы.
Данные лабораторных исследований не носят специфический характер и подтверждают наличие воспалительного. В анализе крови, помимо увеличения СОЭ, отмечается резко повышенный уровень СРБ и интерлейкина-6 (более 6 пг/мл). Мало помогают диагностике ГА инструментальные исследования (УЗИ, МРТ), т. к. полученные данные не позволяют дифференцировать воспалительные поражения сосудов от атеросклеротических. Для подтверждения диагноза целесообразно проведение биопсии височной артерии, однако признаки артериита обнаруживаются не всегда. Этот процент колеблется от 5% до 50% [20]. Однако отрицательные результаты при биопсии не позволяют полностью исключить этот диагноз, поскольку при ГА нередко наблюдается и очаговое сегментарное поражение сосудов.
Вместе с тем существуют диагностические критерии ГА [21]:
Наличие трех и более любых критериев позволяет поставить диагноз ГА с чувствительностью 93,5% и специфичностью 91,2% [21].
Таким образом, ГА должен быть заподозрен у всех больных, особенно у женщин, старше 50 лет с выраженными головными болями, нарушением зрения, выраженным увеличением СОЭ, часто анемией, а также с перемежающей хромотой в сочетании с ишемической болезнью сердца (ИБС), нередко — с признаками РП.
Дифференциальную диагностику ГА, также как и при РП, проводят с широким спектром заболеваний, протекающих с поражением крупных сосудов (в том числе атеросклеротическим). Если ГА сочетается с РП, то в круг заболевания, с которым приходится его дифференцировать, входят все воспалительные заболевания суставов у пожилых, плечелопаточный периартериит, воспалительные миопатии и т. п.
Целью проводимого лечения РП и ГА является достижение ремиссии, а в дальнейшем выздоровления.
Единственное эффективное средство для лечения этих заболеваний — глюкокортикостероиды. Лечение РП осуществляется, как правило, преднизолоном. Больные «оживают» уже на следующий день после приема небольших доз преднизолона, а через 2–4 недели наступает клинико-лабораторная ремиссия заболевания. Стандартная доза преднизолона — 15 мг/сут, причем она должна распределяться равномерно по 5 мг на 2–3 приема в день [22]. Альтернирующая схема (прием препарата через день) для лечения этого заболевания не подходит, так как эффекта терапии не наблюдается. Назначение преднизолона обязательно и должно осуществляться сразу при постановке диагноза, что снизит риск присоединения ГА. При сочетании РП + ГА требуются значительно большие дозы кортикостероидов. Из других лекарственных препаратов рекомендуется только те, которые предупреждают осложнения глюкокортикоидной терапии — гипокалиемии, остеопороза, артериальной гипертонии, стероидных язв желудка, стероидной миопатии, сахарного диабета, катаракты и др.
Ремиссию удается достичь через 2–3 недели, а затем подобранная доза должна сохраняться еще в течение месяца. У подавляющего большинства больных кортикостероидная терапия длится 2–3 года. Достижение ремиссии — это первый этап лечения. После развития ремиссии подавляющую дозу преднизолона сохраняют не менее одного месяца [23].
Второй этап лечения — постепенное снижение дозы преднизолона — производится очень медленно (!), на 1/4 таблетки с интервалом приблизительно в 14 дней под контролем СОЭ. Малейшие признаки обострения РП заставляют вернуться к предыдущей дозе гормона, то есть темп снижения дозы должен быть индивидуальным (подбор поддерживающей терапии РП кортикостероидами называют искусством). Отмена глюкокортикоидов возможна в среднем через год, редко — через 6 месяцев, если не возникали обострения. Однако некоторые больные вынуждены принимать преднизолон до 3–10 лет. Оптимальная поддерживающая доза 5 мг/сут (осложнения минимальны).
Попытка применения гидроксихлорохина, метотрексата, азатиоприна и циклоспорина для лечения РП оказалась неуспешной, либо полученные результаты противоречивы.
По последним данным проведенного в 2007 в Италии и США исследования, добавление к терапии кортикостероидами инфликсимаба (моноклональные антитела к фактору некроза опухоли альфа (ФНО-альфа)) не оказывает никакого положительного влияния, не предотвращает рецидивы заболевания, не позволяет уменьшить дозу кортикостероидов [7].
Единичные исследования показали, что комбинированное применение преднизолона и этанерцепта (блокатор рецепторов ФНО-альфа) является эффективным и безопасным и позволяет уменьшить дозу преднизолона [23].
Лечение ГА следует начинать немедленно для предотвращения развития слепоты и поражений внутренних органов. При лечении ГА доза преднизолона колеблется от 40 до 60 мг в сутки, выдается в несколько приемов и продолжается до нормализации СОЭ и исчезновения симптомов. Снижать дозу преднизолона по половине таблетки рекомендуют каждые 2 недели до достижения дозы 20 мг в сутки. Затем дозу снижают лишь на 10% каждые 2 недели до дозы 10 мг в сутки. И лишь потом по 1 мг через день или (ежедневно) каждые 4 недели. В процессе снижения дозы преднизолона необходимо тщательно наблюдать за динамикой симптомов и контролировать СОЭ каждые 4 недели (хотя бы в первые 2–3 мес).
При тяжелом течении ГА первоначальные дозы глюкокортикоидов следует увеличить до 60–80 мг в сутки или провести пульс-терапию (метилпреднизолон по 1 г в течение трех дней) с последующим переходом на поддерживающую дозу преднизолона 20–30 мг в сутки, принимаемого внутрь.
Комбинация преднизолона с метатрексатом, азатиоприном возможна и способствует уменьшению дозы преднизолона [24, 25]. Эффективность монотерапии метатрексатом и циклоспорином А не доказана [25, 27].
Из средств дополнительной терапии рекомендуют прием ацетилсалециловой кислоты (75–150 мг) с целью снижения риска слепоты и цереброваскулярных осложнения.
Длительность терапии индивидуальна у каждого пациента. Критерием является отсутствие клинических проявлений ГА после шестимесячной терапии преднизолоном в дозе 2,5 мг в сутки.
При изолированной РП (без ГА) прогноз для жизни благоприятный; при наличии темпорального васкулита прогноз всегда сомнительный. При снижении дозы преднизолона возможны рецидивы артериита с наступлением слепоты; васкулит может привести к внезапной смерти вследствие стеноза и окклюзии церебральных, коронарных артерий, аневризмы аорты. В ряде случаев ГА, хотя и имеет длительное течение, заканчивается выздоровлением.
Литература
За остальным списком литературы обращайтесь в редакцию.
С. И. Овчаренко, доктор медицинских наук, профессор
И. С. Щендрина, кандидат медицинских наук
М. П. Троицкая
Первый МГМУ им. И. М. Сеченова, Москва
Болезнь Хортона
Гигантоклеточный темпоральный артериит (болезнь Хортона) — воспалительное заболевание (васкулит) с аутоиммунным механизмом развития, поражающее преимущественно крупные и средние интра- и экстракраниальные сосуды. Наиболее часто наблюдается воспаление сосудистой стенки ветвей наружной сонной артерии. Диагностика болезни Хортона включает клиническое и неврологическое обследование пациента, оценку лабораторных данных, состояния органа зрения и результатов биопсии височной артерии, проведение УЗДГ, МРТ и КТ головного мозга. Лечение болезни Хортона состоит из начальной и поддерживающей терапии глюкокортикоидами. Оно проводится в течение двух лет и может быть отменено только в случае отсутствия рецидивов.
Общие сведения
Болезнь Хортона носит свое название по имени американского врача Хортона, впервые описавшего ее в 1932 году. Второе название — темпоральный (височный) артериит — заболевание получило в связи с тем, что в большинстве случаев оно протекает с поражением височной артерии. Клиническая ревматология включает болезнь Хортона в группу системных васкулитов, к которой также относятся болезнь Такаясу, узелковый периартериит, болезнь Кавасаки, гранулематоз Вегенера.
Болезнь Хортона чаще встречается в странах Северной Европы и Скандинавии, где заболеваемость составляет 15-35 человек на 100000. Значительно ниже заболеваемость в азиатских, арабских странах и Японии, где она составляет 1,47 на 100000 человек. Наиболее подвержены развитию болезни Хортона люди пожилого возраста (после 50 лет), пик заболеваемости приходится на возрастную группу около 70 лет. Женщины болеют болезнью Хортона чаще мужчин. На 3 заболевших мужчин приходится примерно 5 женщин.
Причины возникновения болезни Хортона
Ведущим механизмом в развитии болезни Хортона считается нарушение иммунной реакции по типу аутоиммунного процесса. В подтверждение этого у многих заболевших выявляются антитела к иммуноглобулинам М и А, наблюдается отложение циркулирующих иммунных комплексов в эластическом слое сосудистой стенки пораженной артерии.
В качестве провоцирующих факторов болезни Хортона предположительно указываются инфекционные агенты, в основном вирусы (вирусный гепатит, грипп, герпес). У 33% пациентов с болезнью Хортона в крови выявляются Hbs-антигены и антитела к ним, Hbs-антиген нередко обнаруживается и в стенках пораженных артерий. Выявленное во многих случаях болезни Хортона носительство генов HLA В14, А10, В8 подтверждает мнение большинства авторов о существовании генетической предрасположенности к развитию заболевания.
Симптомы болезни Хортона
Проявления болезни Хортона могут возникать постепенно на протяжении нескольких недель. В других случаях, как правило, после перенесенного ОРВИ или другой вирусной инфекции, наблюдается острое начало. Составляющими типичной клинической картины болезни Хортона являются: общая симптоматика, сосудистые проявления и поражение органа зрения.
Общие симптомы болезни Хортона включают достигающую фебрильных цифр лихорадку, интенсивную головную боль, анорексию, снижение массы тела, повышенную утомляемость, нарушение сна, артралгии и миалгии. Головная боль при болезни Хортона может быть одно- или двусторонней, имеет пульсирующий тупой характер и зачастую височную локализацию, усиливается ночью и нарастает в течение 2-3 недель. Она может сопровождаться болезненностью кожи головы, острыми болями и онемением в области лица, болью при жевании. Миалгии, как правило, захватывают мышцы плечевого и тазового пояса. Их симптоматика сходна с ревматической полимиалгией.
Сосудистые проявления болезни Хортона выражаются в уплотнении и болезненности при прощупывании теменных и височных артерий, часто наблюдается отсутствие их пульсации. При пальпации волосистой части головы выявляются узелки. Нередко при осмотре пациента с болезнью Хортона обнаруживается отечность и покраснение кожи в височной области. Поражения отдельных ветвей внутренней сонной артерии проявляются приступами транзиторных ишемических атак или ишемическим инсультом соответствующего участка головного мозга. В редких случаях болезни Хортона наблюдаются поражения других крупных артерий, характеризующиеся соответствующей симптоматикой. Они могут приводить к развитию перемежающейся хромоты и инфарктов соматических органов, в том числе инфаркта миокарда.
Поражения органа зрения при болезни Хортона проявляются двоением предметов (диплопия), болью в глазном яблоке, приходящим нарушением четкости зрения. Пациенты жалуются на то, что иногда видят «размытую» или «затуманенную» картину окружающего. Эти симптомы связаны с происходящим при типичном течении болезни Хортона нарушением кровоснабжения зрительного нерва и развитием его ишемической невропатии, которая в конечном итоге может привести к снижению зрения и слепоте. Необратимые изменения зрительного нерва обычно формируются спустя несколько месяцев после начала болезни Хортона, поэтому своевременно начатое лечение позволяет их избежать.
Диагностика болезни Хортона
Совокупность клинических признаков, характерный возраст пациентов, лабораторные данные, результаты биопсии височной артерии, заключения окулиста и невролога в большинстве случаев позволяют своевременно диагностировать болезнь Хортона. Положительный эффект глюкокортикостероидной терапии также говорит в пользу правильно поставленного диагноза.
Клинический анализ крови при болезни Хортона обычно выявляет гипохромную анемию, лейкоцитоз и значительное ускорение СОЭ (50-70мм/ч), в биохимическом анализе крови характерна диспротеинемия с уменьшением количества альбуминов, повышение Ig G. На консультации окулиста проводят определение остроты зрения и осмотр глазного дна. Для выявления сосудистых нарушений головного мозга производят неврологический осмотр пациентов с болезнью Хортона, УЗГД экстракраниальных сосудов и глазных сосудов, КТ и МРТ головного мозга, ангиографию сосудов головного мозга.
Гистологическое исследование материалов биопсии височной артерии выявляет характерные для болезни Хортона изменения в виде утолщения внутреннего и среднего слоя сосудистой стенки; образования в стенке сосуда гранулем и скоплений гигантских клеток, лимфоцитарных инфильтратов; пристеночного тромбоза; сужения просвета пораженного сосуда. Однако отсутствие характерной гистологической картины при наличии типичных клинических симптомов не исключает диагноз болезни Хортона. Это связано с тем, что поражение артерии носит сегментарный характер и в ходе биопсии возможно взятие непораженного участка артерии. Дифференциальная диагностика болезни Хортона проводится с ревматической полимиалгией, мигренью, болезнью Такаясу, фибромиалгиями.
Американской Ревматологической Ассоциацией разработаны диагностические критерии болезни Хортона, специфичность которых по мнению авторов достигает 91,2%. К ним относятся: возраст заболевших старше 50 лет; возникновение характерной головной боли; не связанные с атеросклерозом изменения височной артерии (уплотнение, снижение пульсации, болезненность); показатели СОЭ более 50 мм/ч; типичная гистологическая картина при биопсии височной артерии. Диагноз болезни Хортона ставится в случае наличия 3 из 5 указанных признаков.
Лечение и прогноз болезни Хортона
Терапия болезни Хортона осуществляется преимущественно глюкокортикоидными гормонами. Начальная терапия проводится преднизолоном, доза которого зависит от наличия поражений крупных артерий и осложнений со стороны зрения. Острое возникновение нарушений зрения является показанием для пульс-терапии высокими дозами метилпреднизолона. Постепенное снижение дозы препарата при болезни Хортона может быть начато не ранее, чем через месяц от начала терапии. Еженедельно снижая дозировку преднизолона на 10%, постепенно переходят на поддерживающую дозу. В среднем лечение болезни Хортона продолжается 2 года и может быть отменено при отсутствии признаков заболевания в течении полугода на фоне поддерживающей терапии преднизолоном.
При отсутствии ожидаемого эффекта глюкокортикоидной терапии или из-за наличия выраженных побочных эффектов при ее проведении переходят на лечение цитостатиками (циклофосфамид, метотрексат). В качестве симптоматической терапии болезни Хортона возможно применение противовоспалительных препаратов, антикоагулянтов и вазодилятаторов.
Прогноз для жизни у пациентов с болезнью Хортона благоприятный. Как правило, заболевание хорошо поддается лечению. Однако возможна потеря зрения, артериальные тромбозы и возникновение осложнений в связи с проводимой глюкокортикоидной терапией.