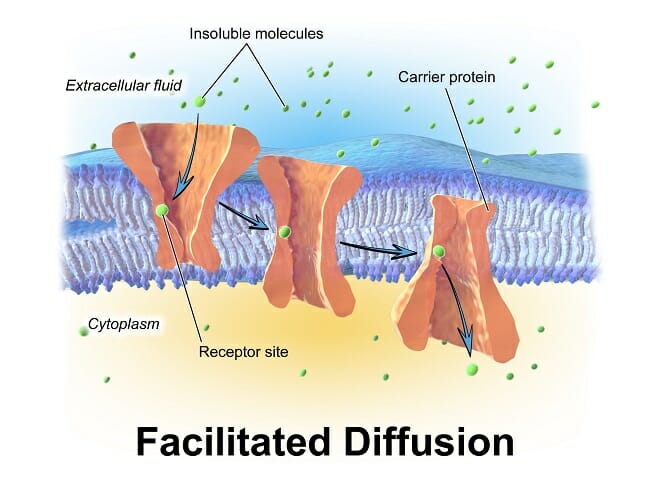
Что влияет на скорость диффузии
Digitrode
цифровая электроника вычислительная техника встраиваемые системы
Четыре фактора, которые влияют на скорость диффузии
Диффузия происходит из-за случайного движения частиц. Это обычно происходит из-за градиента концентрации, что означает, что молекулы перемещаются из области высокой концентрации в область более низкой концентрации.
Пример показан на изображении выше. Когда краситель добавляется в раствор, он со временем диффундирует. Сначала вы видите полосы синего цвета, проходящие через раствор, пока, наконец, весь раствор не станет синим, потому что концентрация красителя везде одинакова. В этот момент, хотя молекулы красителя все еще движутся, вы не сможете их почувствовать, поскольку синий краситель рассеял и окрасил весь объем жидкости.
Диффузия, таким образом, является пассивным процессом (это означает, что он не требует затрат энергии). Вещество перемещается из области высокой концентрации в область более низкой концентрации. Это движение продолжается до тех пор, пока концентрация вещества не выровняется. Как только концентрация выровняется, вещество все еще движется, но больше не будет иметь градиент концентрации. Это состояние называется динамическим равновесием.
Молекулы постоянно движутся вокруг из-за количества тепловой энергии, которую они имеют. Это движение зависит от размера частицы и среды, в которой она находится. Частицы всегда будут перемещаться в среде, но на общую скорость диффузии могут влиять многие факторы.
Концентрация: диффузия молекул полностью зависит от перемещения из области с более высокой концентрацией в область с более низкой концентрацией. Другими словами, диффузия происходит вниз по градиенту концентрации рассматриваемой молекулы. Если разница в концентрации выше, то молекулы будут снижаться градиент концентрации быстрее. Если разница в концентрации не так велика, молекулы не будут двигаться так быстро, и скорость диффузии уменьшится.
Температура: частицы движутся из-за кинетической энергии, связанной с ними. По мере повышения температуры кинетическая энергия, связанная с каждой частицей, также увеличивается. В результате частицы будут двигаться быстрее. Если они могут двигаться быстрее, то они также могут распространяться быстрее. И наоборот, когда кинетическая энергия, связанная с молекулами, уменьшается, их движение уменьшается. В результате скорость диффузии будет ниже.
Масса частиц: более тяжелые частицы будут двигаться медленнее и, следовательно, будут иметь меньшую скорость диффузии. С другой стороны, более мелкие частицы будут диффундировать быстрее, потому что они могут двигаться быстрее. Как и все ключевые факторы, влияющие на диффузию, движение частицы имеет первостепенное значение при определении замедления или ускорения диффузии.
Свойства растворителя: вязкость и плотность сильно влияют на диффузию. Если среда, через которую должна распространяться данная частица, является очень плотной или вязкой, то частице будет труднее диффундировать через нее. Так что скорость диффузии будет ниже. Если среда менее плотная или менее вязкая, частицы смогут двигаться быстрее и быстрее диффундировать.
Все факторы, влияющие на диффузию, могут иметь комбинированный эффект. Например, маленький ион может диффундировать быстрее через вязкий раствор, чем большая молекула сахара. Ион имеет меньший размер и поэтому может двигаться быстрее. Большая молекула сахара движется медленнее из-за своего размера. Вязкость раствора влияет на оба, но усугубит замедленную диффузию, которой подвергается большая молекула
Скорость диффузии
Вы будете перенаправлены на Автор24
Скорость диффузии
Диффузия относится к наиболее простым явлениям, которые изучаются в рамках курса физики. Этот процесс можно представить на бытовом ежедневном уровне.
Диффузия представляет собой физический процесс взаимного проникновения атомов и молекул одного вещества между такими же структурными элементами другого вещества. Итогом этого процесса становится выравнивание уровня концентрации в проникающих соединениях. Диффузию или смешивание можно видеть каждое утро на собственной кухне, когда происходит приготовление чая, кофе или иных напитков, в состав которых входит несколько основных компонентов.
Подобный процесс первый раз смог научно описать Адольф Фик в середине 19 века. Он дал ему оригинальное название, которое переводится с латинского языка как взаимодействие или распространение.
Скорость диффузии зависит от нескольких факторов:
В различных газах, где существуют очень большие расстояние между молекулами, скорость диффузии будет самой большой. В жидкостях, где расстояние между молекулами заметно меньше, скорость также уменьшает свои показатели. Самая маленькая скорость диффузии отмечается в твердых телах, поскольку в молекулярных связях наблюдается строгий порядок. Атомы и молекулы сами совершают незначительные колебательные движения на одном месте. Скорость протекания диффузии увеличивается при росте окружающей температуры.
Закон Фика
Скорость диффузии принято измерять количеством вещества, которое переносится за единицу времени. Все взаимодействия должны осуществляться через площадь поперечного сечения раствора.
Основной формулой скорости диффузии является:
Готовые работы на аналогичную тему
Такую формулу представил в виде математического описания Фик.
Согласно ей, скорость диффузии прямо пропорциональна градиенту концентрации и площади, через которую осуществляется процесс диффузии. Коэффициент пропорциональности определяет диффузию вещества.
Известный физик Альберт Эйнштейн вывел уравнения для коэффициента диффузии:
$D=RT/NA \cdot 1/6\pi\etaŋr$, где:
Из этих уравнений следует, что скорость диффузии будет возрастать:
Скорость диффузии уменьшается:
Если молярная масса увеличивается, тогда коэффициент диффузии уменьшается. В этом случае скорость диффузии также уменьшается.
Ускорение диффузии
Существуют различные условия, которые способствуют ускорению протекания диффузии. Быстрота диффузии зависит от агрегатного состояния исследуемого вещества. Большая плотность материала замедляет химическую реакцию. На скорость взаимодействия молекул влияет температурный режим. Количественной характеристикой скорости диффузии является коэффициент. В системе измерений СИ его обозначают в виде латинской большой буквы D. Он измеряется в квадратных сантиметрах или метрах на секунду времени.
Коэффициент диффузии равняется количеству вещества, которое распределяется среди другого вещества через определенную единицу поверхности. Взаимодействие должно осуществляться на протяжении единицы времени. Для эффектного решения задачи необходимо добиться условия, когда разность плотностей на обеих поверхностях будет равна единице.
Также на скорость диффузии в твердых телах, жидкости в газах влияет давление и излучение. Излучение может быть разных видов, в том числе индукционное, а также высокочастотное. Диффузия начинается при воздействии определенного вещества-катализатора. Они часто выступают в роли пускового механизма для возникновения стабильного процесса рассеивания частиц.
При помощи уравнения Аррениуса описывают зависимость коэффициента от температуры. Оно выглядит следующим образом:
Формула позволяет больше понять о характерных чертах всего процесса диффузии и определяет скорость реакции.
Специальные методы диффузии
Сегодня практически нельзя применить обычные методы для определения молекулярного веса белков. Они обычно основаны на измерении:
Для эффективного решения задачи применяются специальные методы, которые разработаны для исследования веществ с высокой молекулярной структурой. Они предполагают определение скорости диффузии или вязкости растворов.
Метод определения ориентации и формы пор по скорости диффузии основан на исследовании скоростей диализа. В мембране должна происходить в этот момент свободная диффузия.
Также для определения скорости диффузии натрия могут применяться различные радиоизотопы. Такой специальный метод применяется для решения поставленных задач в сфере минералогии и геологии.
Активно применяется метод диффузии, который основан на определении диффузии макромолекул в растворе. Он был разработан для полимерных материалов. Согласно методу, идет определение коэффициента диффузии, а затем по этим данным узнают среднемассовую молекулярную массу.
В настоящее время отсутствуют прямые методы определения скорости диффузии водорода в катализаторе. Для этого используется так называемый второй путь активации.
Для определения скорости принято использовать специальные приборы. Они отличаются по виду от поставленных практических и научных задач.
Диффузия – определение, примеры и типы
Определение диффузии
Диффузия – это физический процесс, который относится к чистому перемещению молекул из области высокой концентрации в область с более низкой концентрацией. Материал, который диффундирует, может быть твердым, жидким или газообразным. Точно так же среда, в которой происходит диффузия, также может находиться в одном из трех физических состояний.
Одной из основных характеристик диффузии является движение молекул вдоль градиент концентрации, Хотя это может быть облегчено другими молекулами, в нем напрямую не участвуют молекулы высоких энергий, такие как аденозинтрифосфат (АТФ) или гуанозинтрифосфат (ГТФ).
Скорость диффузии зависит от характера взаимодействия среды и материала. Например, газ очень быстро диффундирует в другой газ. Примером этого является то, как вредный запах газообразного аммиака распространяется в воздухе. Аналогичным образом, если емкость с жидким азотом протекает незначительно, выделяющийся азот быстро диффундирует в атмосферу. Тот же газ будет диффундировать немного медленнее в жидкости, такой как вода, и медленнее в твердом.
Аналогично, две смешиваемые жидкости также будут диффундировать друг в друга, образуя однородную решение, Например, когда вода смешивается с глицерин Со временем две жидкости диффундируют в радиальном направлении друг к другу. Это может даже наблюдаться визуально путем добавления красителей разного цвета к каждой из жидкостей. Однако это же явление не наблюдается, когда смешиваются несмешивающиеся жидкости, такие как бензин и вода. Диффузия происходит медленно и только по небольшой поверхности взаимодействия двух жидкостей.
Примеры диффузии
Диффузия является важной частью многих биологических и химических процессов. В биологических системах диффузия происходит в любой момент, через мембраны в каждом клетка а также через тело.
Например, кислород находится в более высокой концентрации внутри артерий и артериол по сравнению с уровнями кислорода в активно дышащих клетках. Тем временем кровь течет в капилляры в мускул или печень например, существует только один слой клеток, отделяющий этот кислород от гепатоцитов или скелетная мышца волокна. Через процесс пассивной диффузии, без активного участия каких-либо других молекула кислород проходит через капиллярную мембрану и проникает в клетки.
Клетки используют кислород в митохондрии за аэробного дыхания, который генерирует углекислый газ в качестве побочного продукта. Еще раз, когда концентрация этого газа увеличивается внутри клетки, он диффундирует наружу в направлении капилляров, где сила текущей крови удаляет избыток газа из ткань область. Таким образом, капилляры остаются с низкой концентрацией углекислого газа, что позволяет постоянное движение молекулы от клеток.
Этот пример также показывает, что диффузия любого одного материала не зависит от диффузии любых других веществ. Когда кислород движется к тканям из капилляров, углекислый газ попадает в кровоток.
В химических процессах диффузия часто является центральным принципом, определяющим многие реакции. В качестве простого примера, несколько кристаллов сахара в стакане воды будут медленно растворяться со временем. Это происходит из-за чистого движения молекул сахара в водной среде. Даже в крупных промышленных реакциях, когда две жидкости смешиваются вместе, диффузия объединяет реагенты и позволяет реакции протекать гладко. Например, одним из способов синтеза полиэфира является смешивание подходящей органической кислоты и спирта в их жидкой форме. Реакция протекает, когда два реагента диффундируют друг к другу и подвергаются химической реакции с образованием сложных эфиров.
Факторы, влияющие на диффузию
На диффузию влияют температура, площадь взаимодействия, крутизна градиента концентрации и размер частиц. Каждый из этих факторов, независимо и совместно, может изменять скорость и степень распространения.
температура
В любой системе молекулы движутся с определенным количеством кинетической энергии. Обычно это не направлено каким-либо особым образом и может показаться случайным. Когда эти молекулы сталкиваются друг с другом, происходит изменение направления движения, а также изменения импульса и скорости. Например, если блок из сухого льда (двуокись углерода в твердой форме) помещен в коробку, молекулы углекислого газа в центре блока в основном сталкиваются друг с другом и задерживаются в твердой массе. Однако для молекул на периферии быстро движущиеся молекулы в воздухе также влияют на их движение, позволяя им диффундировать в воздух. Это создает градиент концентрации, при котором концентрация углекислого газа постепенно уменьшается по мере удаления от комка сухого льда.
С увеличением температуры кинетическая энергия всех частиц в системе увеличивается. Это увеличивает скорость, с которой растворенное вещество а также растворитель молекулы движутся, и увеличивает столкновения. Это означает, что сухой лед (или даже обычный лед) будет испаряться быстрее в более теплый день просто потому, что каждая молекула движется с большей энергией и с большей вероятностью быстро выйдет за пределы твердого состояния.
Область взаимодействия
Чтобы расширить приведенный выше пример, если блок сухого льда разбивается на несколько частей, площадь, которая взаимодействует с атмосферой, немедленно увеличивается. Количество молекул, которые только сталкиваются с другими частицами углекислого газа в сухом льде, уменьшается. Следовательно, скорость диффузии газа в воздух также увеличивается.
Это свойство можно наблюдать даже лучше, если газ имеет запах или цвет. Например, когда йод сублимируется над горячей плитой, начинают появляться фиолетовые пары и смешиваться с воздухом. Если сублимацию проводят в узком тигле, пары медленно диффундируют к устью контейнера, а затем быстро исчезают. Хотя они ограничены меньшей площадью поверхности внутри тигля, скорость диффузии остается низкой.
Это также видно, когда два жидких реагента смешаны друг с другом. Перемешивание увеличивает площадь взаимодействия между двумя химическими веществами и позволяет этим молекулам быстрее диффундировать друг к другу. Реакция идет к завершению с более высокой скоростью. Аналогичным образом, любое растворенное вещество, которое разбивается на мелкие кусочки и смешивается с растворителем, быстро растворяется, что является еще одним показателем того, что молекулы лучше диффундируют при увеличении площади взаимодействия.
Крутизна градиента концентрации
Поскольку диффузия обусловлена, главным образом, вероятностью того, что молекулы отойдут от области с более высоким насыщением, из этого сразу следует, что когда среда (или растворитель) имеет очень низкую концентрацию растворенного вещества, вероятность диффузии молекулы от центральной области выше. Например, в примере с диффузией газообразного йода, если тигель помещают в другой закрытый контейнер и кристаллы йода нагревают в течение продолжительного периода времени, скорость, с которой фиолетовый газ, по-видимому, «исчезает» в устье тигель уменьшится. Это очевидное замедление связано с тем, что со временем в более крупном контейнере начинает появляться достаточное количество йодного газа, и часть его будет перемещаться «назад» к тиглю. Даже при том, что это случайное ненаправленное движение с большим объемом, оно может создать сценарий, в котором нет чистого движения газа из контейнера.
Размер частицы
При любой данной температуре диффузия частицы меньшего размера будет более быстрой, чем диффузия молекулы большего размера. Это связано как с массой молекулы, так и с площадью ее поверхности. Более тяжелая молекула с большей площадью поверхности будет диффундировать медленно, в то время как более мелкие, более легкие частицы будут диффундировать быстрее. Например, в то время как газообразный кислород будет диффундировать немного быстрее, чем диоксид углерода, оба они будут двигаться быстрее, чем газообразный йод.
Функции диффузии
Диффузия в организме человека необходима для поглощения усваиваемых питательных веществ, газообмена, распространения нервных импульсов, движения гормонов и других метаболитов к их цели. орган и почти для каждого события в эмбриональном развитии.
Типы диффузии
Диффузия может быть простая диффузия и быть облегчен другой молекулой
Простая диффузия
Простая диффузия – это просто движение молекул вдоль градиента их концентрации без непосредственного участия каких-либо других молекул. Это может включать в себя либо распространение материала через среду, либо перенос частицы через мембрану. Все приведенные выше примеры были примерами простой диффузии.
Простая диффузия важна в химических реакциях, во многих физических явлениях и может даже влиять на глобальные погодные условия и геологические события. В большинстве биологических систем диффузия происходит через полупроницаемую мембрану из липидный бислой, Мембрана имеет поры и отверстия для прохождения определенных молекул.
Облегченная диффузия
Поскольку они представляют собой относительно большие отверстия в плазматической мембране, эти интегральные мембранные белки также обладают высокой специфичностью. Например, канальный белок который транспортирует ионы калия, имеет гораздо более высокое сродство к этому иону, чем очень похожий ион натрия, с почти таким же размером и зарядом.
викторина
1. Какое из этих утверждений о диффузии молекул верно?A. Облегченная диффузия полностью обеспечивается гидролизом ГТФB. Никогда не нуждается в присутствии какой-либо другой молекулыC. Диффузия каждой молекулы зависит от градиента ее концентрации и не зависит от концентрации других молекул вид в средеD. Все вышеперечисленное
Ответ на вопрос № 1
С верно. На движение одной молекулы вдоль градиента концентрации не влияют градиенты концентрации любых других веществ в той же среде.
2. Если бы в устье тигля, нагревавшего йод, находилась охлаждающая жидкость, как это повлияло бы на скорость ее диффузии?A. Останется без измененийB. УвеличениеC. УменьшитьD. Это будет зависеть от характера и температуры охлаждающей жидкости
Ответ на вопрос № 2
С верно. Присутствие охлаждающей жидкости в устье тигля понизит температуру газообразного йода. Это уменьшит скорость диффузии.
3. Какое из этих утверждений не соответствует действительности?A. Большие полярные молекулы не могут диффундировать через биологическую мембрануB. Диоксид углерода будет диффундировать быстрее, чем газообразный бромC. Интегральные мембранные белки, которые облегчают диффузию, очень специфичны в отношении своего грузаD. Все вышеперечисленное
Ответ на вопрос № 3
верно. Полярные молекулы могут диффундировать через мембраны, но им необходимо присутствие трансмембранного канала или белка. Углекислый газ легче брома и поэтому быстрее диффундирует.
Факторы, влияющие на скорость диффузии
На скорость диффузии оказывают влияние такие факторы, как температура; тип примесных атомов и среда, в которой они диффундируют; наличие дефектов кристаллической решетки; концентрация вводимой примеси и концентрация примеси, уже имеющейся в пластине. С повышением температуры скорость диффузии возрастает, поскольку увеличивается вероятность перескока примесного атома из одного положения в другое, причем зависимость эта примерно экспоненциальная.
Тип атомов также влияет на скорость диффузии, поскольку для разных атомов различны энергия активации диффузии и, что более важно, может быть различен и сам механизм диффузии. Как уже отмечалось, примесные атомы, диффундирующие по вакансионному механизму, имеют значительно более низкий коэффициент диффузии, чем атомы, диффундирующие по междоузлиям.
Влияние дефектов кристаллической структуры на скорость диффузии примесных атомов обусловлено тем, что дефекты создают вокруг себя механические напряжения, способствующие образованию вакансий. Это, в свою очередь, увеличивает скорость диффузии атомов, перемещающихся по вакансионному механизму.
Влияние концентрации примесных атомов (вводимых в пластину или уже имеющихся в ней) обусловлено тем, что при высоких температурах практически все они находятся в ионизированном состоянии: доноры становятся положительно заряженными ионами, акцепторы – отрицательно заряженными. Если, например, пластина была легирована донорами, а в нее вводятся акцепторы, то за счет дополнительного воздействия электрического поля доноров ионы-акцепторы будут диффундировать быстрее. Если же пластина была легирована донорами, а в нее вводятся снова доноры, то их скорость диффузии из-за электрического поля будет меньше.
На скорость диффузии влияет и концентрация самой вводимой в пластину примеси, причем это влияние проявляется заметно лишь при условии, что концентрация вводимой примеси превышает собственную концентрацию свободных носителей заряда в полупроводнике. Если, например, вводятся доноры, то, как уже отмечалось, в кристаллической решетке они ионизируются с образованием свободных электронов и положительно заряженных ионов-доноров. Электроны являются значительно более подвижными частицами, поэтому они быстро диффундируют в глубь кристалла и создают электрическое поле, действующее на ионы-доноры. В результате эффективный коэффициент диффузии донорных примесных атомов возрастает. Разумеется, данный эффект заметно проявляется только тогда, когда дополнительное увеличение свободных электронов в кристалле превышает количество собственных носителей.
Формирование структур методом ионной имплантации
Сущность метода и отличительные особенности
Ионная имплантация – это управляемое введение примесных атомов в поверхностный слой подложки путем бомбардировки ее ионами с энергией от нескольких килоэлектрон-вольт до нескольких мегаэлектрон-вольт (обычно от 20 кэВ до 100 кэВ). Процесс ионного легирования осуществляют для модификации свойств (в первую очередь электрофизических) поверхностного слоя. Избирательность процесса легирования обеспечивается либо сканированием остросфокусированного ионного пучка по заданной программе, либо перемещением широкого ленточного пучка по предварительно маскированной поверхности.
Ионы при движении в подложке сталкиваются с атомами подложки и выбивают их из своих узлов. В результате вдоль траектории движения имплантированных ионов образуются многочисленные вакансии и междоузельные атомы, то есть создаются радиационные дефекты. Когда плотность пучка ионов превышает некоторое критическое значение, может образоваться сплошной аморфный слой. В результате столкновений ионов с атомами мишени они теряют свою энергию и, в конечном итоге, останавливаются (обычно в междоузлиях). Для того чтобы внедренные таким образом атомы смогли выполнить свои функции доноров или акцепторов, их необходимо перевести из междоузлий в узлы кристаллической решетки. Это осуществляют с помощью термического отжига. Другой важной задачей отжига является устранение возникших радиационных дефектов и восстановление исходной кристаллической структуры. Температура и продолжительность отжига определяется тем, насколько сильно нарушена кристаллическая структура подложки.
Метод ионного легирования имеет ряд преимуществ по сравнению с методом диффузии. Во-первых, этот метод универсален, так как с его помощью можно вводить любые примеси в любое твердое тело. Во-вторых, он обеспечивает высокую чистоту легирования, практически исключающую попадание неконтролируемых примесей в легированный слой. В-третьих, ионное легирование проводится при низких температурах (вплоть до комнатных), что позволяет использовать в качестве масок слои из фоторезиста. В-четвертых, данный метод легирования гораздо более управляем, чем метод диффузии. Изменяя плотность пучка ионов и их энергию, можно в достаточно широких пределах варьировать количество имплантированных примесных атомов и глубину их залегания.
Серьезным ограничением метода является малая глубина проникновения ионов в подложку и, вследствие этого, малая глубина залегания р-п-переходов. Это затрудняет выполнение последующих технологических операций и предъявляет высокие требования к качеству поверхности исходной подложки. Есть проблемы с легированием пластин большого диаметра из-за расфокусировки ионного пучка при больших отклонениях его от нормали. Радиационные дефекты хотя и устраняются в значительной степени отжигом, тем не менее оставшаяся часть может негативно сказаться на работе полупроводниковых приборов.
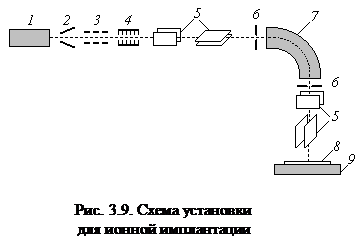
Наличие в установке для ионной имплантации магнитного сепаратора обеспечивает высокую чистоту легирования. Принцип действия сепаратора основан на взаимодействии магнитного поля, созданного в сепараторе, с движущимися ионами. В результате действия силы Лоренца ионы движутся по дуге окружности, радиус Rкоторой определяется выражением
Физические основы метода. Распределение имплантированных ионов
Дата добавления: 2018-05-12 ; просмотров: 2354 ; Мы поможем в написании вашей работы!