Что влияет на днк человека
Код жизни. Что такое ДНК и как она влияет на жизнь человека
25 апреля – Международный день ДНК
Обо всём, что вы хотели и не хотели знать про эти три буквы, «ОнОнас» спросил у доктора медицинских наук профессора БелГУ Михаила Чурносова.
Что такое ДНК?
Мы знаем, что внешность человека, привычки и некоторые заболевания передаются по наследству. Информация о живом существе закодирована в генах, и носителем всех генов человека или животного является ДНК – дезоксирибонуклеиновая кислота.
Молекула ДНК – одна из трёх основных, которые содержат информацию обо всех генетических характеристиках. Другие – это РНК и белки. По сути ДНК – это длинная молекула, состоящая из структурных элементов – нуклеотидов. Чтобы понять, что такое ДНК, лучше представлять не химическое соединение, а программный код, в языке которого всего четыре буквы: А (аденин), Т (тимин), Г (гуанин) и Ц (цитозин). В этом коде записано, когда, сколько и каких белков будет произведено в нашем теле, начиная от формирования в виде эмбриона и до самой смерти.
А нуклеотиды – это что?
Нуклеотид – это, скажем так, кирпичик, и их нужно очень много, чтобы построить дом с кухней, залом и другими комнатами, которые находятся в определённой последовательности. ДНК человека содержит около 3 млрд пар нуклеотидов. Без них наш организм не будет существовать. В одной молекуле ДНК есть две цепочки нуклеотидов, которые спирально закручены вокруг друг друга. Три рядом расположенных нуклеотида кодируют аминокислоту. Основных аминокислот всего 20. Зачем они нужны? Чтобы построить белок – основной структурный элемент, из которого в нашем организме состоит всё. И белок как раз таки кодирует ДНК.
И как же происходит синтез белка?
Считается, что у человека около 20 тыс. генов. Здесь надо понимать, что дело не в количестве. Возьмём, к примеру, рис – у него их 30 тыс. Казалось бы, человек более высокоорганизованное существо, чем рис, он вершина эволюции! У него должно быть больше генов, чем у какого‑то растения. Но важнее, как сложно устроена работа организма. С помощью белка строятся мембраны клеток, ферменты. Условно говоря, у нас есть завод, где производятся машины. Чтобы машину собрать до конца, нужны колёса. А шины производят на соседнем заводе, их необходимо привезти. Так и здесь: есть молекула ДНК, и, чтобы синтезировать белок, она должна синтезироваться с РНК.
Если у нас есть ДНК, РНК тогда зачем?
Для того чтобы прочитать молекулу, её нужно сначала выделить, затем многократно скопировать, а после – нарезать на небольшие кусочки, удобные для анализа. И если ДНК хранит информацию, то РНК её копирует с ДНК и несёт из ядра на рибосому, в цитоплазму – этот процесс называется транскрипцией.
Интересно, что по своему химическому составу РНК является двойником ДНК. Главное отличие этих кислот заключается в их углеводном компоненте. В РНК это рибоза, а в ДНК – дезоксирибоза. И там, где у ДНК есть атом водорода (Н), у РНК стоит оксигруппа (ОН).
Чем отличаются ДНК мужчины и женщины?
Новый организм начинает формироваться ещё при оплодотворении, когда соединяются яйцеклетка и сперматозоид. В женском организме 44 аутосомы и две половые хромосомы. Они одинаковые: XX. Мужчина же может продуцировать половинный набор: у него 44 таких же, как и у женщины, аутосомы, а половые хромосомы разные: одна – X, другая – Y. То есть от матери ребёнок может унаследовать только женскую Х-хромосому, тогда как от отца он может получить либо женскую Х (родится девочка), либо мужскую Y (родится мальчик).
Кстати, папы, которые очень хотят мальчика, иногда винят мам, если в итоге рождается девочка. Но вина здесь исключительно отцов: какую половую клетку они отдают ребёнку, такой пол и получается.
Как узнать информацию о своём генеалогическом древе?
Родословную каждый может составить сам, пообщавшись с родственниками. Если есть интерес узнать более глубокое происхождение, за десятки и сотни тысяч лет, то генетики могут дать чёткий ответ, изучив генетические маркеры, которые записаны в X- и Y-хромосоме. В клетках человека часть информации есть в ядре, о чём мы уже говорили, и часть – в органоидах, вне ядра – в цитоплазме. В последней есть митохондриальные гены. По анализу их ДНК также можно проследить ход эволюции. И выяснить, что определённые изменения произошли, условно, 10 тысяч лет назад. Если генетики находят это изменение, то они могут точно сказать, когда появились и где жили прародители человека. Картотека расселения человечества есть в Интернете в свободном доступе.
А без сдачи анализов это можно определить?
Без них не обойтись: делаются выборки из разных этнических групп, достаточно большие по численности. Они анализируются, и только потом генетики строят карты. Кстати, на основании такого исследования учёные выяснили, что первые люди на Земле появились в Африке. В ДНК всех женщин есть следы, ведущие к одной прародительнице, жившей в Юго-Восточной Африке 150 тысяч лет назад. И гены всех мужчин сходятся к предку, проживавшему там же. Они отправная точка всех народов.
В Белгороде тоже проводят такие исследования?
Да, учёные-генетики из БелГУ собирали анализы ДНК коренных жителей Белгородской области, чьи семьи проживают на этой земле много поколений. При этом обязательно учитывали национальность, ведь у нас много как русских, так и украинцев. В Алексеевском, Грайворонском, Красногвардейском районах, например, 100 лет назад были целые поселения украинцев, которые старались до 30–40-х годов прошлого века жениться только между собой. Эти материалы вошли в крупные международные проекты. В отношении антропогенетики Белгородская область хорошо изучена.
У нас есть центр, где можно сделать анализ ДНК?
Есть только филиалы, точки сбора анализов. Любые исследования должны окупаться. Спрос среди белгородцев на это низкий, поэтому люди, у которых есть научный интерес, едут в Москву или Питер либо обращаются в сетевые лаборатории, которые сами отправляют материалы в крупные города.
Здесь важен и другой вопрос: у человека могут быть различные заболевания, которые контролируются генами. И исследования помогают разобраться в природе заболеваний, выявить их или предотвратить. Например, рак молочной железы. Если в организме происходят мутации, то риск того, что женщина заболеет, составляет 70–80 %. Зачастую это заболевание наследственное. Для того чтобы убедиться, если ли риск заболеть раком молочной железы у родственников, достаточно всем сдать анализы ДНК и наблюдаться у специалистов. Известный пример: у мамы Анжелины Джоли выявили эту болезнь. Анжелина протестировала свою ДНК на мутации, и подтвердилось, что они есть. Она сразу же сделала операцию. Анализы на такие заболевания в Белгороде сдают в перинатальном центре.
Правда, что отправлять пробирки со своими анализами ДНК за пределы России запрещено?
Как и для чего делают анализ ДНК?
В качестве материала для анализа можно использовать слюну, кровь, сперму, ногти, волосяные луковицы, ушную серу, кусочки кожи и так далее. Чтобы получить достоверный результат, лучше сдавать на ДНК-анализ кровь из вены.
С помощью анализа ДНК можно определить наследственную предрасположенность к патологиям, которые уже встречались в семье, какие заболевания могут возникнуть у конкретного человека в будущем, индивидуальную непереносимость лекарств, вероятность осложнений во время беременности, склонность к алкоголизму или наркомании, возможные причины бесплодия и многое другое.
Анализ используется не только в медицине, но и в юриспруденции, криминалистике. Самая популярная потребность в таком исследовании – определение отцовства. Сравнение ДНК ребёнка и его отца позволяет получить 100%-ный результат.
А не замахнуться ли нам на. изменение генома?
А не замахнуться ли нам на. изменение генома?
Ученые научились редактировать молекулу ДНК в интересующем месте
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Человек стремится покорить природу, и ключ для этого — ДНК. Но чтобы подобраться к молекуле ДНК и повлиять на нее, необходимо использовать точнейшие молекулярные инструменты — белки или РНК. В этой статье рассказывается о новейшем инструменте для внесения мутаций в геном in vivo — сиквенс-cпецифичных нуклеазах.
Конкурс «био/мол/текст»-2013
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Лучший обзор».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
История изучения ДНК непроста, как и любое значительное исследование. Открыта она была еще в 1868 году Иоганном Фридрихом Мишером, который выделил некое вещество, содержащее азот и фосфор, из остатков клеток в гное [1]. После того, как Мишер обнаружил, что оно обладает кислотными свойствами, вещество назвали нуклеиновой кислотой. Однако долгое время функция ДНК была неясной: ее считали всего лишь способом запасания фосфора в организме. Данная теория считалась правильной почти до середины XX века; в качестве косвенного доказательства ученые ссылались на однообразное, по их мнению, строение молекулы ДНК (состоящей исключительно из четырех различных видов нуклеотидов: дезоксиаденозина — А, дезоксигуанозина — G, дезокситимидина — Т, дезоксицитидина — С).
Функцию ДНК, естественно, открыли раньше, чем ее вторичную структуру, которая оставалась неизвестной вплоть до 1953 года. Соответственно, из-за этого не могли установить, как проходят такие процессы как передача наследственной информации, как белки распознают определенные последовательности в ДНК и т.п.
В 1949–1951 годах Эрвин Чаргафф сформулировал свои знаменитые правила, которые говорят о строгом соотношении количества азотистых оснований внутри каждой молекулы ДНК [4] (в частности, что количество аденина равняется количеству тимина, а количество цитозина — количеству гуанина); затем Морисом Уилкинсом и Розалиндой Франклин были получены рентгеноструктурные данные, несущие структурную информацию о ДНК. На основании этих двух фактов Френсис Крик и Джеймс Уотсон предложили структуру двойной спирали ДНК [5], которая была доказана позднее в опытах Мэтью Мезельсона и Франклина Сталя [6].
Как только была открыта вторичная структура ДНК, стало легче предсказывать, а затем доказывать экспериментами механизмы различных процессов, происходящих с ДНК. Репликация (удвоение молекулы ДНК), транскрипция (перенос генетической информации с ДНК на РНК), различная регуляция экспрессии генов стали главными проблемами, интересующими молекулярных биологов.
Очевидно, что для осуществления этих процессов необходимы определенные белки, которые, в свою очередь, взаимодействуют как друг с другом, так и с ДНК. И если некоторые стадии протекают неспецифично (например, у эукариот репликация ДНК может начаться во множестве участков ДНК [7]), то, например, регуляция экспрессии генов происходит с помощью взаимодействия белков с довольно консервативными, т.е. строгими последовательностями ДНК.
Эндонуклеазы рестрикции: «Режем ДНК в нужном вам месте!»
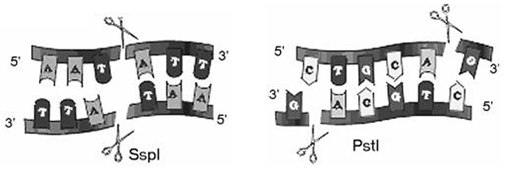
Одними из первых открытых белков, специфически связывающих ДНК, являются эндонуклеазы рестрикции. Это ферменты, которые разрезают ДНК по специфическим нуклеотидным последовательностям, называемым сайтами рестрикции (рис. 1) [8].
Рисунок 1. Рестрикция с образованием а) «тупых» концов; б) «липких» концов
Сам термин «рестрикция» появился благодаря исследованиям фага λ и феномена контролируемой рестрикции и модификации бактериальных вирусов клетками-хозяевами. Этот процесс был впервые обнаружен в результате работ Сальвадора Лурии [9] и Джузеппе Бертани [10] в 1950-х годах. Ученые обнаружили, что если фаг λ хорошо растет в одном штамме Escherichia coli, то в другом штамме его рост падает на несколько порядков, т.е. клетка-хозяин может снижать его биологическую активность. Оказалось, что запрет роста — «рестрикция» — вызывается ферментативным расщеплением ДНК фага. Соответственно, и фермент, отвечающий за этот процесс, назвали ферментом рестрикции.
Сами ферменты были обнаружены в лабораториях Вернера Арбера и Мэттью Мезельсона [11]; причем эндонуклеазы, которые исследовались в их работах, принадлежали, как определили позже, к I классу эндонуклеаз рестрикции. Они разрезают ДНК в случайном месте снаружи от места распознавания, причем как минимум на расстоянии 1000 нуклеотидов.
В 1970-х годах Гамильтон Смит, Томас Келли и Кент Велкокс выделили и охарактеризовали первую эндонуклеазу рестрикции II класса. Этот тип ферментов рестрикции более удобен для лабораторного использования, поскольку расщепляет ДНК внутри своего сайта распознавания, который, как правило, представляет собой палиндром из 4–8 нуклеотидов. Кроме того, эндонуклеазы этого класса не нуждаются в энергетической молекуле АТФ для активности, — только в ионах магния в качестве кофактора.
В 1990-х и ранних 2000-х годах были открыты другие представители данного семейства, которые не соответствовали всем критериям этого класса ферментов [12]. На данный момент уже открыты эндонуклеазы типов IIB, IIE, IIF, IIG, IIM, IIS, IIT. Возможно, в будущем этот список еще значительно расширится.
Существует также III класс эндонуклеаз рестрикции. Они были также открыты как компоненты прокариотической защитной системы против чужеродной ДНК. Эндонуклеазы III типа распознают две отдельных последовательности ДНК длиной 5–6 нуклеотидов и разрезают её примерно через 20–30 пар после сайта распознавания. Для их работы необходимы молекулы АТФ.
Эндонуклеазы рестрикции используют для обработки ДНК в различных лабораторных экспериментах. Обычно их применяют для вставки генов в процессах генного клонирования и экспериментах по исследованию белков.
Кроме того, эндонуклеазы могут быть использованы для выявления различий в аллелях гена [13]. Это возможно только в случае, если мутация произойдет в сайте узнавания, содержащемся внутри аллеля. Таким образом, отпадает нужда в дорогостоящем секвенировании гена; в частности, до изобретения секвенирования обработка эндонуклеазами рестрикции использовалась для картирования геномов.
Одно из новейших применений нуклеаз — внесение с помощью них различных изменений в геном клетки, таких как мутации уже имеющихся генов, вставка новых генов или вырезание исходных. Это очень перспективное направление генной инженерии с широчайшими возможностями практического применения! О нем будет рассказано в следующем разделе.
Эндонуклеазы — это эффекторы, т.е. белки действия. Если они окажутся у цели, то точно ее разрежут. Но природные белки распознают лишь небольшое число последовательностей ДНК, что накладывает огромные ограничения на использование этого уникального инструмента. Ах, если бы можно было доставить эндонуклеазу к любой желаемой последовательности ДНК.
Революция в области ДНК-связывающих белков: «Доставим ваш белок по любому адресу ДНК, используя TAL-эффекторы или CRISPR/Cas9-систему»
Одной из наиболее заманчивых идей для ученых является возможность напрямую точечно влиять на работу клетки. Для этого необходимо прицельно воздействовать на ДНК именно в области интересующего гена. Воздействие может быть разного характера: включение/выключение гена, внесение мутации и др. Для этого потребовалось уметь синтезировать белки, узнающие конкретную последовательность ДНК («следопыты»), к которым можно было бы пришить белки «действия».
Недавно открытые белки TAL-эффекторы и система Cas9 произвели настоящую революцию в нацеливании различных эффекторов на специфическую последовательность ДНК!
TAL-эффекторы: «Используем паразитов во благо»
TAL-эффекторы (Transcription Activator Like Effectors) — белки, синтезируемые многочисленным видами бактерий рода Xanthomonas — паразитами растений. Они были открыты в 2009 году практически одновременно несколькими группами ученых. TAL-эффекторы активируют считывание нужных паразитам генов в растениях-хозяевах (крайне специфично связываясь с хозяйской ДНК), что облегчает бактериальную колонизацию этого растения и выживание бактерий внутри него [14].
TAL-эффектор можно мысленно поделить на три части (рис. 2); наибольший интерес представляет средняя, крайне консервативная центральная область белка, состоящая из повторяющихся блоков размером 34 аминокислоты. В 2009 же году была показана простая и однозначная связь между повторами и узнаваемыми нуклеотидами. Блоки отличаются друг от друга лишь аминокислотами № 12 и № 13, которые и определяют вид нуклеотида, распознаваемый данным мономером. На каждый из четырех нуклеотидов ДНК приходится определенное сочетание этих аминокислот TAL-эффектора [15]; т.е. можно представить себе этот белок как паровозик, состоящий из одинаковых вагонов, центральное окошко которых покрашено в один из четырех цветов.
Рисунок 2. Строение TAL-эффектора на примере avrBs3
Простота «TALE-кода» открывает многочисленные возможности для биологического применения этих белков. Недавние исследования показали, что можно специально подобрать «вагоны» для искусственного «паровозика» и синтезировать ранее не существовавшие в природе белки для узнавания конкретных последовательностей ДНК в различных типах клеток — как растений, так и млекопитающих. Многие группы ученых уже используют искусственные TAL-эффекторы, узнающие новые последовательности ДНК, например, в томатах, Arabidopsis thaliana [16] и клетках человека [17].
Синтезированные TAL-эффекторы также сшивают с каталитическим доменом нуклеазы (см. раздел «Эндонуклеазы рестрикции») для создания TAL-эффекторных нуклеаз. Эти нуклеазы могут быть полезны для генной инженерии и генной терапии [18].
TAL-нуклеазы используют для создания двуцепочечных разрывов в строго определенном месте ДНК. Известно, что нарушенные таким образом гены клетка может чинить двумя путями: либо просто соединением концов (что может привести к случайным мутациям), либо заново синтезируя поврежденную цепь по комплементарной ей цепи ДНК (т.н. гомологичная рекомбинация).
Во втором случае вырезается значительный по длине участок ДНК, а вместо него по комплементарной (на краях разрыва) матрице синтезируется вставка, закрывающая брешь [19]. Если в клетку поместить ДНК специально мутированного гена, то он будет использован в качестве донорной матрицы, и в геном встроится желаемая мутация. Можно таким методом даже вырезать отдельные гены — или вставлять новые! Таким образом, благодаря разработанной технике сборки ДНК-узнающих повторов, TAL-эффекторы в составе гибридных белков предоставляют возможность направить желаемый эффектор к любой специфической последовательности ДНК — и добиться самых разных воздействий на ДНК: от регуляции транскрипции до внесений мутаций.
CRISPR/Cas9 система: «Неожиданное альтернативное применение защитного комплекса бактерий»
В нашем организме, после того, как мы переболели какой-то болезнью, остаются клетки памяти иммунной системы, которые при повторном попадании в организм вредителей активизируются и помогают ускоренно справиться с ними.
Бактерии справляются со своими патогенами с помощью аналогичной «системы памяти»: CRISPR/Cas-системы обеспечивают иммунитет бактерий и архей против вирусов и плазмид. Этот защитный комплекс состоит из:
Этот комплекс был открыт в 2012 году при совместной работе ученых из США, Швейцарии, Австрии и Швеции [20], [21].
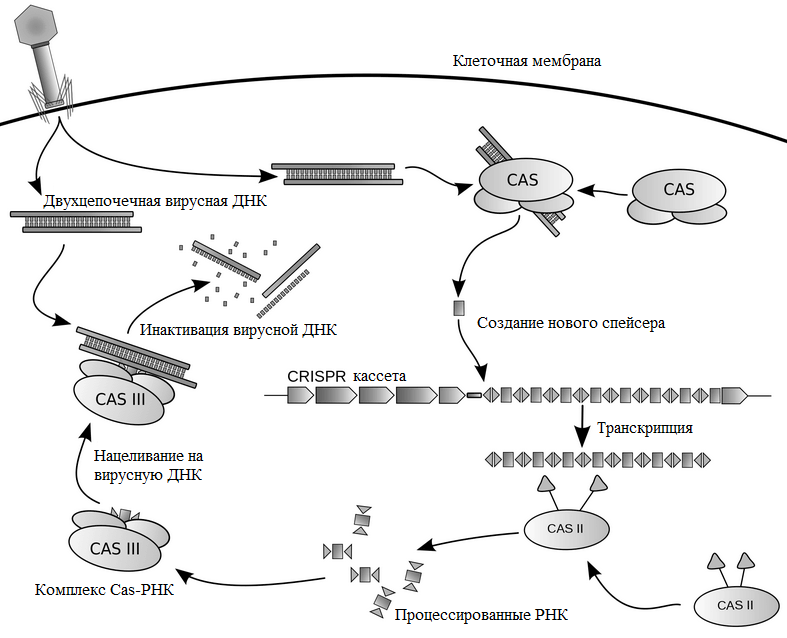
Иммунитет, обусловленный CRISPR/Cas, возникает за три стадии (рис. 3). В первой фазе бактерии или археи, у которых в геноме есть «блокнотик для записи» — CRISPR-кассета, — отвечают на появление вируса включением в конец кассеты коротких фрагментов чужеродной ДНК. На следующей стадии происходит транскрипция — считывание этой свежевключенной последовательности (образование описанных выше двух РНК) и обработка их нуклеазами. Теперь эти РНК могут специфично связаться с вирусной ДНК, и это взаимодействие через цепь событий приводит к ее расщеплению и «смерти» вредителя.
Рисунок 3. Схема работы комплекса Cas—РНК и CRISPR-кассеты
Грубо говоря, ситуация напоминает сказку про репку: первая РНК связывается с «репкой» — чужеродной ДНК — и «зовёт» вторую, вторая — специальный белок Cas9, который уже осуществляет двухцепочечный разрыв цепи чужой ДНК [22].
Несмотря на то, что в природе две РНК системы Cas9 разделены, учёные показали, что химерная РНК, представляющая собой сшитые в одну цепь вышеуказанные РНК, так же способна направлять Cas9 к ДНК-мишени. Более того, при соблюдении ряда условий можно менять последовательность первой внутри химерной РНК так, чтобы нацеливать Cas9 на желаемые гены.
Эта система даже проще TAL-эффекторов, поскольку для распознавания одного дезоксирибонуклеотида ДНК не нужен громоздкий «вагон» белка: один рибонуклеотид РНК легко и точно узнаёт комплементарный ему дезоксирибонуклеотид ДНК мишени! Экономия как в размере инструмента, так и в легкости его синтеза.
К настоящему времени показано, что эта система работает не только в археях и бактериях, но и в организмах рыб (Danio rerio), а также в клетках млекопитающих [23]. Уже установлено, что, как и в случае TAL-эффекторных нуклеаз, обработка ДНК Cas9-системой приводит к эффективному (10–30% случаев) возникновению мутаций.
Человек стремится покорить природу, и ключ для этого — ДНК. Но чтобы подобраться к ДНК и повлиять на нее, необходимо спуститься на молекулярный уровень и использовать белки или РНК. Сейчас развитие данных направлений идет стремительно, каждый месяц случаются значительные прорывы в этой области. Кто знает, какие чудеса ожидают нас через год? Возможно, будет найдена новая система, максимально упрощающая исходно сложный и кропотливый процесс вмешательства человека в работу природы.
Что влияет на днк человека
Если эта ошибка остается неисправленной, синтез белка и репликация ДНК усложняется во много раз — это и есть мутагенез. Солнечный свет нужен для выработки витамина D. Однако образование пиримидиновых димеров является одной из основных причин меланомы. Помимо этого, ультрафиолетовое излучение вредно для глаз. Вывод: длительное пребывание на солнце вредно. Солнечные ожоги опасны. Пренебрегать кремами с UV-фильтрами и находиться под прямыми солнечными лучами — легкомысленно, а ходить в солярий запрещено категорически. Прочее взаимодействие с солнцем (пробежка по пляжу на рассвете, например) нужно и полезно.
Враг №2: активные формы кислорода Самый распространенный мутаген. Хитрость заключается в том, что эти активные формы генерируются в ходе самых обычных химических реакций, которые протекают в человеческом теле. Тут может возникнуть недоумение, ведь кислород — это газ, который содержится в атмосфере нашей планеты, с ним ассоциируется дыхание полной грудью, свежесть и еще какие-то приятные ощущения из рекламы стиральных порошков.
Разгадка кроется в названии. Кислород окисляет вещества, которые встречает на своем пути. Вспомните перекись водорода, которую выливают на разбитую коленку — примерно то же самое происходит в клеточных масштабах при выделении активных форм кислорода. Активные формы кислорода разрушают мембраны, из которых построены живые клетки, выдергивают отдельные основания из цепи ДНК и вносят разрывы. Страшно не только то, что они делают, но и то, как изощренно это происходит. Поскольку выделение АФК осуществляется постоянно, при поломке нейтрализующего их механизма клетки постоянно подвергаются бомбардировке мутагенами и гибнут в муках.
Важно учитывать собственную генетическую предрасположенность к усвоению витаминов, так как антиоксиданты при чрезмерном потреблении вредны: они могут препятствовать усвоению других микроэлементов.
Доказано: полезные пищевые привычки помогут избежать этого врага. Будьте аккуратны и не ешьте просроченные продукты. Старайтесь тщательно мыть продукты и готовить еду непосредственно перед употреблением. Впрочем, люди с непереносимостью глютена, лактозы или кофеина в отношении афлатоксина чувствуют себя немного спокойнее: больше половины продуктов из группы риска уже исключены из их меню. Такая особенность пищевого поведения, как привычка переедать, может быть вдвойне вредна в данной ситуации.
Враг №4: бензол. Бензол — химическое соединение, без которого невозможно представить современную жизнь. Это токсин и канцероген, который входит в состав нефти и бензина, а также широко применяется в производстве лекарств, пластмасс, резины и красителей. Если поместить человека в замкнутое пространство и постепенно закачивать туда бензол, то сначала он почувствует эйфорию. Затем появятся сонливость, тошнота, головная боль, мышечные подергивания. Если оставить испытуемого в этой камере на длительное время, то он умрет, если же его выпустить, то можно будет наблюдать целый комплекс расстройств, вызванных отравлением бензолом. Однако нам интересно не это. Бензол часто встречается в некачественной косметической продукции и пластмассовых изделиях, то есть не исключено систематическое отравление бензолом в небольших количествах, что может провоцировать возникновение различных видов гемато-онкологических заболеваний.
Доказано: витамины группы В — Ниацин, фолат и кобаламин — необходимы для репарации ДНК. Дефицит этих витаминов в первую очередь заметен при отравлении бензолом. Зачастую люди получают витамины этой группы с мясом животных. Подробнее узнать о том, на какие процессы влияют витамины группы В и как диагностировать их недостаток, можно по ссылке.
Берегите себя. Враги в лице мутагенов могут быть повсюду. Когда речь заходит о здоровом образе жизни, тем, кто пытается изменить все своими силами, приходится балансировать между массой советов и здравым смыслом. Граница зыбкая и устоять на ней больше шансов у того,, кто знает себя и не наносит себе вред.