что такое авк в кардиологии
Что такое авк в кардиологии
АВК может сочетаться с другими врожденными пороками сердца (открытым артериальным протоком, аномалиями полых вен) и пороками развития других органов (селезенки, печени) либо с тяжелыми генетическими заболеваниями (синдром Дауна – врожденное заболевание, вызванное мутацией хромосом (переносчиков генетической информации), проявляющееся в характерных внешних признаках и снижении интеллекта).
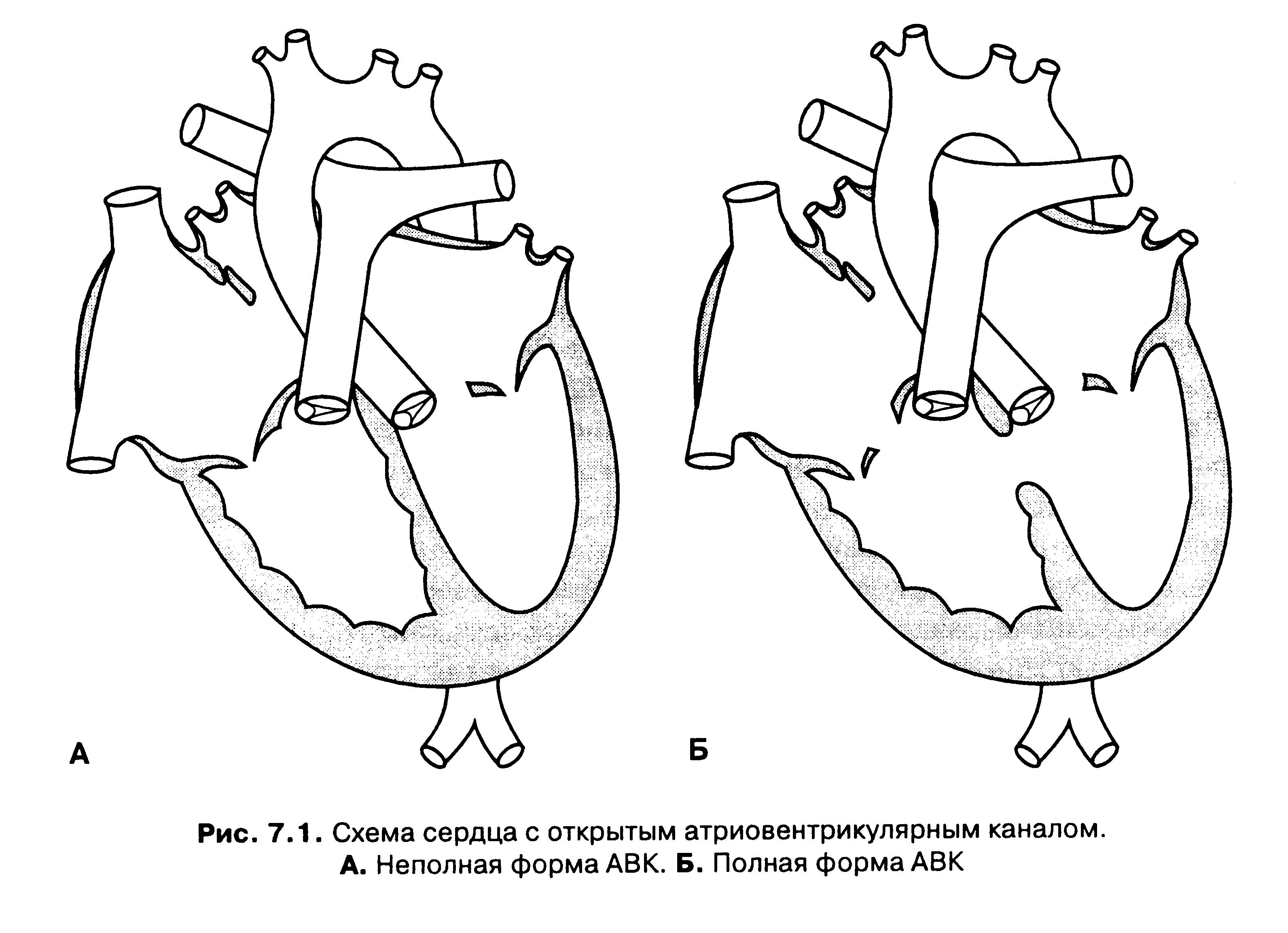
Полная форма АВК (рисунок Б) имеет несколько составляющих: дефект межпредесердной перегородки и дефект межжелудочковой перегородки, сливающиеся в одно огромное отверстие, и одно общее для обоих желудочков клапанное кольцо, регулирующееся двумя большими общими створками. Все отделы сердца работают с огромной перегрузкой, постоянно увеличенным объемом крови. Особенно оказывается переполненным малый круг. Давление в нем, естественно, повышается и, как и при больших ДМЖП, опасность быстрого развития необратимых изменений легочных сосудов очень высока.
Клинически порок протекает тяжело. Симптомы сердечной недостаточности появляются уже в первые месяцы жизни, и состояние ребенка требует постоянной лекарственной поддержки. Сердце быстро увеличивается в размерах — все его четыре камеры перегружены и с трудом справляются с работой. Ребенок очень болен, плохо ест и развивается, постоянно «подхватывает» простудные заболевания, часто заканчивающиеся воспалением легких. Состояние не критическое, но очень опасное. Операция необходима вскоре после точного установления диагноза. В нашей клинике радикальную коррекцию данного порока проводят в возрасте 3-6 мес.
В некоторых случаях оперативное лечение необходимо разбить на два этапа, т.е. вначале сузить легочную артерию (как при ДМЖП), а через несколько месяцев сделать радикальную операцию.
Неполная форма АВК (рисунок А) характеризуется отсутствием дефекта межжелудочковой перегородки, протекает более благоприятно. Оперативное лечение проводится обычно в возрасте старше 1 года.
Открытый атриовентрикулярный канал
Общие сведения
Открытый атриовентрикулярный канал – сочетанный врожденный порок сердца, характеризующийся недоразвитием внутрисердечных перегородок и аномалиями предсердно-желудочковых клапанов. Частота выявления открытого атриовентрикулярного канала в кардиологии составляет 2-6% от всего числа врожденных пороков сердца. Открытый атриовентрикулярный канал обычно обнаруживается в возрасте до 1 года.
В 25–30% случаев открытый атриовентрикулярный канал встречается при синдроме Дауна. У 13-18% пациентов, кроме открытого атриовентрикулярного канала, выявляются другие сердечные аномалии: стеноз или атрезия легочной артерии, тетрада Фалло, коарктация аорты и пр.
Причины открытого атриовентрикулярного канала
В основе формирования открытого атриовентрикулярного канала лежат эмбриологические нарушения. Факторами, способными вызвать недоразвитие перегородок и клапанов сердца, могут являться наследственная история по врожденным порокам, хромосомные нарушения, токсикозы беременности, вирусные инфекции беременной (краснуха, герпес, ветрянка, грипп), эндокринные нарушения у матери (сахарный диабет), употребление алкоголя или лекарственных препаратов с тератогенным действием.
Структуру дефекта при открытом атриовентрикулярном канале составляют следующие компоненты: дефекты предсердной и желудочковой перегородок, нарушение строения клапанов (митрального и трикуспидального).
Классификация открытого атриовентрикулярного канала
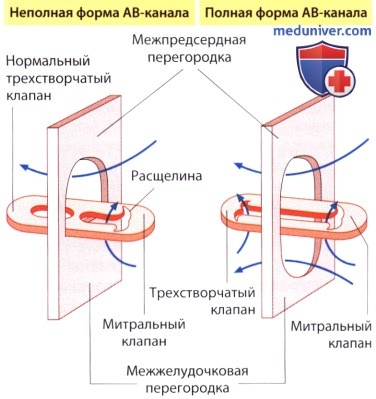
Неполная форма атриовентрикулярного канала (дефект первичной межпредсердной перегородки) характеризуется сообщением камер сердца на уровне предсердий, а также деформацией или расщеплением передней митральной и/или перегородочной трикуспидальной створок.
К полной форме открытого атриовентрикулярного канала (общий ОАВК) относят сочетание сливающегося дефекта мембранозной части МЖП с высоко расположенным дефектом МЖП и наличие одного общего клапана между обеими половинами сердца. При промежуточных формах порока (косых каналах, дефектах Гербоде) имеются левожелудочково-правопредсердные сообщения.
Особенности гемодинамики при открытом атриовентрикулярном канале
Нарушения внутрисердечной гемодинамики при открытом атриовентрикулярном канале зависят от анатомической формы порока. Наличие частично открытого атриовентрикулярного канала обусловливает лево-правое шунтирование крови; легочная гипертензия незначительна, митральная недостаточность выражена умеренно.
При общем открытом атриовентрикулярном канале имеется лево-правый сброс и небольшой шунт крови справа налево. Митральная и трикуспидальная недостаточность приводит к систолической регургитации крови из желудочков в предсердия. В этом случае рано развиваются легочная гипертензия и синдром Эйзенменгера. Промежуточные формы открытого атриовентрикулярного канала сопровождаются поступлением крови из левого желудочка непосредственно в правое предсердие, перегрузкой правого желудочка, расширением ствола легочной артерии.
Симптомы открытого атриовентрикулярного канала
Клинические проявления открытого атриовентрикулярного канала развиваются на первом году жизни, в дальнейшем состояние больных прогрессирующе ухудшается. Отмечается отставание ребенка в физическом развитии, быстрая утомляемость при кормлении, снижение аппетита, бледность кожи и слизистых. При полной форме открытого атриовентрикулярного канала вследствие артериальной гипоксемии выражен цианоз кожных покровов в области носогубного треугольника, ладоней и стоп.
Диагностика открытого атриовентрикулярного канала
Для подтверждения диагноза открытого атриовентрикулярного канала проводятся ЭКГ, фонокардиография, УЗИ сердца, зондирование полостей сердца, рентгенографическое исследование органов грудной клетки, атрио- и вентрикулография.
На электрокардиограмме регистрируется отклонение ЭОС влево, гипертрофия левого предсердия, гипертрофия желудочков, блокада правой ножки пучка Гиса или атриовентрикулярная блокада. Рентгенография выявляет кардиомегалию за счет увеличения обоих желудочков и правого предсердия, усиление легочного рисунка, умеренное выбухание дуги легочной артерии, признаки митральной недостаточности.
Прямые указания на открытый атриовентрикулярный канал дает эхокардиография: при сканировании виден ДМЖП, ДМПП, расщепление и аномалии прикрепления створки митрального клапана, регургитация крови в области клапанов. Полученные данные подтверждаются при катетеризации полостей сердца и вентрикулографии.
Лечение открытого атриовентрикулярного канала
Медикаментозная терапия при открытом атриовентрикулярном канале направлена на профилактику инфекционного эндокардита и купирование сердечной недостаточности. Радикальное устранение порока может быть проведено только хирургически. Раннее оперативное лечение показано при полной форме открытого атриовентрикулярного канала; при частичной и промежуточных формах корригирующая операция проводится в 6-10 лет.
Коррекция неполной формы атриовентрикулярного канала предусматривает восстановление передней створки митрального клапана, закрытие дефекта межпредсердной перегородки, при необходимости – пластику трикуспидального клапана.
Коррекция полного открытого атриовентрикулярного канала включает одномоментную пластику ДМПП, ДМЖП, митрального и трехстворчатого клапанов. У детей раннего возраста иногда предварительно выполняется паллиативная операция по сужению легочного ствола. При промежуточных вариантах открытого атриовентрикулярного канала проводится пластика ДМЖП и аннулопластика трикуспидального клапана. Операции производятся в условиях искусственного кровообращения.
Прогноз при открытом атриовентрикулярном канале
Течение полной формы открытого атриовентрикулярного канала неблагоприятно: без своевременной коррекции порока 95% пациентов погибают в течение первых 5 лет жизни. При частичной форме открытого атриовентрикулярного канала средняя продолжительность жизни больных без операции – 15-20 лет. Промежуточные формы протекают относительно благоприятно, однако также нуждаются в хирургической коррекции. Послеоперационные результаты открытого атриовентрикулярного канала удовлетворительные.
Что такое авк в кардиологии
Для многих врожденных пороков сердца характерно сочетание нескольких аномалий развития. Это проявляется большим разнообразием клинической симптоматики или изменением клинической картины основного порока (например, степени выраженности цианоза). В некоторых случаях даже при сочетанных врожденных пороках сердца больные могут жить длительное время.
Под открытым атриовентрикулярным каналом понимают недоразвитие атриовентрикулярной перегородки, которая закладывается в области эндокардиальных валиков (подушек). Различают неполную и полную форму открытого атриовентрикулярного канала. Неполная форма характеризуется отсутствием каудальной части межпредсердной перегородки и частично митральной половины атриовентрикулярной перегородки с расщеплением створки митрального клапана. Для полной формы, помимо этих изменений, характерны также дефект трехстворчатого клапана с расщеплением его створки и дефект межжелудочковой перегородки.
а) Общие изменения, выявляемые при эхокардиографии. Эхо кардиографическая картина, выявляемая при открытом атриовентрикулярном канале, патогномонична для этого порока сердца. Она характеризуется не только высокой специфичностью, но и позволяет уточнить форму порока и оценить степень его тяжести.
б) Двумерная эхокардиография. Ведущим признаком открытого атриовентрикулярного канала при двумерной ЭхоКГ является прикрепление септальных створок атриовентрикулярных клапанов к межжелудочковой перегородке на одинаковом уровне, в то время как в норме септальная створка трехстворчатого клапана и аортальная створка митрального клапана отчетливо смещены друг относительно друга, при этом створка трехстворчатого клапана расположена апи-кальнее. Прикрепление обеих септальных створок к межжелудочковой перегородке на одном уровне отмечается при всех без исключения формах открытого атриовентрикулярного канала, даже при изолированном расщеплении створки митрального клапана.
в) Эхокардиография в М-режиме. При ЭхоКГ в М-режиме в типичных случаях выявляют размашистое диастолическое движение митрального клапана, вызываемое межжелудочковой перегородкой, а также расширение полостей сердца, о котором подробнее говорится далее.
Видео ЭхоКГ при атриовентрикулярном канале у плода
г) Неполная форма открытого атриовентрикулярного канала. При неполной форме открытого атриовентрикулярного канала имеется дефект лишь части межпредсердной и атриовентрикулярной перегородки. По существу это дефект межпредсердной перегородки типа ostium primum в сочетании с дефектом переднего отдела митрального клапана. Гемодинамически значимый дефект межжелудочковой перегородки отсутствует.
1. Патологическая анатомия. При морфологическом исследовании выявляют дефект межпредсердной перегородки типа ostium primum, а именно отсутствие каудальной ее части, расположенной непосредственно над атриовентрикулярными клапанами. Из-за дефекта развития атриовентрикулярной перегородки септальные створки обоих атриовентрикулярных клапанов смещены в одну общую плоскость; движение передней створки митрального клапана нарушено и, кроме того, она расщеплена. Длина вносящего тракта левого желудочка существенно короче длины его выносящего тракта, что делает полость желудочка похожей на «гусиную шею».
2. Гемодинамика. Неполная форма открытого атриовентрикулярного канала с характерным для него дефектом межпредсердной перегородки относится к претрикуспидальным порокам сердца. Левоправый сброс крови, присущий этим порокам, обусловливает перегрузку объемом правых отделов сердца и присущее дефектам межпредсердной перегородки нарушение гемодинамики (см. статью «Вариант дефекта вторичной межпредсердной перегородки: открытое овальное окно»). Кроме того, из-за часто наблюдающегося расщепления передней створки митрального клапана развивается митральная недостаточность, вызывающая расширение левого предсердия и повышение сократительной функции миокарда левого желудочка.
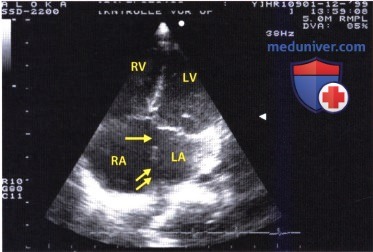
3. Результаты эхокардиографии. Эхокардиографические изменения, выявляемые при открытом атриовентрикулярном канале, патогномоничны для этого порока сердца и, помимо высокой диагностической специфичности, позволяют также оценить степень его тяжести.
4. Двумерная эхокардиография. Ведущим признаком при двумерной ЭхоКГ, наряду со смещением септальных створок обоих атриовентрикулярных клапанов в общую плоскость, является полное отсутствие эхо-сигналов от каудальной части межпредсердной перегородки непосредственно над атриовентрикулярными клапанами. Аналогичная картина представлена на видеозаписи ниже. Кроме того, отмечается также выпячивание верхней части межжелудочковой перегородки в правый желудочек, обусловленное недоразвитием желудочковой части атриовентрикулярной перегородки, которое нередко становится причиной появления сброса крови на уровне желудочков (промежуточная форма открытого атриовентрикулярного канала).
6. Цветовая допплерография. Предсердный сброс крови происходит непосредственно проксимальнее атриовентрикулярных клапанов; кровь забрасывается прямо в отверстие трехстворчатого клапана. При расщеплении створки митрального клапана можно выявить струю митральной регургитации, забрасываемую в левое предсердие.
7. Спектральная допплерография. При оптимальном угле наклона датчика можно измерить скорость струи митральной регургитации и по скорости рассчитать систолический градиент давления между левым желудочком и левым предсердием. Зная систолическое давление в желудочке, можно определить высоту V-волны кривой давления в левом предсердии. Если имеется недостаточность трехстворчатого клапана, то можно определить также систолическое давление в правом желудочке.
8. Другие изменения, выявляемые при эхокардиографии. При выполнении ЭхоКГ не следует забывать, что у больного могут быть также сопутствующие пороки сердца, в частности открытый артериальный проток, стеноз легочной артерии или перешейка аорты.
д) Полная форма открытого атриовентрикулярного канала. Эта форма открытого атриовентрикулярного канала включает в себя все компоненты, присущие данному пороку сердца. Дети с полной формой открытого атриовентрикулярного канала в зависимости от особенностей дефектов атриовентрикулярных клапанов и межпредсердной перегородки обычно нуждаются в ранней (обычно уже в грудном возрасте) хирургической коррекции. Без лечения они почти никогда не доживают до взрослого состояния.
1. Патологическая анатомия. Помимо дефекта межпредсердной перегородки и расщепления передней створки митрального клапана, имеется также высокий дефект межжелудочковой перегородки, над которым смыкаются септальные створки атриовентрикулярных клапанов. Полная форма открытого атриовентрикулярного канала по сравнению с неполной характеризуется более выраженными изменениями и обусловливает более тяжелое состояние больных. В зависимости от положения створок атриовентрикулярных клапанов и атриовентрикулярного дефекта Rastelli выделяет 3 формы порока. На рисунке ниже показан атриовентрикулярный дефект при промежуточной форме открытого атриовентрикулярного канала, соответствующий типу А по классификации Rastelli.
2. Гемодинамика. При большом дефекте межжелудочковой перегородки отмечается значительный левоправый сброс, поэтому обычно выявляют легочную гипертензию, гиперволемическая ее стадия вскоре переходит в склеротическую, которая быстро приводит к развитию синдрома Эйзенменгера.
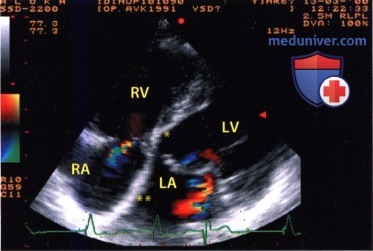
4. Эхокардиография в М-режиме. При ЭхоКГ в М-режиме выявляют уже описанное патологическое движение митрального клапана, являющееся неспецифическим признаком перегрузки левых отделов сердца, расширение левого предсердия и левого желудочка, а также повышение фракции выброса.
5. Цветовая допплерография. Сброс крови на уровне предсердий направлен исключительно слева направо; для полной формы порока характерен также сброс крови на уровне желудочков, направление которого зависит от соотношения давления в них (перекрестный сброс крови), отмечается митральная недостаточность.
6. Спектральная допплерография. Если дефект межжелудочковой перегородки большой, градиент давления на нем практически не определяется; это указывает на легочную гипертензию. Недостаточность трехстворчатого клапана, если она имеется, выявляют на основании систолической струи обратного кровотока из правого желудочка в предсердие, характеризующейся высокой скоростью.
7. Послеоперационное обследование. Почти всегда у взрослых больных с общим атриовентрикулярным каналом порок бывает уже корригированным или же отмечается его неполная или промежуточная форма без выраженного нарушения гемодинамики. В тех случаях, когда выполнена хирургическая коррекция, при сканировании в плоскости четырех камер сердца выявляют длинную заплату, которая подшита к краниальному и каудальному краю дефекта межжелудочковой перегородки. Общий атриовентрикулярный канал, который имелся в результате полного расщепления септальных створок атриовентрикулярных клапанов, разделен с помощью искусственной перегородки.
Заплата, которая тянется от нижнего края межпредсердной перегородки до верхнего края межжелудочковой перегородки, устраняет сброс крови. Резидуальный сброс, как правило, отсутствует. Обычно, как это показано на рисунке выше, имеется митральная недостаточность в покое, а также недостаточность трехстворчатого клапана. Это обусловлено неполным закрытием расщелины в створке митрального, а также трехстворчатого (если она имеется) клапана или развитием стеноза. При выраженной митральной недостаточности показана повторная операция с имплантацией при необходимости клапанного протеза. При недостаточности трехстворчатого клапана коррекцию можно не выполнять.
При ЭхоКГ в М-режиме после операции часто остается диастолическое движение митрального клапана. Митральная недостаточность в покое проявляется признаками перегрузки объемом левого желудочка.
Сопутствующие пороки сердца, как правило, также подлежат коррекции, и имеющиеся дефекты должны быть закрыты в дальнейшем.
Видео ЭхоКГ при полной полной форме атриовентрикулярного канала у плода
Редактор: Искандер Милевски. Дата публикации: 16.1.2020
Если вашему ребенку поставили диагноз врожденный порок сердца, не стоит опускать руки, нужно узнать все способы поддержания здоровья таких детей, а также причины развития данного заболевания, пройти необходимое обследование, чтобы врач назначил соответствующее лечение.
Сердце человека состоит из четырех камер: правое предсердие (ПП) и правый желудочек (ПЖ), левое предсердие (ЛП) и левый желудочек (ЛЖ). Правые и левые отделы сердца между собой никак не сообщаются. В этом нет необходимости, так как они обеспечивают движение крови каждый по своему кругу. Левые отделы сердца отвечают за движение крови по большому кругу кровообращения. Из левого предсердия через левый желудочек в аорту (Ао) поступает артериальная кровь, богатая кислородом. Из аорты по многочисленным артериям, а потом и по капиллярам она разносится по всему организму, доставляя клеткам кислород. В свою очередь, «отработанная» организмом венозная кровь собирается в мелкие вены, которые сливаются в более крупные венозные сосуды – верхнюю и нижнюю полые вены (ВПВ и НПВ). Конечная точка путешествия венозной крови – правое предсердие. Оттуда через правый желудочек кровь попадает в легочную артерию (ЛА). Малый круг кровообращения проходит через легкие, где венозная кровь обогащается кислородом и вновь становится артериальной. Отток обновленной крови осуществляется по легочным венам (ЛВ), впадающим, в свою очередь, в левое предсердие.
Особенности кровообращения у плода и новорожденного
Находясь в утробе матери, плод не дышит самостоятельно и его легкие не функционируют. Кровообращение осуществляется через плаценту. Насыщенная кислородом кровь матери поступает к плоду через пуповину: в венозный проток, откуда через систему сосудов в правое предсердие. У плода между правым и левым предсердием имеется отверстие – овальное окно. Через него кровь попадает в левое предсердие, затем в левый желудочек, аорту – и ко всем органам плода. Малый круг кровообращения отключен. В легкие плода кровь поступает через артериальный проток – соединение между аортой и легочной артерией. Венозный проток, овальное окно и артериальный проток имеются только у плода. Они называются «фетальными сообщениями». Когда ребенок рождается и пуповину перевязывают, схема кровообращения радикально изменяется. С первым вдохом ребенка его легкие расправляются, давление в сосудах легких снижается, кровь притекает в легкие. Малый круг кровообращения начинает функционировать. Фетальные сообщения больше не нужны ребенку и постепенно закрываются (венозный проток – в течение первого месяца, артериальный проток и овальное окно – через два-три месяца). В некоторых случаях своевременного закрытия не происходит, тогда у ребенка диагностируют врожденный порок сердца (ВПС). Иногда при развитии плода возникает аномалия и ребенок рождается с анатомически измененными структурами сердца, что также считается врожденным пороком сердца. Из 1000 детей с врожденными пороками рождается 8-10, и эта цифра увеличивается в последние годы (развитие и совершенствование диагностики позволяет врачам чаще и точнее распознавать пороки сердца, в том числе, когда ребенок еще в утробе матери).
«Синие» и «бледные» пороки сердца
Аномалии могут быть очень разнообразными, наиболее часто встречающиеся имеют названия и объединяются в группы. Например, пороки разделяют на «синие» (при которых кожные покровы ребенка синюшные, «цианотичные») и «бледные» (кожные покровы бледные). Для жизни и развития ребенка более опасны «синие» пороки, при которых насыщение крови кислородом очень низкое. К «синим» порокам относятся Тетрада Фалло, транспозиция магистральных сосудов, атрезия легочной артерии. К «бледным» порокам относятся дефекты перегородок – межпредсердной, межжелудочковой. В некоторых случаях порок может частично компенсироваться за счет открытого артериального протока (в норме он закрывается, как только легкие ребенка расправляются с первым криком). Также у ребенка может недоразвиться клапан сердца – сформируется клапанный порок (наиболее часто, аортальный клапан или клапан легочной артерии).
Причины развития врожденного порока сердца
У плода формирование структур сердца происходит в первом триместре, на 2-8 неделе беременности. В этот период развиваются пороки, которые являются следствием наследственных генетических причин или воздействия неблагоприятных внешних факторов (например, инфекция или отравления). Иногда у ребенка имеется несколько пороков развития, в том числе и порок сердца. Риск рождения ребенка с врожденным пороком сердца очень высок, если:
— ранее у женщины были выкидыши или мертворожденные
— возраст женщины более 35 лет
— женщина во время беременности принимает алкоголь, психоактивные вещества (наркотики), курит
— в семье женщины есть история рождения детей с пороками или мертворождения
— женщина живет в экологически неблагоприятной местности (радиация, отравляющие вещества)
или работает на экологически неблагоприятном производстве
— во время беременности (особенно первые 2 месяца) женщина перенесла инфекционные, вирусные заболевания
— женщина принимала во время беременности лекарственные препараты
с тератогенным эффектом (приводящие к развитию уродств у плода) или
эндокринные препараты для сохранения беременности (гормоны).
Можно ли поставить диагноз ВПС у плода?
Врожденный порок сердца у новорожденных
При рождении ребенка или в первые дни его жизни врачи могут заподозрить врожденный порок сердца.
На чем они основывают свои предположения?
— Шум в сердце. В первые несколько дней жизни ребенка шум в сердце нельзя расценивать как достоверный симптом врожденного порока сердца. Такого ребенка наблюдают, при сохранении шумов более 4-5 суток – обследуют. Само появление сердечного шума объясняется нарушением тока крови через сосуды и полости сердца (например, при наличии аномальных сужений, отверстий, резкой смены направления кровотока).
— синюшность кожных покровов (цианоз). В норме артериальная кровь богата кислородом и придает коже розовую окраску. Когда к артериальной крови примешивается бедная кислородом венозная кровь (в норме не происходит), кожа приобретает синюшный оттенок. В зависимости от типа порока цианоз может быть разной степени выраженности. Однако, врачам приходится уточнять причины цианоза, так как он может быть симптомом болезней органов дыхания и центральной нервной системы.
— проявления сердечной недостаточности. Сердце перекачивает кровь, работая как насос. Когда снижается насосная способность сердца, кровь начинает застаиваться в венозном русле, питание органов артериальной кровью снижается. Учащаются сердечные сокращения и дыхание, появляется увеличение печени и отечность, быстрая утомляемость и одышка. К сожалению, эти признаки очень трудно распознать у новорожденных. Высокая частота сердечных сокращений и дыхания наблюдается у маленьких детей в нормальном состоянии. Только при значительных отклонениях можно с достаточной уверенностью говорить о развитии у малыша сердечной недостаточности. Часто следствием развития сердечной недостаточности является спазм периферических сосудов, что проявляется похолоданием конечностей и кончика носа, их побледнением. Эти признаки помогают косвенно судить о недостаточности сердца.
— нарушения электрической функции сердца (сердечного ритма и проводимости), проявляющиеся аритмиями и, иногда, потерей сознания. Врач может услышать неровное сердцебиение при аускультации (выслушивании фонендоскопом) или увидеть на записи электрокардиограммы.
Как сами родители могут заподозрить у ребенка врожденный порок сердца?
Подтверждение диагноза врожденного порока сердца
В настоящее время наиболее доступным, простым, безболезненным для ребенка и высокоинформативным методом диагностики пороков сердца является эхокардиография. Во время исследования с помощью ультразвукового датчика врач видит толщину стенок, размеры камер сердца, состояние клапанной системы и расположение крупных сосудов. Допплеровский датчик позволяет увидеть направления кровотока и измерить его скорость. Во время исследования можно выполнить снимки, подтверждающие заключение специалиста. Также ребенку обязательно запишут электрокардиограмму. При необходимости более точного исследования (как правило, для определения тактики хирургического лечения порока) врач порекомендует зондирование сердца. Это инвазивная методика, для выполнения которой ребенок госпитализируется в стационар. Зондирование проводится врачем-рентгенхирургом в рентгеноперационной, в присутствии врача-анестезиолога, под внутривенным наркозом. Через прокол в вене или артерии специальные катетеры вводятся в сердце и магистральные сосуды, позволяя точно измерить давление в полостях сердца, аорте, легочной артерии. Введение специального рентген-контрастного препарата позволяет получить точное изображение внутреннего строения сердца и крупных сосудов (см. рисунок).
Диагноз – не приговор. Лечение ВПС (врожденного порока сердца)
Современная медицина позволяет не только своевременно диагностировать, но и лечить врожденные пороки сердца. Лечением ВПС занимаются кардиохирурги. При выявлении порока, сопровождающегося серьезным нарушением гемодинамики, влияющего на развитие ребенка и угрожающего жизни малыша, операция проводиться как можно раньше, иногда в первые дни жизни ребенка. При пороках, которые не влияют значительно на рост и развитие ребенка, операция может проводиться позже. Выбор сроков операции определяется хирургом. Если ребенку рекомендовали хирургическое вмешательство и его не удалось выполнить своевременно (часто из-за отказа родителей, непонимания серьезности проблемы), у ребенка может начаться патологическое изменение гемодинамики, приводящее к развитию и прогрессированию сердечной недостаточности. На определенном этапе изменения становятся необратимыми, операция уже не поможет. Отнеситесь внимательно к советам и рекомендациям врачей, не лишайте своего ребенка возможности расти и развиваться, не быть инвалидом на всю жизнь!
Операция при врожденных пороках сердца
Многие годы операции при врожденных пороках сердца выполнялись только на открытом сердце, с использованием аппарата искусственного кровообращения (АИК), который берет на себя функции сердца во время его остановки. Сегодня при некоторых пороках такой операции существует альтернатива – устранение дефекта структур сердца с помощью системы AMPLATZER. Такие операции значительно безопаснее, не требуют раскрытия грудной клетки, не отличаясь по эффективности от «большой» хирургии. Если операция выполнена своевременно и успешно, ребенок полноценно развивается и растет, и часто – навсегда забывает о существовании порока. После операции обязательным является наблюдение педиатра, контрольные эхокардиографические исследования. Дети с врожденными пороками сердца часто болеют простудными заболеваниями из-за снижения иммунитета, поэтому в послеоперационном периоде проводится общеукрепляющее лечение и ограничиваются физические нагрузки. В дальнейшем у многих детей эти ограничения снимают и даже разрешают посещать спортивные секции.
Статья была опубликована сотрудниками нашего Центра ранее на «Сибирском медицинском портале».