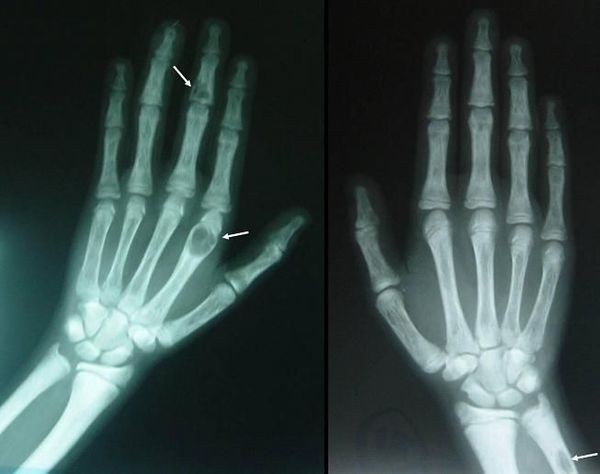
что снижает кальций в крови
Что снижает кальций в крови
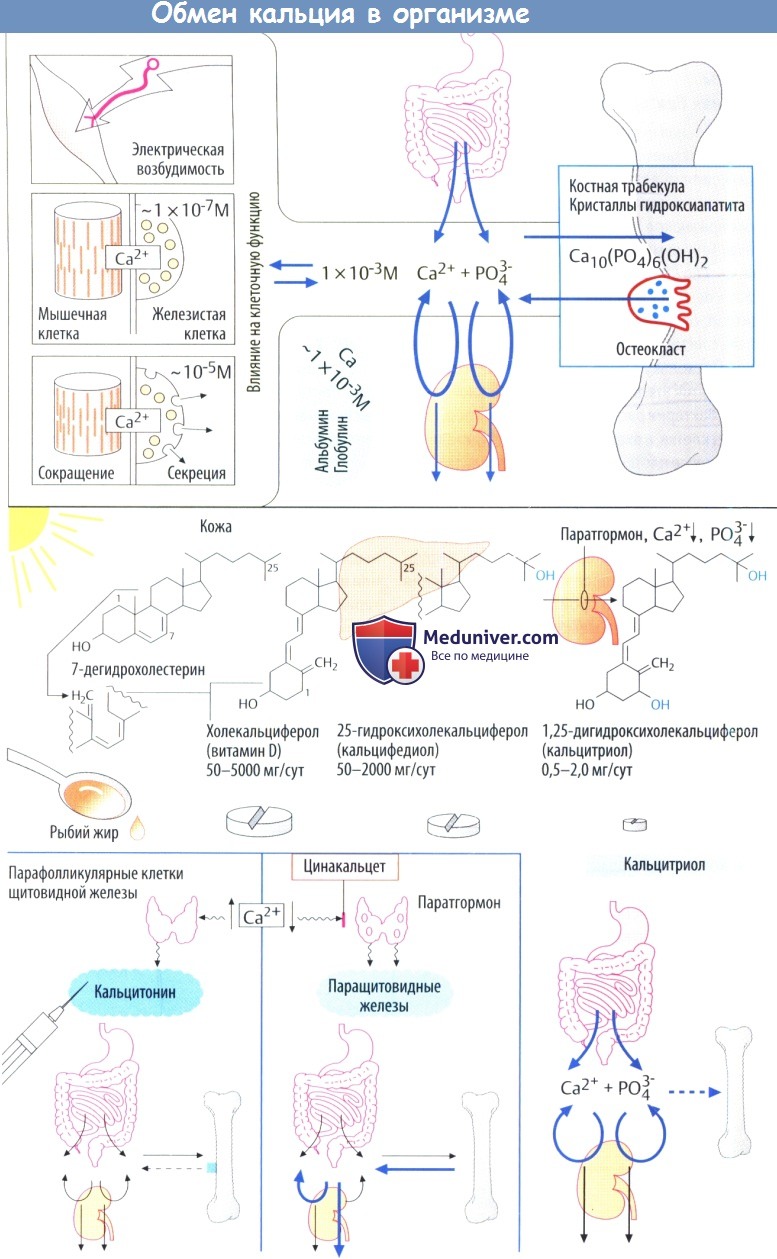
В покое внутриклеточная концентрация свободных ионов Са 2+ сохраняется на уровне 0,1 мкмоль/л. Во время возбуждения временное повышение концентрации до 10 мкмоль/л вызывает сокращение мышечных клеток (электромеханическое сопряжение) и секрецию железистых клеток (электросекреторное сопряжение).
Клеточное содержание Са 2+ находится в равновесии с внеклеточной концентрацией (1000 мкмоль/л), как и связанная с белком фракция Са 2+ в плазме. Са 2+ может кристаллизироваться с фосфатом до образования гидроксиапатита, т. е. минеральной кости. Остеокласты представляют собой фагоциты, которые мобилизуют Са 2+ за счет резорбции кости.
Витамин D. Биологически неактивная форма витамина D (холекальциферол) образуется в коже из дегидрохолестерина при УФ-облучении. При недостаточной инсоляции основным источником становится пища, причем особенно много его содержится в рыбьем жире. Метаболически активный кальцитриол является результатом двух успешных реакций гидроксилирования: в печени в положении 25 (=> кальцифедиол) и в почках в положении 1 (=> кальцитриол).
1-гидроксилирование зависит от уровня гомеостаза Са 2+ и стимулируется паратгормоном, который вызывает снижение уровня Са 2+ и фосфата. Кальцитриол стимулирует кишечное всасывание и почечную реабсорбцию Са 2+ и фосфата. В результате повышения концентрации в крови Са 2+ и фосфата все больше ионов откладывается в кости в виде кристаллов гидроксиапатита. Дефицит витамина D приводит к недостаточной минерализации костей (рахит, остеомаляция). Витамин D используется в качестве заместительной терапии: при заболеваниях печени показан кальцифедиол, при заболеваниях почек — кальцитриол.
Передозировка может вызывать гиперкальциемию с отложениями кальциевых солей в тканях (в частности, в почках и кровеносных сосудах) — кальциноз.
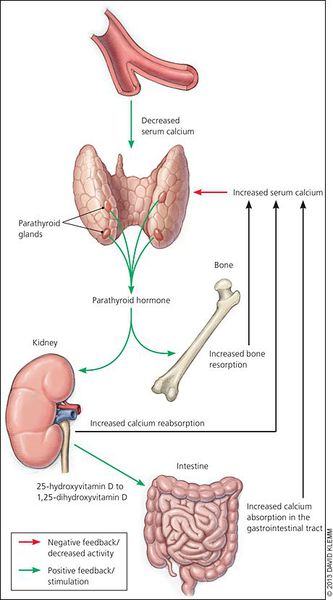
Полипептид паратгормон высвобождается из паращитовидных желез при падении уровня Са 2+ в плазме. Он стимулирует остеокласты, что приводит к повышению резорбции костей. В почках он стимулирует реабсорбцию Са 2+ при увеличении экскреции фосфата. Поскольку снижается концентрация фосфат в крови, меньшее количество Са 2+ переходит в минеральную кость. За счет стимуляции образования гормона витамина D паратгормон оказывает прямое действие на захват Са 2+ и фосфата в тонкой кишке.
При дефиците паратгормона витамин D может использо ваться в качестве замещающего средства, который в отличие от паратгормона эффективен при введе нии внутрь. Терипаратид — рекомбинантное укоро ченное производное паратгормона, содержащее уча сток, необходимый для связывания с рецепторами Он используется при лечении остеопороза в постме нопаузе и стимулирует образование костей. Хотя данный эффект кажется парадоксальным в сравнении с гиперпаратиреозом, он, очевидно, связан с особым режимом дозирования: п/к инъекция 1 раз в сутки создает квазипульсирующую стимуляцию.
Полипептид кальцитонин секретируется С-клетками щитовидной железы во время угрожающей гиперкальциемии. Он снижает повышенный уровень Са 2+ в плазме за счет ингибирования активности остеокластов. Используется при гиперкальциемии и остеопорозе. Примечательно, что инъекция кальцитонина может вызывать устойчивый обезболивающий эффект при болезнях костей (болезнь Педжета, остеопороз, опухолевые метастазы) или синдроме Зудека.
Гиперкальциемию можно устранить путем введения:
1) 0,9% раствора NaCI с фуросемидом (при необходимости) => почечная экскреция
2) кальцитонина клодроната (бисфосфоната), ингибирующего остеокласты => мобилизация Са 2+ из костей;
3) глюкокортикоидов.
Учебное видео расшифровки биохимического анализа крови
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в оглавление раздела «фармакология»
Что такое гиперпаратиреоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Курашова О. Н., терапевта со стажем в 27 лет.
Определение болезни. Причины заболевания
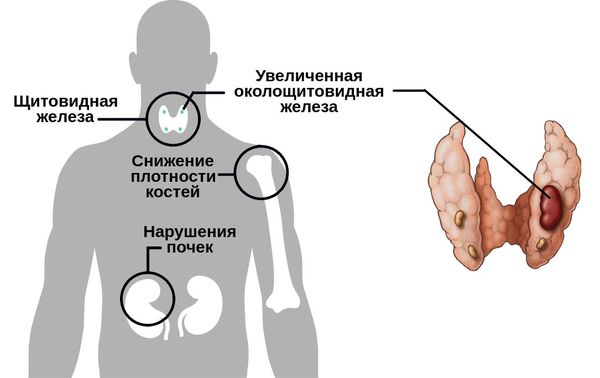
Гиперпаратиреоз — это эндокринное заболевание, развивающееся при чрезмерном количестве паратиреоидного гормона (паратгормона) в организме, который выделяется околощитовидными железами.
Существуют разные формы данного нарушения.
Первичный гиперпаратиреоз помимо нарушения околощитовидных желёз и избыточного выделения паратиреоидного гормона сопровождается верхне-нормальным или повышенным содержанием кальция в крови. Среди эндокринных заболеваний он встречается довольно часто: по распространённости эта форма гиперпаратиреоза находится на третьем месте после сахарного диабета и патологий щитовидной железы.
Ежегодная заболеваемость первичной формой составляет около 0,4–18,8% случаев на 10000 человек, а после 55 лет — до 2% случаев. [6] [12] У женщин эта патология возникает чаще, чем у мужчин — примерно 3:1. Преобладающее число случаев первичного гиперпаратиреоза у женщин приходится на первое десятилетия после менопаузы.
Первичный гиперпаратиреоз может быть как самостоятельным заболеванием, так и сочетаться с другими наследственными болезнями эндокринной системы. [1] [12] Он проявляется многосимптомным поражением различных органов и систем, что приводит к значительному снижению качества жизни с последующей инвалидизацией, а также к риску преждевременной смерти.
Причины возникновения связаны с развитием в одной или нескольких околощитовидных железах таких патологий, как:
В 5% случаев на возникновение первичного гиперпаратиреоза влияет наследственность.
При вторичном гиперпаратиреозе кроме общих клинических признаков заболевания отличается снижением кальция и повышением фосфора в крови. Эта форма болезни обычно развивается как реакция компенсации и сочетает в себе усиленный синтез паратгормона и изменения в паращитовидных железах. Как правило, обнаруживается при синдроме недостаточного всасывания кальция в тонком кишечнике, дефиците витамина D и хронической почечной недостаточности.
Третичный гиперпаратиреоз развивается в случае аденомы околощитовидной железы и повышенном выделении паратгормона в условиях длительного вторичного гиперпаратиреоза.
Псевдогиперпаратиреоз развиваться п ри других злокачественных опухолях, которые способны продуцировать вещество, похожее на паратгормон.
Симптомы гиперпаратиреоза
Гиперпаратиреоз протекает длительно и бессимптомно и может быть выявлен случайно во время обследования по поводу другого заболевания.
У пациентов с гиперпарат иреозом одновременно возникают симптомы поражения различных органов и систем: язва желудка, остеопорозные проявления, мочекаменная и желчнокаменная болезни и другие. При пальпации шеи в зоне паращитовидных желёз можно нащупать достаточно большую «аденому».
Развивается быстрая утомляемость при физической повседневной нагрузке, мышечная слабость, ноющая головная боль, затруднение при ходьбе (особенно во время подъёма по лестнице или при преодолении больших расстояний), формируется как бы переваливающаяся походка.
У большинства людей с гиперпаратиреозом нарушено восприятие и память, они эмоционально неуравновешенны, тревожны, депрессивны.
При опросе пациенты с подозрением на нарушение функции околощитовидных желёз обычно жалуются на:
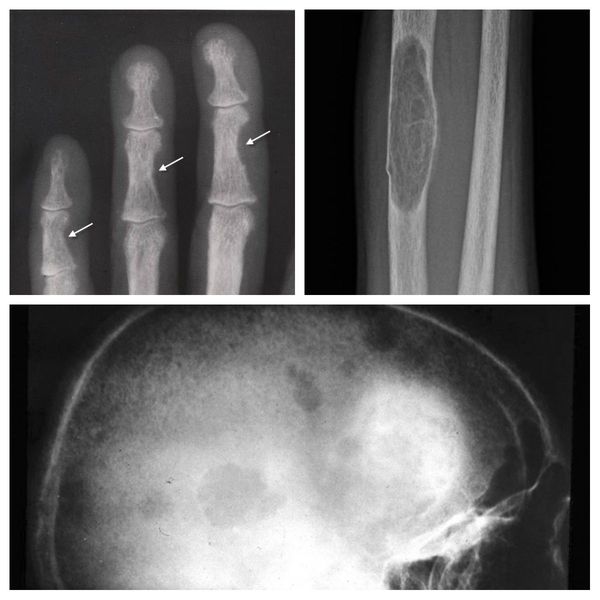
Если патологический процесс в костях продолжает развиваться, это может стать причиной расшатывания и выпадения здоровых зубов, а также деформации костей скелета, в связи с которой пациенты становятся ниже ростом. Возникающие переломы очень медленно восстанавливаются, часто с деформациями р ук и ног и образованием непрочных суставов. На конечностях появляются кальцинаты — результат отложения солей.
У женщин с повышенной функцией щитовидной железы в менопаузе риск костных осложнений возрастает.
В большинстве случаев первые проявления гиперпаратиреоза сопровождаются:
При развитии поражения сосудов в виде кальциноза и склероза нарушается питание тканей и органов, а повышенный уровень кальция в крови способствует развитию и ухудшению ишемической болезни сердца.
Гиперпаратиреоз с нехарактерными симптомами и постепенным началом часто сопровождается:
Патогенез гиперпаратиреоза
Кальций является важным компонентом, который влияет на прочность костей и обменные процессы в организме. В норме уровень кальция, а также фосфора поддерживает паратгормон, выделяемый околощитовидными железами.
При аденоме или ином нарушении этих желёз взаимосвязь кальция и паратгормона нарушается: если раньше повышенное содержания кальция сдерживало уровень паратгормона, то теперь развивается дефект рецепторов, чувствительных к кальцию, которые расположены на поверхности главных клеток паращитовидных желёз.
В связи с этим в организме происходит ряд нарушений:
При избытке паратгормона усиливается выведение из костной ткани кальция и фосфора. Клинически это проявляется изменениями в костях: их искривлением и размягчением, возникновением переломов. При этом уровень кальция в костях снижается, а его уровень в крови заметно увеличивается, т. е. возникает гиперкальциемия. Она проявляется мышечной слабостью, избыточным выделением минералов с мочой при усиленном мочеиспускании и постоянной жаждой, что приводит к почечнокаменной болезни и нефрокальцинозу — накоплению и отложению солей кальция в главной ткани почек. Также избыток кальция в крови становится причиной нарушения тонуса сосудов и возникновения артериальной гипертензии. [1] [12]
У пациентов с первичным гиперпаратиреозом часто наблюдается острая нехватка витамина D, а после оперативного лечения заболевания повышается вероятность развития синдрома голодных костей — последствия гиперкальциемии. [15]
Классификация и стадии развития гиперпаратиреоза
Как уже говорилось, бывает первичный, вторичный и третичный гиперпаратиреоз. При этом первичную форму заболевания разделяют на три вида:
Согласно МКБ 10, выделяют четыре формы заболевания:
Другая классификация гиперпаратиреоза, опубликованная в 2014 году, по степени выраженности симптомов разделяет заболевание на три формы:
В зависимости от того, какие именно органы или системы поражены, выделяют:
Осложнения гиперпаратиреоза
Длительное течение заболевания сказывается на формировании костей. Так, н а поздних стадиях вовремя не диагностированного гиперпаратиреоза наблюдаются:
Самое тяжёлое осложнение гиперпаратиреоза — гиперкальциемический криз. Он возникает внезапно после резкого повышения уровня кальция в крови до 3,5-5 ммоль/л (в норме этот показатель составляет 2,15-2,50 ммоль/л). [17] Проявляется резким обострением всех симптомов гиперпаратиреоза.
Пусковые механизмы осложнения — острые инфекционные заболевания (чаще всего ОРВИ), внезапный перелом, длительный постельный режим, беременность, бесконтрольный приём препаратов, содержащих кальций и витамин D, а также тиазидных мочегонных средств.
Риск возникновения криза зависит от того, насколько повышен уровень кальция в крови. [17]
Кальциопенические состояния и их коррекция
Кальций (Са) — один из важнейших элементов в организме человека, особенности его метаболизма обусловливают физиологический гомеостаз и нормальное функционирование практически всех систем организма [1]. Наибольшее значение содержание и состояние метаболизм
Кальций (Са) — один из важнейших элементов в организме человека, особенности его метаболизма обусловливают физиологический гомеостаз и нормальное функционирование практически всех систем организма [1]. Наибольшее значение содержание и состояние метаболизма кальция имеет в детстве, пожилом возрасте, а также в период беременности [2].
Общие сведения о кальции. Кальций является самым распространенным элементом в теле человека, поэтому его относят к «макроэлементам». Организм взрослого в норме содержит примерно 25 000 ммоль (примерно 1000 г) кальция, из них 99% входят в состав скелета. Общее содержание минеральных веществ в человеческом организме — около 5% от массы тела, а на долю Са приходится почти треть от их общего количества [3].
По химическим свойствам Са относится к элементам, образующим прочные соединения с белками, фосфолипидами, органическими кислотами и другими веществами.
Функции Са. Кальций выполняет многочисленные функции в минеральном обмене, но этим его свойства не ограничиваются. Принято выделять следующие наиболее важные функции: участие в формировании и поддержании структуры костной ткани и зубов; активизация ферментных систем, обеспечивающих гемокоагуляцию и мышечное сокращение; участие в регуляции трансмембранного потенциала клетки, нервной и нервно-мышечной проводимости; поддержание сердечной деятельности; регуляция продукции и высвобождения гормонов и нейропептидов (нейромедиаторов); регуляция сосудистого тонуса; контроль всех этапов каскада свертывания крови; участие в важнейших метаболических процессах (гликогенолиз, глюконеогенез, липолиз и т. д.); функционирование в качестве «информационной» молекулы для многих ферментативных реакций; стимуляция секреторного и инкреторного процессов пищеварительных и эндокринных желез; pегуляция тонуса симпатической и парасимпатической нервной системы; биологическая сигнализация об активации всех стадий клеточного цикла и транскрипции генов; регуляция процессов внутриклеточного метаболизма; обеспечение стабильности клеточных мембран; препятствование высвобождению медиаторов аллергического воспаления; выполнение пластической роли при формировании тканевых и клеточных структур; способствование клеточной адгезии; участие в формировании кратковременной памяти и обучающих навыков; активация апоптоза и транскрипционного аппарата клеток (кофактор эндонуклеаз, участвующих в деградации ДНК при апоптозе); важна роль кальция в иммунологической активности (активация лимфоцитов, в частности, бластная трансформация в ответ на стимуляцию митогенами) [1, 2, 3].
Абсорбция кальция. Всасывается из верхних отделов тонкого кишечника, чему способствуют витамин D, аскорбиновая кислота, лактоза и кислая среда.
Всасыванию Са препятствуют избыток щавелевой кислоты, фитиновой кислоты, жиров, пищевых волокон и фосфатов. Один из важнейших механизмов поддержания уровня Са в крови — его экскреция с мочой, зависящая от фильтрации минерала и реабсорбции в почках [1].
Регуляция метаболизма кальция. Гипокальциемия, независимо от вызвавших ее причин, сопровождается снижением экскреции Са. Предполагается, что уменьшение выведения Са с мочой может происходить за счет увеличения накопления минералов в костной ткани или других тканях организма.
На регуляцию содержания Са в крови оказывают влияние: гормоны (в первую очередь, паратиреоидный гормон (ПТГ) и кальцитриол); сывороточные белки; содержание фосфатов (РО 3- 4) в сыворотке крови (реципрокные взаимоотношения).
Кальций депонируется в трабекулах костей; динамическое равновесие кальция поддерживается ПТГ и тиреокальцитонином. Pегуляция кальциевого гомеостаза является одной из наиболее сложных интегративных реакций организма человека, в осуществлении которой ведущая роль принадлежит нервной системе и железам внутренней секреции [1, 3].
Кальций и центральная нервная система (ЦНС). Гомеостаз Са имеет прямое отношение к ЦНС. Наряду с другими микро- и макроэлементами Са играет значительную роль в нейрофизиологических процессах. Еще в 1928 г. А. А. Богомолец подчеркивал исключительную важность Са в регуляции тонуса симпатической и парасимпатической нервной системы [1].
В нервной системе Са имеет значение в модуляции активности рецепторов к нейромедиаторам и нейропептидам. Повышенное высвобождение Ca способствует ишемическому повреждению нейронов вследствие вазоконстрикции и инициации каскада апоптоза [1, 3, 4]. Конкурентные взаимоотношения между различными микроэлементами (Zn, Hg, Cu, Cd) и кальцием могут определять самые разнообразные биологические эффекты и, в конечном счете, — течение неврологических процессов [4].
При рассмотрении Са на клеточном уровне необходимо выделять его участие в регуляции ионной проницаемости мембраны нейрона, генерации возбуждения.
При гипокальциемии различного генеза могут отмечаться симптомы, имеющие отношение к сфере неврологии: отклонения в поведении; онеменение и парестезии; судороги; спазмы мышц; положительные симптомы Хвостека или Труссо (гипопаратиреоз) и т. д. Нарушениям обмена Са нередко сопутствуют фебрильные судороги, пароксизмы гипоксического, метаболического или эндокринного генеза, нейрофиброматоз (1-го типа), гидроцефалия, краниостеноз и ряд других видов патологии ЦНС [1, 4]. У детей первых лет жизни ярким примером кальциопенической соматоневрологической патологии является классический (витамин D-дефицитный) рахит [2].
Существуют данные, свидетельствующие о том, что действие Са зависит от типа нервной деятельности и ее функционального состояния. На необходимость коррекции нарушений содержания Са в организме детей грудного и раннего возраста при неврологических заболеваниях указывает Е. М. Мазурина (2005) [2].
Следует помнить, что избыточное накопление в организме Са может привести к нейротоксичности, угрозе патологической кальцификации стенок сосудов и тканей организма [3, 4].
Потребность в кальции. Ha первом году жизни она составляет (по разным данным) от 350 мг до 1000 мг/сут, на втором — 370–1000 мг/сут, на третьем — 300–1000 мг/сут. У детей более старшего возраста и взрослых она возрастает до 1000–1500 мг/сут [1, 2]. Внимания заслуживает то обстоятельство, что в разных странах мира рекомендации по суточной потребности в Са2+ значительно отличаются. По-видимому, это объясняется особенностями разных регионов (климато-географическими, экологическими и др.).
Алиментарное поступление Са имеет огромное значение в любом возрасте. J. C. Leblanc et al. (2005) изучены паттерны диетического потребления 18 элементов во Франции, a R. B. Ervin et al. (2004) — отдельных минеральных веществ в США [5, 6]. Применительно к Са они признаны неудовлетоворительными в обеих странах.
Нормы содержания кальция в организме. Считается, что около 70% Са экскретируется с калом, 10% — c мочой, а ретенция элемента составляет 15–25% (в зависимости от темпов роста).
Сывороточное содержание Са (в норме) равняется 9–11 мг%, причем 50–60% — в ионизированной форме. У здоровых детей независимо от возраста в сыворотке крови содержится 4,9–5,5 мг% (1,22–1,37 ммоль/л) ионизированного Ca, исходя их данных, полученных с использованием ион-селективных электродов. Экскреция Са с калом (при следовании обычной диете) составляет менее 140 ммоль/сутки (560 мг/сутки). Определяется прямая зависимость содержания Са в кале от особенностей диеты.
Содержание Са в моче также находится в прямой зависимости от количества алиментарно потребляемого элемента. В частности, при нормальной диете суточная экскреция равняется 2,5–7,5 ммоль/сут (100–300 мг/сут, 5–15 мЭкв/сут). При потреблении Са на уровне менее 200 мг/сут — 0,33–4,5 ммоль/сут (13–180 мг/сут), 200–600 мг/сут — 1,25–5,0 ммоль/сут (50–200 мг/сут), 1000 мг/сут — 7,5 ммоль/сут (до 300 мг/сут) [1, 2].
Снижение содержания кальция в физиологических средах организма. Наиболее значимо снижение Са в сыворотке крови. В этой физиологической жидкости Са представлен тремя следующими формами: связанный с белками (недиффундирующий — 30–55%); хелатированный (диффундирующий, но неионизированный — около 15%); ионизированный Са (около 30–55%) [3].
Физиологическое снижение содержания Са в крови может отмечаться при повышенной утилизации углеводов или назначении инсулина. Патологическое снижение содержания Са свойственно следующим клиническим ситуациям: гипопаратиреоидизм (следствие хирургического вмешательства в области паращитовидных желез); псевдогипопаратиреоидизм; дефицит витамина D; стеаторея (сочетанные нарушения абсорбции витамина D, Ca и РО 3- 4); нефрит (снижение неионизированной фракции Са, переносимой белками сыворотки, по-видимому вследствие потери Са с мочой); болезни почек с ретенцией фосфатов; острый панкреатит; внутривенное введение солей Mg, оксалатов или цитратов; остеопороз у пожилых людей (нижняя граница нормы); неонатальная гипокальциемия (первый день жизни — вследствие низкой массы тела при рождении, острой интранатальной асфиксии, наличия у матери сахарного диабета, гиперпаратиреоза или нелеченой целиакии; недоразвития плаценты, гестоза, оперативных родов посредством кесарева сечения, при заменных переливаниях крови; 5–10 день — вследствие гиперфосфатемии, вызванной потреблением коровьего молока или малоадаптированных смесей на его основе); гипомагниемия; длительный прием антиконвульсантов (обычно при эпилепсии); состояние после удаления щитовидной железы; болезнь Педжета — при лечении кальцитонином. Особое внимание в отечественной и зарубежной литературе различных лет уделяется кальциопеническим состояниям при остеопорозе и сходных с ним видах костной патологии [1].
Снижение содержания Са в кале обнаруживается в следующих случаях: остеомаляция, успешно вылеченная препаратами витамина D; гипервитаминоз D; низкое содержание фосфора в рационе питания; саркоидоз Бека (в некоторых случаях).
В моче снижение содержания Са возможно при низком потреблении этого макроэлемента с пищей, а кроме того, нередко отмечается на поздних сроках беременности.
Концентрация Са в спинномозговой жидкости (СМЖ) составляет около 1/2 от сывороточного содержания. Изменения в содержании Са в СМЖ невелики, а их регистрация не имеет большого значения для диагностики различных патологических состояний. Уровень Са в СМЖ может снижаться у некоторых пациентов с эпилепсией, длительно получающих терапию фенитоином и другими аниэпилептическими препаратами (АЭП). Практически все известные к настоящему времени АЭП обладают Са-изгоняющими свойствами. Дети грудного и раннего возраста, страдающие эпилепсией, наиболее подвержены риску гипокальциемии [1].
Методы коррекции кальциопенических состояний. Если при острых нарушениях концентрации Са в сыворотке крови тактика лечения уже давно разработана и является почти хрестоматийной, то в области профилактики и коррекции умеренной гипокальциемии до сих пор отмечается определенный пробел.
В различных областях медицины нередко имеет место эмпирический подход к данной проблеме. Попытки компенсировать индуцированный приемом антиконвульсантов дефицит Са за счет приема антиэпилептических препаратов, в состав которых включены соли кальция, в подавляющем большинстве случаев малоэффективны. Так, одна 300-миллиграммовая таблетка препарата Конвульсофин содержит всего 33 мг кальциевой соли, а в составе Паглюферала обнаруживается 250 мг глюконата Са (в составе глюферала — 200 мг). Указанные количества макроэлемента явно недостаточны для нивелирования Са-изгоняющих эффектов этих антиэпилептических средств.
Широкая распространенность, мультифакториальность и потенциальная предотвратимость кальциопенических состояний предполагают необходимость совершенствования методов их профилактики и коррекции. J.-Y. Reginster et al. (2002) подчеркивает влияние ежедневного приема Са и витамина D на секрецию гормонов паращитовидной железой [7]. Сомнения относительно существующих рекомендаций по профилактическому приему препаратов Са и витамина D высказывали A. Prentice (2002) и J. A. Amorim Cruz (2003) [8, 9]. H. L. Newmark et al. (2004) считают необходимым добавление Са и кальциферола в зерновые продукты промышленного производства [10]. В отличие от профилактики кальциопенических состояний, в их коррекции диета малоэффективна. Поэтому для коррекции дефицита Са в организме используются препараты, содержащие этот макроэлемент [1, 2].
Препараты кальция, используемые в медицине, и показания к их применению. В используемых справочниках лекарственных средств приводятся следующие основные формы кальция: хлорид, глюконат, лактат, карбонат и цитрат, хотя данный макроэлемент может быть представлен и другими соединениями (кальция фолинат, ацетат, g-гидроксибутират, глицерофосфат, глутаминат, добезилат, пангамат, пантотенат, тринатрия пентенат, фосфат и др.) [11, 12, 13].
В числе показаний к назначению основных перечисленных препаратов Са фигурируют следующие: недостаточная функция паращитовидных желез, сопровождающаяся тетанией или спазмофилией; усиленное выделение Са из организма (при длительной обездвиженности больных, синдромах мальабсорбции или приеме АЭП); аллергические заболевания; уменьшение проницаемости сосудов; кожные заболевания; паренхиматозный гепатит; токсические поражения печени; нефрит; гиперкалиемическая форма пароксизмальной миоплегии; хроническая почечная недостаточность; остеопороз [11, 12, 13].
В литературе последних лет представлены и другие показания к применению препаратов Са: синдром хронической усталости; сахарный диабет; артериальная гипертензия у детей с солевой чувствительностью. Помимо этого, кальций может назначаться для повышения свертываемости крови (как гемостатическое средство). В качестве показаний к использованию препаратов Са необходимо привести различные виды рахита (витамин D-зависимый, витамин D-резистентный, витамин D-дефицитный, остеопения маловесных детей и т. д.) [1].
К сожалению, даже при продолжительном назначении препаратов, обладающих Са-изгоняющим действием, а также других лекарственных средств, индуцирующих гипокальциемию, рутинной коррекции уровня кальция обычно не проводится, а в существующих рекомендациях подобной процедуры не предусмотрено.
Положительный эффект препаратов кальция проявляется только при индивидуальном подборе их дозировки. При назначении всегда необходимо учитывать утилизацию (усвоение) данного макроэлемента, выраженную в процентах от назначаемого количества. В частности, для глюконата, лактата и хлорида кальция она составляет соответственно 9%, 13% и 27%. Для карбоната и цитрата кальция характерны более высокие показатели всасывания из кишечника. B. W. Downs et al. (2005) cообщают о высокой биологической эффективности новой соли на основе кальций-калиевого соединения гидроксицитрусовой кислоты [14].
Литература
В. М. Студеникин, доктор медицинских наук, профессор
Э. М. Курбайтаева
НЦЗД РАМН, Москва