Что будет если смешать азотную и серную кислоту
Особые свойства азотной и концентрированной серной кислоты.
При нагревании азотная кислота распадается по той же реакции. Азотную кислоту можно перегонять (без разложения) только при пониженном давлении.
Азотная кислота является сильным окислителем, концентрированная азотная кислота окисляет серу до серной, а фосфор — до фосфорной кислоты, некоторые органические соединения (например, амины и гидразин, скипидар) самовоспламеняются при контакте с концентрированной азотной кислотой.
Степень окисленности азота в азотной кислоте равна 4-5. Выступая в качестве окислителя, НNО 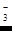
Какое из этих веществ образуется, т. е. насколько глубоко восстанавливается азотная кислота в том или ином случае, зависит от природы восстановителя и от условий реакции, прежде всего от концентрации кислоты. Чем выше концентрации HNO 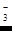
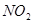
При взаимодействии разбавленной азотной кислоты с малоактивными металлами, например, с медью, выделяется NO. В случае более активных металлов — железа, цинка, — образуется 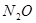
Золото, некоторые металлы платиновой группы и тантал инертны к азотной кислоте во всём диапазоне концентраций, остальные металлы реагируют с ней, ход реакции при этом определяется её концентрацией. Так, концентрированная азотная кислота реагирует с медью с образованием диоксида азота, а разбавленная — оксида азота (II):
Cu + 4HNO3—-> Cu(NO3)2 + NO2 + 2H2O
Большинство металлов реагируют с азотной кислотой с выделением оксидов азота в различных степенях окисления или их смесей, разбавленная азотная кислота при реакции с активными металлами может реагировать с выделением водорода и восстановлением нитрат-иона до аммиака.
Некоторые металлы (железо, хром, алюминий), реагирующие с разбавленной азотной кислотой, пассивируются концентрированной азотной кислотой и устойчивы к её воздействию.
Смесь азотной и серной кислот носит название «меланж». Азотная кислота широко используется для получения нитросоединений.
Смесь трех объёмов соляной кислотой и одного объёма азотной называется «царской водкой». Царская водка растворяет большинство металлов, в том числе и золото. Её сильные окислительные способности обусловлены образующимся атомарным хлором и хлоридом нитрозила:
Серная кислота – тяжелая маслянистая жидкость, не имеющая цвета. Смешивается с водой в любых отношениях.
Концентрированная серная кислота активно поглощает воду из воздуха, отнимает её от других веществ. При попадании органических веществ в концентрированную серную кислоту происходит их обугливание, например, бумаги:
(C6H10O5)n + H2SO4 => H2SO4 + 5nH2O + 6C
При взаимодействии концентрированной серной кислоты с сахаром образуется пористая угольная масса, похожая на черную затвердевшую губку:
C12H22O11 + H2SO4 => C + H2O + CO2 + Q
Химические свойства разбавленной и концентрированной серной кислоты отличаются.
Разбавленныерастворы серной кислоты реагируют с металлами, расположенными в электрохимическом ряду напряжений левее водорода, с образованием сульфатов и выделением водорода.
Концентрированные растворы серной кислоты проявляют сильные окислительные свойства, обусловленные наличием в её молекулах атома серы в высшей степени окисления (+6), поэтому концентрированная серная кислота является сильным окислителем. Так окисляются некоторые неметаллы:
S + 2H2SO4 => 3SO2 + 2H2O
C + 2H2SO4 => CO2 + 2SO2 + 2H2O
P4 + 8H2SO4 => 4H3PO4 + 7SO2 + S + 2H2O
H2S + H2SO4 => S + SO2 + 2H2O
Она взаимодействует с металлами, расположенными в электрохимическом ряду напряжений металлов правее водорода (медь, серебро, ртуть), с образованием сульфатов, воды и продуктов восстановления серы. Концентрированные растворы серной кислоты не реагируют с золотом и платиной вследствие их малой активности.
а) малоактивные металлы восстанавливают серную кислоту до диоксида серы SO2 :
Cu + 2H2SO4 => CuSO4 + SO2 + 2H2O
2Ag + 2H2SO4 => Ag2SO4 + SO2 + 2H2O
б) с металлами средней активности возможны реакции с выделением любого из трех продуктов восстановления серной кислоты:
Zn + 2H2SO4 => ZnSO4 + SO2 + 2H2O
3Zn + 4H2SO4 => 3ZnSO4 + S + 4H2O
4Zn + 5H2SO4 => 4ZnSO4 + H2S + 2H2O
в) с активными металлами могут выделяться сера или сероводород:
8K + 5H2SO4 => 4K2SO4 + H2S + 4H2O
6Na + 4H2SO4 => 3Na2SO4 + S + 4H2O
2Fe + 6H2SO4 => Fe2(SO4)3 + 3SO2 + 6H2O
2Al + 6H2SO4 => Al2(SO4)3 + 3SO2 + 6H2O
Получение кислот.
1. Бескислородные кислоты получают путем синтеза водородных соединений неметаллов из простых веществ и последующего растворения полученных продуктов в воде
Неметалл + H2 = Водородное соединение неметалла
2. Оксокислоты получают взаимодействием кислотных оксидов с водой.
Кислотный оксид + H2O = Оксокислота
3. Большинство кислот можно получить взаимодействием солей с кислотами.
Соль + Кислота = Соль + Кислота
Основания– это сложные вещества, молекулы которых состоят из атома металла и одной или нескольких гидроксидных групп.
6.Классификация оснований:
1.По числу гидроксильных групп в молекуле:
а)· Однокислотные, молекулы которых содержат одну гидроксидную группу.
б)· Двухкислотные, молекулы которых содержат две гидроксидные группы.
в)· Трехкислотные, молекулы которых содержат три гидроксидые группы.
2. По растворимости в воде: Растворимые и Нерастворимые.
7.Физические свойства оснований:
Все неорганические основания– твердые вещества (кроме гидроксида аммония). Основания имеют разный цвет: гидроксид калия—белого цвета, гидроксид меди—голубого, гидроксид железа—красно-бурого.
Растворимые основания образуют мыльные на ощупь растворы, через что эти вещества получили название щелочь.
Щёлочи образуют лишь 10 элементов периодической системы химических элементов Д. И. Менделеева: 6 щелочных металлов – литий, натрий, калий, рубидий, цезий, франций и 4 щелочноземельных металла – кальций, стронций, барий, радий.
8.Химические свойства оснований:
2. Взаимодействуют :
а) с кислотами: Основание + Кислота = Соль + H2O
KOH + HCl = KCl + H2O
б) с кислотными оксидами: Щелочь + Кислотный оксид = Соль + H2O
в) с растворами: Раствор щелочи + Раствор соли = Новое основание + Новая соль
г) с амфотерными металлами: Zn + 2NaOH = Na2ZnO2 + H2
а) Реагируют с кислотами с образованием соли и воды:
Гидроксид меди (II) + 2HBr = CuBr2 + вода.
Zn(OH)2 + 2CsOH = соль + 2H2O.
Нерастворимые в воде основания при нагревании разлагаются на основной оксид и воду:
Нерастворимое основание = Основной оксид + H2O
Соли– это продукты неполного замещения атомов водорода в молекулах кислот атомами металла или это продукты замещения гидроксидных групп в молекулах оснований кислотными остатками.
Классификация:
Нормальные соли. Это продукты полного замещения атомов водорода в молекуле кислоты атомами неметалла, или продукты полного замещения гидроксидных групп в молекуле основания кислотными остатками.
Кислые соли. Это продукты неполного замещения атомов водорода в молекулах многоосновных кислот атомами металла.
Основные соли.Это продукты неполного замещения гидроксидных групп в молекулах многокислотных оснований кислотными остатками.
Типы солей:
Двойные соли — в их составе присутствует два различных катиона, получаются кристаллизацией из смешанного раствора солей с разными катионами, но одинаковыми анионами.
Смешанные соли — в их составе присутствует два различных аниона.
Гидратные соли (кристаллогидраты) — в их состав входят молекулы кристаллизационной воды.
Комплексные соли — в их состав входит комплексный катион или комплексный анион.
Физические свойства:
Большинство солей—твердые вещества белого цвета. Некоторые соли имеют окраску. Например, дихромат калия—оранжевого, сульфат никеля—зеленого.
По растворимости в воде соли делятся на растворимые в воде, малорастворимые в воде и нерастворимые.
Химические свойства:
Растворимые соли в водных растворах диссоциируют на ионы:
1. Средние соли диссоциируют на катионы металлов и анионы кислотных остатков:
· Кислые соли диссоциируют на катионы металла и сложные анионы:
· Основные металлы диссоциируют на сложные катионы и анионы кислотных остатков:
2. Соли взаимодействуют с металлами с образованием новой соли и нового металла: Ме(1) + Соль(1) = Ме(2) + Соль(2)
3. Растворы взаимодействуют с щелочами Раствор соли + Раствор щелочи = Новая соль + Новое основание:
4. Соли взаимодействуют с кислотами Соль + Кислота = Соль + Кислота:
5. Соли могут взаимодействовать между собой Соль(1) + Соль(2) = Соль(3) + Соль(4):
6. Основные соли взаимодействуют с кислотами Основная соль + Кислота = Средняя соль + H2O:
7. Кислые соли взаимодействуют с щелочами Кислая соль + Щелочь = Средняя соль + H2O:
8. Многие соли разлагаются при нагревании: MgCO3 = MgO + CO2
Представители солей и их значение:
Соли повсеместно используются как в производстве, так и в повседневной жизни:
— Соли соляной кислоты. Из хлоридов больше всего используют хлорид натрия и хлорид калия.
— Хлорид натрия (поваренную соль) выделяют из озерной и морской воды, а также добывают в соляных шахтах. Поваренную соль используют в пищу. В промышленности хлорид натрия служит сырьём для получения хлора, гидроксида натрия и соды.
— Хлорид калия используют в сельском хозяйстве как калийное удобрение.
— Соли серной кислоты. В строительстве и в медицине широко используют полуводный гипс, получаемый при обжиге горной породы (дигидрат сульфата кальция). Будучи смешан с водой, он быстро застывает, образуя дигидрат сульфата кальция, то есть гипс.
— Декагидрат сульфата натрия используют в качестве сырья для получения соды.
— Соли азотной кислоты. Нитраты больше всего используют в качестве удобрений в сельском хозяйстве. Важнейшим из них является нитрат натрия, нитрат калия,нитрат кальция и нитрат аммония. Обычно эти соли называют селитрами.
— Из ортофосфатов важнейшим является ортофосфат кальция. Эта соль служит основной составной частью минералов — фосфоритов и апатитов. Фосфориты иапатиты используются в качестве сырья в производстве фосфорных удобрений,например, суперфосфата и преципитата.
— Соли угольной кислоты. Карбонат кальция используют в качестве сырья для получения извести.
— Карбонат натрия (соду) применяют в производстве стекла и при варке мыла.
— Карбонат кальция в природе встречается и в виде известняка, мела и мрамора.
Материальный мир, в котором мы живем и крохотной частичкой которого мы являемся, един и в то же время бесконечно разнообразен. Единство и многообразие химических веществ этого мира наиболее ярко проявляется в генетической связи веществ, которая отражается в так называемых генетических рядах.
Генетической называют связь между веществами разных классов, основанную на их взаимопревращениях.
Если основу генетического ряда в неорганической химии составляют вещества, образованные одним химическим элементом, то основу генетического ряда в органической химии (химии углеродных соединений) составляют вещества с одинаковым числом атомов углерода в молекуле.
Контроль знаний:
1.Дать определение солям, основаниям, кислотам, их характеристику, основных характерных реакций.
2.Почему кислоты и основания объединяются в группу гидроксиды? Что у них общего и чем они отличаются? Почему щелочь нужно приливать к раствору соли алюминия, а не наоборот?
3. Задание: Приведите примеры уравнений реакций, иллюстрирующих указанные общие свойства нерастворимых оснований.
4. Задание: Определите степень окисления атомов металлических элементов в приведенных формулах. Какая закономерность прослеживается между их степенью окисления в оксиде и основе?
ДОМАШНЕЕ ЗАДАНИЕ:
Проработать: Л2.стр.162-172,пересказ конспекта лекции №5.
Лекция № 6.
Тема: Металлы. Положение металлических элементов в периодической системе. Нахождение металлов в природе. Металлы. Взаимодействие металлов с неметаллами (хлором, серой и кислородом).
Оборудование: периодическая система химических элементов, коллекция металлов, ряд активности металлов.
План изучения темы
(перечень вопросов, обязательных к изучению):
2. Металлы как простые вещества. Металлическая связь, металлические кристаллические решетки.
3. Общие физические свойства металлов.
4. Распространенность металлических элементов и их соединений в природе.
Что будет если смешать азотную и серную кислоту
Из них в настоящее время известны только два — одноазотный и трехазотный. Первый, получаемый при смешении глицерина с умеренно разведенной азотной кислотой (1ч. HNO 3 на 3 ч. Н 2 O) представляет жидкость, легко растворимую в воде и спирте, почти не растворимую в эфире и не взрывающуюся от удара. Трехазотный эфир получается при действии на глицерин смеси наиболее крепких кислот азотной и серной и отличается от предыдущего по своему отношению к растворителям, и в особенности по чрезвычайно сильной взрывчатости при быстром нагревании и ударе. Этот последний эфир и есть то могущественное взрывчатое вещество, которое впервые было приготовлено Собреро в лаборатории Пелуза в 1847 г. и с тех пор во взрывчатой технике называется Н. В числе первых лиц, давших толчок к применению его в практике, следует назвать профессора Зинина (1854 г.) и поручика артиллерии (впоследствии ген.-лейтенанта) В. Ф. Петрушевского, но главная заслуга в этом отношении бесспорно принадлежит шведскому инж. Альфреду Нобелю, который изобрел способ (превращением в динамиты) делать его достаточно безопасным при перевозке и обращении. В настоящее время производство Н. представляет одну из видных отраслей обрабатывающей промышленности.
1) Для приготовления нитроглицерина применяется общая реакция получения азотно-кислых эфиров алкогольных веществ, т. е. действие на глицерин (1 часть) крепкой азотной кислотой (3 части) в присутствии концентрированной серной кислоты (6 частей):
Приcутствие серной кислоты необходимо при этом, с одной стороны, для поглощения выделяющейся при реакции воды, которая, в противном случае, разжижая азотную кислоту, тем самым препятствовала бы полноте нитрации (стали бы получаться неполные азотные эфиры глицерина), с другой — для выделения образующегося Н. из раствора в азотной кислоте, так как он, будучи хорошо растворим в этой кислоте, не растворяется в смеси ее с серной. Эта реакция образования Н. сопровождается значительным самонагреванием, потому что, как самая этерификация глицерина азотной кислотой, так и соединение образующейся воды с серной кислотой отделяют тепло. Если бы вследствие самонагревания температура смеси повысилась до 50°, то действие кислот легко направилось бы в другую сторону: началось бы окисление глицерина и Н., сопровождающееся бурным выделением окислов азота (красно-бурых паров) и еще большим самонагреванием, которое могло бы окончательно привести к взрыву образовавшегося нитроглицерина. Поэтому реакцию должно вести при постоянном охлаждении смеси кислот и глицерин прибавлять к последней понемногу, размешивая каждую прилитую порцию. Образующийся непосредственно при соприкосновении с кислотами Н., обладая меньшим уд. весом (1,6) сравнительно с кислотной смесью (не менее 1,7), всплывает на поверхность, откуда и может быть собран по окончании реакции. Но самонагреванию при приготовлении Н. можно противодействовать и другим способом, именно — заставляя часть тепла выделиться ранее самого образования Н. и в особенности — замедляя реакцию этого образования предварительным изменением химического состояния реагирующих веществ. Бутми и Фоше достигли этого, приготовляя предварительно две отдельные смеси — серно-глицериновую и серно-азотную. Последняя составляется из равных частей Н 2 SО 4 н HNO 3, а первая из одной части С 3H5 (НО) 3 с тройным количеством H 2SO4, при чем образуется серно-глицериновый эфир C 3H5(HO)2HSO4 со значительным отделением тепла. Если обе смеси, после охлаждения, смешать между собой в такой пропорции, чтобы отношение количеств C 3H5 (НО) 3, Н 2 SО 4 и HNO 3 было приблизительно такое же, как в предыдущем способе, то: а) превращение серно-глицеринового эфира в Н. идет постепенно и медленно, так что оканчивается только через 12 и даже 24 часа, б) количество отделяемого тепла в течение всего этого процесса значительно понижается, так как та часть теплоты, которая происходит вследствие соединения воды с серной кислотой, уже выделилась ранее при образовании серно-глицериновой смеси, и с другой стороны, сам глицерин, превратившись в серно-глицериновый эфир, потерял тогда же часть своей энергии в виде тепла. Вследствие обеих приведенных причин приготовление Н. по этому способу и не может сопровождаться значительным разогреванием, так как пониженное количество теплоты при замедленном течении реакции успевает передаваться окружающей среде. Причина, почему система трех тел С 3H5 (НО) 3, H2SO4 и HNO 3, независимо от начального состояния, превращается так, что глицерин предпочтительно соединяется с азотной кислотой, а серная кислота — с выделяющейся водой, по толковании Бертело, заключается в том, что именно такая окончательная система тел отвечает наибольшему отделению тепла, т. е. принимаемому этим ученым принципу максимума работы, как общему правилу хода химических реакций. В действительности же вопрос сложнее, ибо и в реакции образования Н., как и в громадном большинстве других реакций, наблюдается обычное действие общего закона химических масс. В самом деле, опыты показывают, что из данного количества глицерина, при обыкновенных условиях приготовления, никогда не получается теоретического выхода трехазотного его эфира, а именно: из 100 ч. С 3H5 (НО) 3 не более 234, а обыкновенно около 210 ч. вместо 247. Это объясняется тем, что, по мере прибавления данного количества глицерина, в кислотной смеси остается все меньше и меньше HNO 3, между тем как масса H 2SO4 остается одной и той же, пока не наступает, наконец, такое отношение между количествами той и другой кислоты, при котором, в присутствии выделенной ранее воды, глицерин превращается в неполные азотные эфиры или даже совсем перестает нитроваться, образуя только серно-кислый эфир.
Заводское приготовление Н. может производиться по обоим указанным способам. Но способ Бутми и Фоше, примененный вскоре после его появления на нескольких заводах (франц. — в Вонже; бельг. — в Намюре, англ. — в Памберее), ныне совсем оставлен, как менее выгодный (выход продукта только 190 ч. из 100 ч. глицерина) и притом (судя по несчаст. случаям на этих заводах) не более безопасный сравнительно с обыкновенным способом, тем более, что при таком продолжительном соприкосновении Н. с кислотами (12 — 24 час.), какое имеет место при нитровании по этому способу, все-таки не предотвращается возможность развития реакции окисления с бурным выделением окислов азота. Что же касается обыкновенного способа, то, будучи вообще более выгодным в экономическом отношении, он, в то же время, теперь считается и более безопасным при надлежащей чистоте исходных материалов. Форма, в какой он применяется на заводах, может быть очень различна в своих подробностях. Сначала приготовляли Н. обыкновенно малыми порциями подобно тому, как это делается в лабораториях. Так, по Коппу, к 2 8 00 г кислотной смеси в глиняном или чугунном горшке, помещенном в сосуд с водой (5 — 6 литров), приливают 350 г глицерина из кружки при постоянном размешивании стеклянной или железной палочкой; получившуюся смесь переливают в разделительную воронку и выпускают отстоявшиеся кислоты, а Н. выливают в вышеозначенный сосуд с водой для промывания. Позднее стали, с одной стороны, увеличивать порции обрабатываемого за один раз глицерина, с другой — применять для размешивания при нитровании различные механические приспособления. Важным усовершенствованием в последнем отношении явилось применение (в первый раз на фабрики Мовбрея в Массачусетсе) продувания смеси сжатым воздухом, который производит не только перебалтывание, но и охлаждение вследствие своего расширения: в глиняные горшки, помещенные в общей водяной ванне кругом вытяжной трубы, наливается по 7 — 8 кг кислотной смеси обыкновенного состава, см. выше), и к этой смеси приливается по 0,8 кг глицерина с помощью сифонов из бутылей, поставленных на полке; при этом в каждый горшок по особой трубки проводится струя сжатого воздуха. С 1880 г. начали переходить к способам, в которых подвергаются обработке зараз большие количества глицерина, как это делается на заводах Нобеля, что опишем подробнее.
Исходные материалы, т. е. кислоты азотная, серная и глицерин, должны быть возможно чистые и безводные, именно: серная кислота уд. в. 1,84 с содержанием не менее 95 — 96% H 2SO4, азотная — уд. веса 1,50 с содержанием не мене 93% НNO 3 и глицерин уд. в. 1,26 с содержанием не более 3% воды. Такие примеси, как значительные количества азотноватой окиси в азотной кислоте или присутствие жирных кислот в глицерине, особенно вредны, так как они способствуют возбуждению опасных реакций окисления и препятствуют чистоте промывки приготовляемого Н. Приготовление кислотной смеси производится в больших цилиндрических чугунных сосудах с мешалками внутри или без мешалок. В последнем случае сначала вливается все отвешенное количество азотной кислоты, серная же кислота в соответственном количестве прибавляется после, причем вследствие разницы уд. весов обеих кислот местных разогреваний, однородность смешения достигается сама собой. Пропорция смешения, применяемая в настоящее время — на 1 ч. азотной кислоты ок. 1,666 ч. (большей частью) или 2 ч. (реже) серной кислоты. Из сосудов для смешивания смесь переводится в нитрационные аппараты или самотеком, или же с помощью толстостенных чугунных пневматических подъемников (montejus). Относительные количества при нитровании — на 1 ч. глицерина от 8 до 8,5 ч. кислотной смеси. Это количество смеси — значительно больше требуемого теорией, так как в 8 — 8,5 частях ее содержится около 3 ч. HNO 3, между тем как по теории для превращения 1 ч. глицерина в Н. требуется этой кислоты только 2,05 частей. При большом производстве азотная кислота обыкновенно приготовляется на том же заводе из чилийской селитры с помощью отработанной кислотной смеси. Самое нитрование глицерина производится в нитрационном аппарате (фиг. 1).
Он состоит из свинцового сосуда А, помещенного в деревянном чане В и закрывающегося съемной свинцовой крышкою I, которая при работе замазывается цементом. Через крышку проходят: концы двух свинцовых змеевиков D, находящихся внутри аппарата и назначаемых для охлаждения смеси посредством протекающей через них холодной воды; трубки С, приводящей в аппарат сжатый холодный воздух для размешивания при работе; труба F, отводящая из аппарата пары азотной кислоты; термометры Е, из которых один доходит почти до дна, а другой погружен только в верхний слой жидкости; трубка G для наливания отмеренного количества кислотной смеси; трубка Н для приливания глицерина, согнутая у дна аппарата в кольцо, с мелкими отверстиями. Кроме того, в крышке несколько стеклянных оконцев L для наблюдения за явлениями, происходящими в аппарате. Подобное же оконце J устроено и в вытяжной трубе для наблюдения бурых паров окислов азота, образующихся в случаях развития в аппарате опасных реакций окисления или так наз. разложения Н. Сосуд M служит для отмеривания количества глицерина, определяемого по указательной трубке N, а также для впрыскивания его в кислотную смесь посредством сжатого (до 2 атмосф.) воздуха, впускаемого по трубки О. Через кран К жидкость выпускается из аппарата. Холодная вода при работе проводится не только через внутренний змеевик, но и через кольцеобразное пространство между свинцовыми и деревянными наружными станками. За один раз обрабатывают 150 кг глицерина. Впустив требуемое количество кислотной смеси и охладив ее (пропусканием холодного сжатого воздуха и током воды) до 15 — 20°, начинают вбрызгивание глицерина (с температурой не ниже 20°), регулируя приток его таким образом, чтобы нагревание в аппарате не поднималось выше 25 — 30°. Если температура продолжает повышаться, приближаясь к означенному пределу даже по прекращении притока глицерина, то усиливают пропускание холодного воздуха, а если и после того поднятие не останавливается, то содержимое аппарата быстро выпускается в большой чан с водой; в противном случае легко может начаться разложение H., могущее окончиться взрывом. Вся операция обработки глицерина кислотами, считая наполнение смесью и опоражнивание, требует не более 1 — 1 1 /2 часа времени. Отделение Н. от кислот производится отстаиванием их смеси в так наз. сепараторе (фиг. 2).
Это — свинцовый четырехугольный ящик с коническим дном, вставленный в такой же деревянный ящик А. В крышке находятся: вытяжная труба D с оконцем Е; трубка К для введения смеси из нитрационного аппарата; отверстие для вставления термометра и несколько оконцев. Такое же оконце J с плотно заделанным стеклом находится и на боковой стенке для наблюдения уровней кислоты и всплывающего Н. От конического дна сосуда идет трубка G с оконцем F и кранами Н. Всплывание Н. на поверхность кислот происходит легче, если по мере выделения спускать его через кран J в рядом стоящий промывочный чан L. Присутствие посторонних примесей, напр. жиров в глицерине, серно-кислого свинца и т. п., затрудняет выделение. При нормальных условиях, с чистыми материалами, операция продолжается около 30 мин. По окончании сливания почти всей массы Н. выпускают кислотную смесь через один из нижних кранов, пока в оконце F не появятся слой мутной смеси, состоящей из примесей и различных низших нитропродуктов. В этот момент закрывают кран и выпускают остаток смеси в подходящий сосуд для переноса в чан L. Низшие нитропродукты, образующиеся из самого глицерина или посторонних примесей, обладают меньшим уд. весом сравнительно с Н., всплывают на нем в виде пены и являются особенно склонными к разложению со значительным отделением тепла при действии воздуха. Это нужно иметь в виду при производстве отделения Н., так как присутствие означенной пены может вызвать разложение и внутри сепаратора; тогда в оконце Е появляются красно-бурые пары и температура начинает сама собой подниматься. В таких случаях содержимое выпускается через третий нижний кран в большой чан с водой, как при разложениях в нитрационном аппарате.
Промывание Н., отделенного от избытка кислот, производится в два приема. Сначала подвергают его предварительной промывке в вышеупомянутом чане L. Это — цилиндрический свинцовый сосуд с наклонным дном и двумя кранами М, из которых нижний назначен для выпуска Н., а верхний для выливания воды. Перебалтывание производится помощью сжатого (до 2 атмосф.) воздуха, впускаемого по трубе N, которая внизу загнута и снабжена рядом мелких отверстий. Отстаивание, вследствие большой разницы уд. весов воды и Н., происходит быстро. Начальная температура воды должна быть ок. 15°, а во время приливания Н. не должна подниматься выше 30°. После первой промывки таким же образом производят вторую и третью; в последний раз промывают еще в 2,5% растворе соды, наливая этот раствор слоем в несколько сантиметров толщиной. Для окончательного удаления кислоты, Н. спускается в деревянные чаны, выложенные внутри свинцом и по своему устройству подобные предыдущему чану. Употребляя тройной объем воды, здесь производят от 10 до 18 промывок по 15 мин. каждую с перебалтыванием смеси с помощью сжатого воздуха (или механических мешалок); при 3-й и 5-й промывках вместо воды берется 1% раствор соды. Наиболее благоприятная температура воды 25 — 33°; на некоторых заводах первая промывка ведется при 50°. Продукт считается хорошо промытым, если он выдерживает нижеописанное испытание на стойкость при нагревании. Последняя операция при фабрикации состоит в фильтровании Н. для обезвоживания и удаления случайных твердых примесей. С этою целью его пропускают через специальные фильтры (фиг. 3).
В крышку деревянного, выложенного внутри свинцом, цилиндрического сосуда А с наклоненным дном вставлен фильтрационный свинцовый цилиндр G; на нижнем крае его К лежит бронзовое кольцо L с сеткой M и войлоком; на них насыпается слой прокаленной поваренной соли О и сверху кладется еще войлок P со свинцовым кольцом Q; на верхний войлок надавливает груз R. С помощью ручек J фильтрационный цилиндр может легко выниматься для чистки его или осмотра внутренности сосуда. Такой фильтр, смоченный безводным H., не пропускает сквозь себя механически примешанную (эмульсированную) воду, последние же следы влаги (растворенной в Н.) поглощаются поваренной солью; с целью лучшего высушивания — к последней иногда прибавляют высушенный хлористый магний. В кислотной жидкости, отделенной от продукта, с течением времени может образоваться еще небольшое количество Н.; поэтому эта жидкость, прежде чем пустить ее на переработку для извлечения HNO 3 и Н 2 SО 4, подвергается предварительному отстаиванию (около недели) в больших сепараторах, устроенных подобно вышеописанному; всплывающий Н. время от времени сливается и подвергается обычному промыванию. С другой стороны, спускаемые промывные воды также уносят c собой некоторое количество продукта механически; для отделения и улавливания мелко раздробленного в этих водах Н., их пропускают через длинный свинцовый ящик с поперечными перегородками, снабженными вырезами попеременно, то внизу, то вверху (фиг. 4).
Относительно извлекаемого при этих обеих операциях Н. нужно заметить, что он требует особенно тщательной промывки, так как в нем именно накопляются вышеупомянутые вредные низшие нитропродукты.
т. е. образуется: водяной пар, углекислота, азот и кислород. Этот кислород стараются утилизировать в динамитах (см.) с деятельным поглотителем. Отсутствие окиси углерода делает продукты взрыва совершенно безвредными, что особенно ценно при подземных взрывных работах. Об объеме образующихся газов, количестве отделяющегося тепла, скорости распространения взрыва в больших зарядах, силе и т. п. см. соотв. статью По отношению к различным химическим реагентам Н. содержится подобно другим азотным эфирам: щелочами обмыливается, кислотами разлагается с выделением азотной кислоты, восстановителями превращается обратно в глицерин с выделением окиси азота или аммиака. Для открытия самых малых количеств Н. прибавляют к испытуемой жидкости анилина и концентрированной серной кислоты: получается пурпурово-красное окрашивание, которое при разбавлении водой переходит в зеленое (Вербер).
Н. (мед.). При вдыхании паров, равно как после смазывания языка, Н., в малых дозах, вызывает головную боль, тошноту, головокружение, ощущение жара и учащенное сердцебиение; после внутреннего употребления более значительных доз наблюдались головная боль, дрожание, мышечная слабость, доходившая до полного паралича, отдышка, в некоторых случаях смертельного отравления — резкое расстройство дыхания, синюха и глубокое угнетение нервной системы. Несмотря на эти опасные свойства, Н., употребляющийся в гомеопатии при различных нервных заболеваниях (под названием «глоноина»), сравнительно недавно предложен как средство против невралгий, в особенности против припадков грудной жабы; далее, препарат этот испробован при бронхиальной астме, в некоторых случаях мигрени, при падучей, пляске св. Витта, и при остром и хроническом воспалении почек. Н. назначают по 0,0002 — 0,001 г несколько раз в день или в каплях, от 1 до 5 капель в 1% масляном или алкогольном растворе; средство это приготовляют также в пастилках.




